Clear Sky Science · de
Proteomweite Vorhersage der funktionellen Auswirkungen von Missense-Varianten mit ProteoCast
Warum winzige Mutationen für Gesundheit und Krankheit wichtig sind
Jeder Mensch trägt unzählige kleine DNA-Veränderungen, doch nur einige dieser Feinheiten stören die Funktion unserer Proteine und tragen zu Krankheiten bei. Harmlosen Unterschieden von gefährlichen zu unterscheiden ist eine gewaltige Herausforderung, besonders jetzt, wo wir Genome mit Werkzeugen wie CRISPR bearbeiten können. Diese Studie stellt ProteoCast vor, eine rechnerische Methode, die die Evolutionsgeschichte selbst nutzt, um vorherzusagen, welche einzelbuchstabenartigen Änderungen in Proteinen vermutlich von Bedeutung sind, und zeigt, dass sie im Prinzip die gesamte Proteinsammlung eines Organismus auf einmal durchsuchen kann.

Die Spur der Evolution in Proteinen lesen
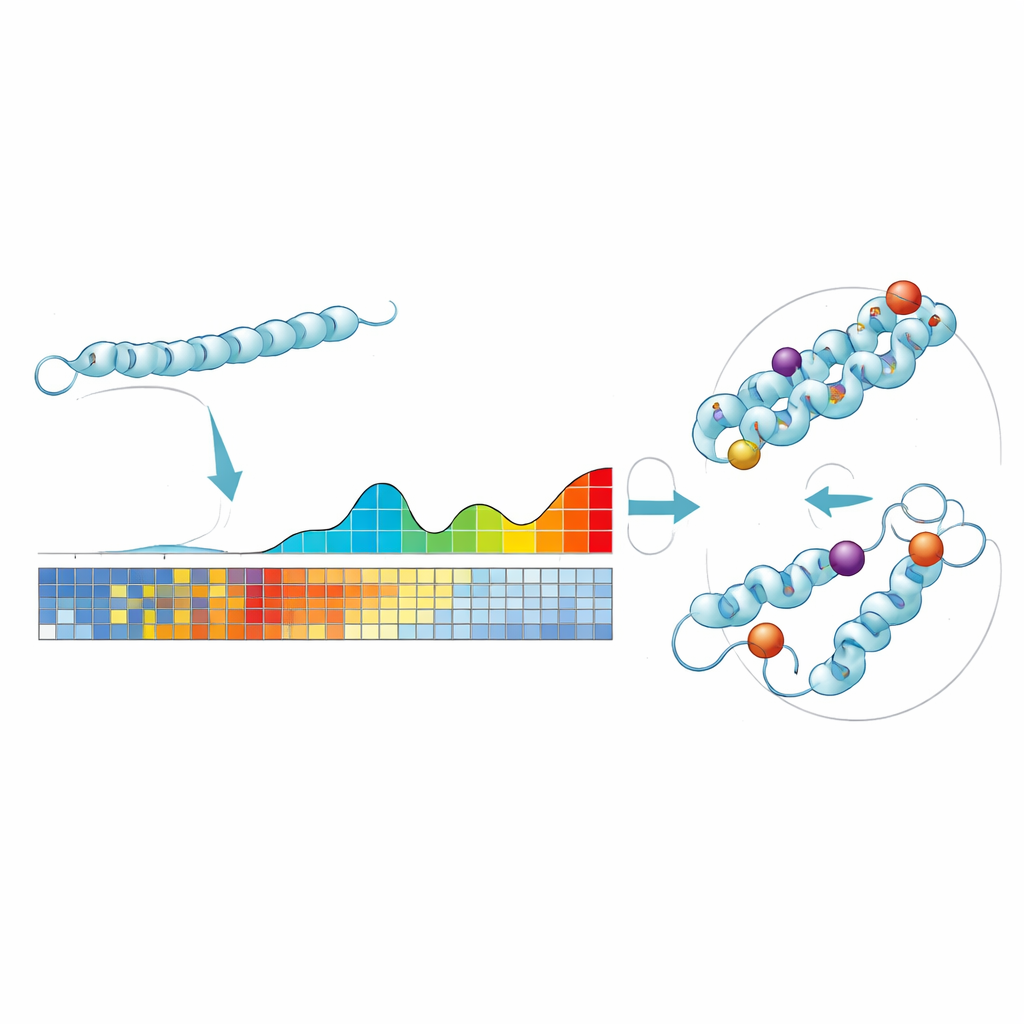
ProteoCast baut auf einer einfachen Idee auf: Wenn eine bestimmte Position in einem Protein über hunderte Millionen Jahre kaum verändert wurde, ist eine Änderung heute eher schädlich. Die Autoren speisen jede Fruchtfliegen-Proteinsequenz in große evolutionäre Datenbanken ein, um verwandte Proteine aus vielen Arten zu sammeln. Mit diesen Daten schätzt ProteoCast ab, wie störend jede mögliche Aminosäuresubstitution an jeder Position wäre und erstellt so eine „mutationale Landschaft“ für dieses Protein. Die Methode ordnet die vorhergesagten Änderungen dann drei einprägsamen Kategorien zu—neutral, mild wirkend oder stark wirkend—und bezeichnet außerdem jede Position im Protein als entweder tolerant oder sensitiv gegenüber Mutationen.
Vorhersagen am ganzen Tier getestet
Das Team wandte ProteoCast auf praktisch das gesamte Proteom der Fruchtfliege Drosophila melanogaster an, deckte mehr als 22.000 Proteinformen und etwa 300 Millionen mögliche Missense-Mutationen ab. Sie verglichen ProteoCasts Vorhersagen mit fast 400.000 bekannten genetischen Varianten, darunter natürliche Unterschiede aus wilden und inzüchtigen Fliegenpopulationen sowie experimentell untersuchte Mutationen, die teilweise Funktionsverlust oder vollständige Letalität verursachen. ProteoCast erkannte etwa 85 % der letalen Mutationen und 73 % der partiellen Funktionsverluste korrekt als mild oder stark wirkend, während die große Mehrheit der Populationsvarianten als neutral klassifiziert wurde. Mit anderen Worten: Das Muster evolutionärer Konservierung allein erwies sich als hochinformativ dafür, welche Änderungen die Fitness des gesamten Organismus beeinträchtigen.
Von Computerwerten zur realen Genom-Editierung
Um zu prüfen, ob ProteoCasts Ergebnisse Experimente leiten können, nutzten die Autoren sie, um gezielt einzelne Aminosäureänderungen für die Genom-Editierung in Fliegen auszuwählen. Sie konzentrierten sich auf ein Enzym, das an der Produktion von NAD beteiligt ist, einem wichtigen metabolischen Cofaktor. ProteoCast identifizierte mehrere Substitutionen nahe dem aktiven Zentrum oder der Dimerisierungsoberfläche des Enzyms als stark wirkend, und andere Substitutionen in Oberflächenbereichen als neutral, selbst wenn sie Chemie oder Größe der Aminosäure drastisch veränderten. Wurden diese fünf Mutationen per CRISPR eingeführt, führten die drei als schädlich vorhergesagten zu rezessiver Entwicklungsletalität, während die zwei als neutral vorhergesagten gesunde Fliegen ergaben—im Einklang mit den rechnerischen Vorhersagen.
Verborgene Kontrollschalter in flexiblen Bereichen finden
Viele wichtige Regulationsstellen in Proteinen liegen in „unstrukturierten“ Regionen, die eher herumflattern als stabile 3D-Formen anzunehmen, was sie schwer zu untersuchen macht. ProteoCast projiziert seine Mutationsscores auf 3D-Modelle von AlphaFold und segmentiert dann jedes Protein in Regionen ähnlicher Sensitivität. Regionen, in denen ein Cluster von Positionen ungewöhnlich sensitiv ist, entsprechen oft Bindungsmotiven oder Hotspots für posttranslationale Modifikationen—subtile Kontrollschalter, die die Aktivität eines Proteins feinjustieren. Im gesamten Fliegenproteom überlapppten ProteoCasts hochsensitiven Segmente mit den meisten bekannten kurzen linearen Motiven und einem großen Teil der Modifikationsstellen und hoben außerdem zuvor nicht annotierte Segmente hervor, die wahrscheinlich an Regulation oder Protein–Protein-Interaktionen beteiligt sind.
Weitreichende Bedeutung über Fruchtfliegen hinaus
Obwohl die Arbeit sich auf Fruchtfliegen konzentriert, ist das Prinzip hinter ProteoCast allgemein: Die Evolution kodiert reichhaltige Informationen darüber, welche Positionen in einem Protein ohne Folgen verändert werden können und welche kritisch sind. Die Autoren zeigen, dass dasselbe Konzept auch bei menschlichen Krankheitsvarianten und bei kuratierten Sätzen regulatorischer Stellen aus Hefe sowie intrinsisch ungeordneten Bindungsregionen gut funktioniert. Da es schnell, skalierbar ist und keine teure Hardware erfordert, kann ProteoCast auf jede Art mit verfügbaren Proteinsequenzdaten angewendet werden. Für Nicht‑Spezialisten lautet die Kernbotschaft: Indem wir die Evolution zum Experimentator machen, gewinnen wir eine leistungsfähige, genomweite Karte jener winzigen genetischen Änderungen, die am wahrscheinlichsten für Gesundheit, Krankheit und künftige Therapien von Bedeutung sind.
Zitation: Abakarova, M., Freiberger, M.I., Liehrmann, A. et al. Proteome-wide prediction of the functional impact of missense variants with ProteoCast. Nat Commun 17, 3813 (2026). https://doi.org/10.1038/s41467-026-72140-1
Schlüsselwörter: Missense-Mutationen, Proteinevolution, Drosophila, Vorhersage von Variantenwirkungen, funktionelle Genomik