Clear Sky Science · sv
Fc-fria enkedjade antikropps-mRNA-terapier för luftvägsinfektion med flerdrogresistent Pseudomonas aeruginosa
Varför denna forskning är viktig för vardagshälsa
Antibiotikaresistenta infektioner dödar redan mer än en miljon människor varje år, och dödstalen förväntas inom några decennier konkurrera med eller överstiga cancer. En av värsta bovarna är Pseudomonas aeruginosa, en sjukhusassocierad bakterie som angriper lungorna hos patienter på ventilator, personer med cystisk fibros och dem med försvagat immunförsvar. Denna studie undersöker ett nytt sätt att bekämpa dessa farliga infektioner utan att förlita sig på traditionella antibiotika: att använda budbärar-RNA (mRNA) för att förvandla kroppen till en fabrik för små, mycket målinriktade antibakteriella antikroppar.
Ett nytt sätt att stärka kroppens försvar
I stället för att ge patienter färdiga antikroppar—som är dyra och tidskrävande att tillverka—paketerade forskarna genetiska instruktioner för ett specialiserat antikroppsfragment i små lipidnanopartiklar, liknande dem som användes i mRNA-vacciner mot COVID-19. När dessa partiklar injiceras i blodet transporteras de huvudsakligen till levern och mjälten, där celler läser av mRNA:t och börjar producera ett enkedjat antikroppsfragment som känner igen en nyckelstruktur på P. aeruginosa. Denna struktur, kallad typ III-sekretion systemet, är en mikroskopisk nål som bakterien använder för att injicera toxiner i lungceller. Genom att blockera denna nål neutraliserar antikroppen bakteriens mest destruktiva vapen i stället för att försöka döda mikroben direkt. 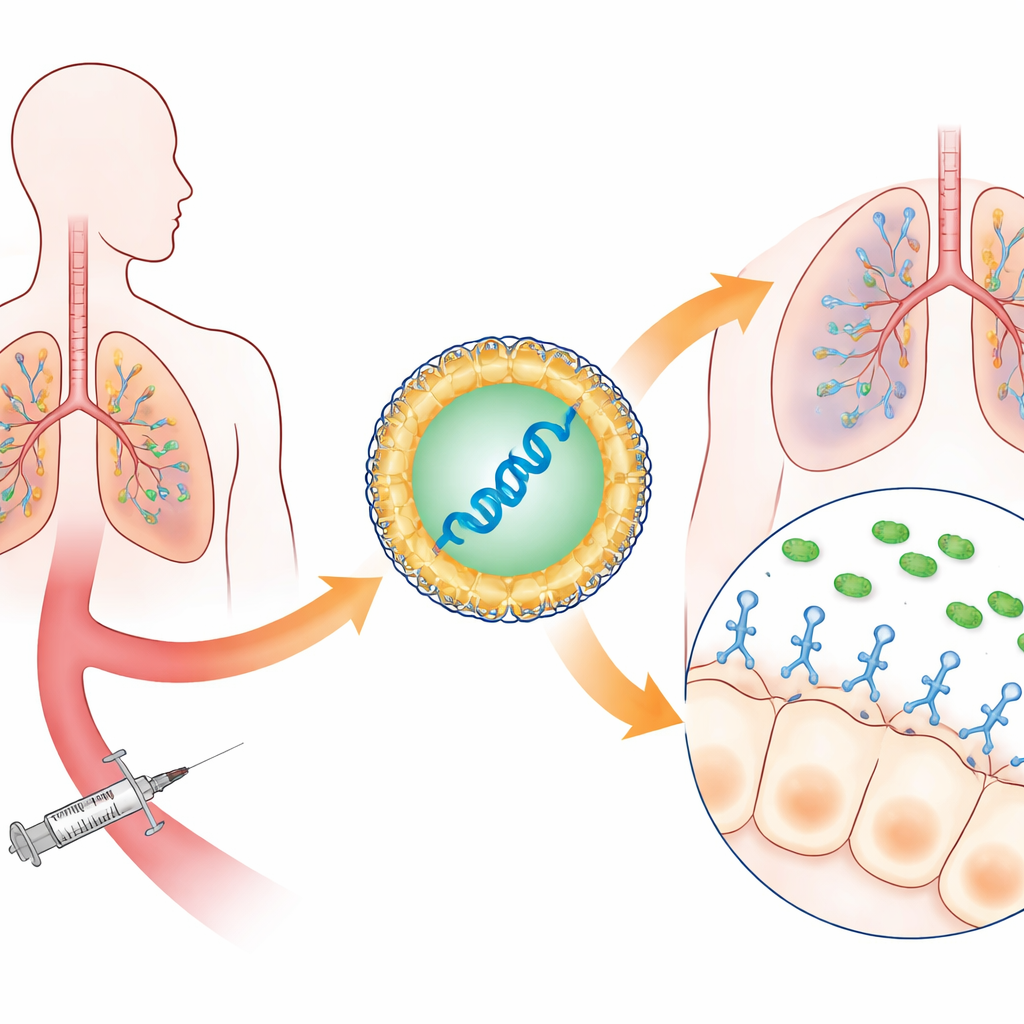
Skydda lungorna före och efter infektion
Teamet testade sin metod på möss som exponerades för dödliga doser av P. aeruginosa levererade direkt till luftvägarna. När mRNA-terapin gavs strax före infektion överlevde nästan alla möss som fick instruktionerna för den antibakteriella antikroppen, medan majoriteten av de obehandlade djuren dog inom en dag. De behandlade mössen hade mindre lungödem, färre bakterier i lungor och blod, och dramatiskt lägre nivåer av inflammatoriska molekyler kopplade till akut lungskaada. Terapin fungerade också när den gavs efter att infektionen redan börjat, vilket är en mer realistisk situation för behandling av inneliggande patienter. I dessa behandlingsliknande experiment var överlevnadsgraderna med den mRNA-producerade antikroppen lika höga eller bättre än de som uppnåddes med bästa tillgängliga antikroppsproteinterapi.
Överträffar antibiotika mot svåra sjukhusstammar
P. aeruginosa som finns i verkliga sjukhus är ofta mycket mer varierade och läkemedelsresistenta än standardstammar i labbet. För att efterlikna denna kliniska verklighet samlade forskarna tio resistenta stammar från patienter och testade dem, tillsammans med två labbstammar, i möss vars immunsystem medvetet försvagats. Många av dessa isolat bar en särskilt destruktiv toxingen kallad exoU och var resistenta mot flera antibiotikaklasser, inklusive karbapenemer, aminoglykosider och fluorokinoloner. Även i denna tuffa miljö—och vid bakteriella doser som pålitligt dödade kontrollgrupper—förbättrade den mRNA-producerade antikroppen överlevnaden avsevärt, särskilt mot de mest toxiska, flerdrogresistenta stammarna. I vissa fall matchade eller överträffade den kolistin, ett sista-handsantibiotikum med betydande biverkningar. När den kombinerades med kolistin räddade mRNA-terapin alla behandlade möss, vilket tyder på att sådana biologiska läkemedel kan förlänga användbarheten hos befintliga antibiotika snarare än att helt ersätta dem.
Små, Fc-fria antikroppar når den infekterade ytan bättre
En central innovation i detta arbete är användningen av ett "Fc-fritt" enkedjat antikroppsfragment, som endast innehåller den verksamma delen som känner igen det bakteriella målet och saknar den skrymmande svans som fullständiga antikroppar använder för att engagera immunceller. Konventionell visdom förespråkar att behålla Fc-svansen eftersom den förlänger cirkulationstiden i blodet. Här jämförde forskarna direkt mRNA som kodar för det lilla fragmentet ensamt med en större version fuserad till en Fc-domän. De fann att medan Fc-bärande formen stannade längre i blodomloppet och organen, korsade det mindre fragmentet mer effektivt från blodet in i det tunna vätskeskikt som täcker lungans luftblåsor—den verkliga slagfältet där bakterierna attackerar. Mätningar av vätska sköljd från luftvägarna visade flera gånger högre nivåer av det lilla fragmentet än av Fc-fuserad antikropp, trots att dess blodnivåer var lägre. Denna överlägsna åtkomst till infektionsplatsen förklarar sannolikt varför den Fc-fria versionen gav bättre överlevnad i flera behandlingsmodeller. 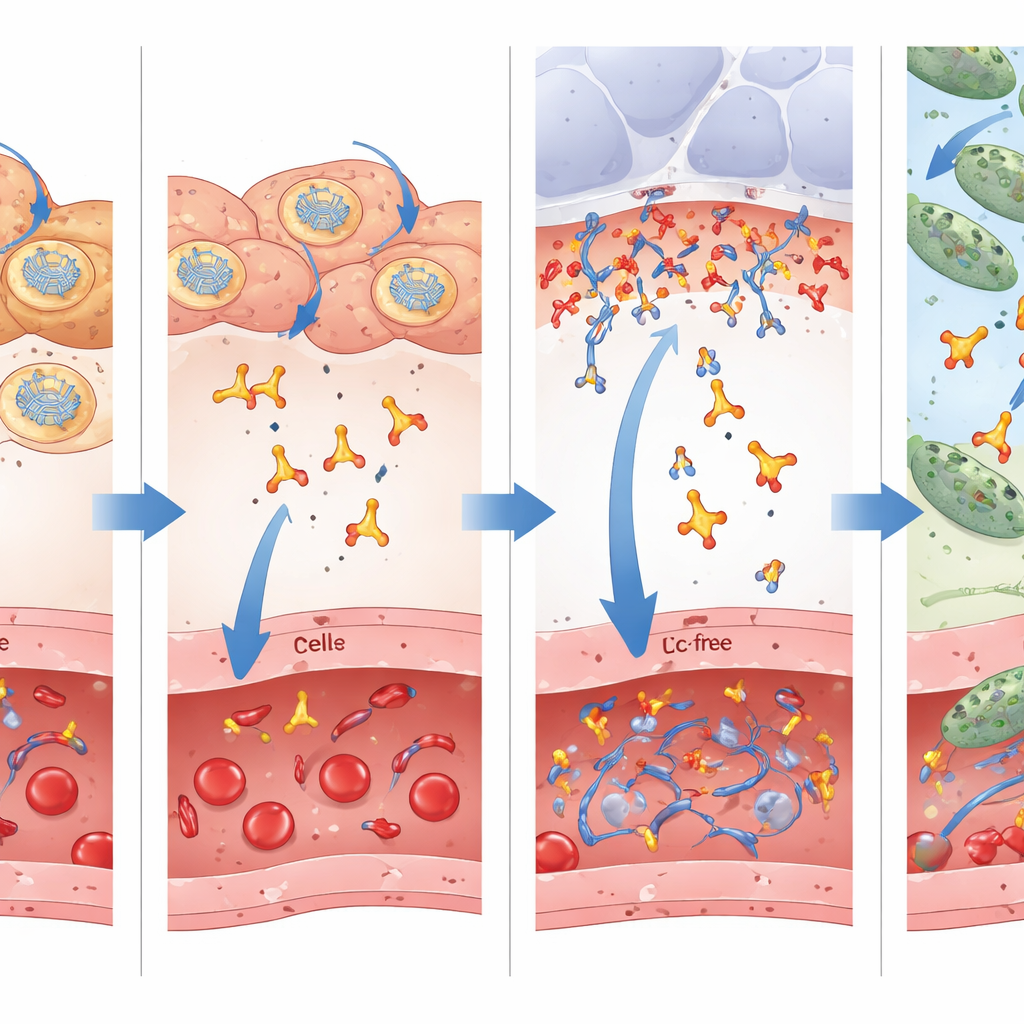
En mångsidig plattform för framtida infektioner
Enkelt uttryckt visar denna studie att en enda injektion av mRNA snabbt kan fylla sårbara lungor med precist riktade, små antikroppsfragment som dämpar de mest skadliga tricksen hos en dödlig, läkemedelsresistent bakterie. Behandlingen minskade inflammation, begränsade bakteriespridning och räddade djur även när deras immunsystem var undertryckta och de infekterande stammarna var resistenta mot standardantibiotika. Eftersom mRNA-tillverkning är snabb och modulär skulle samma strategi i princip kunna anpassas till andra farliga bakterier som använder liknande toxinutleveranssystem. Medan ytterligare arbete krävs för att finslipa dosering, säkerhet och leverans för människor, pekar dessa resultat mot en framtid där läkare snabbt kan "ladda upp" nya försvarsmolekyler i patienter för att hinna före utvecklande mikrober, vilket erbjuder ett kraftfullt nytt verktyg mot den växande krisen med antimikrobiell resistens.
Citering: Kinoshita, M., Kawaguchi, K., Mochida, Y. et al. Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa. Nat Commun 17, 2960 (2026). https://doi.org/10.1038/s41467-026-71040-8
Nyckelord: antimikrobiell resistens, mRNA-terapier, Pseudomonas aeruginosa, antikroppsfragment, lunginfektion