Clear Sky Science · ar
علاج mRNA بأجسام مضادة أحادية السلسلة خالية من Fc لالتهابات طرق الهواء بـ Pseudomonas aeruginosa المقاومة لعدة أدوية
لماذا يهم هذا البحث للصحة اليومية
تسبب العدوى المقاومة للمضادات الحيوية بالفعل في وفاة أكثر من مليون شخص سنوياً، ويتوقع أن يصل عدد الوفيات إلى مستوى يساوي أو يتجاوز السرطان خلال عقود قليلة. أحد أخطر المسببات هو Pseudomonas aeruginosa، بكتيريا تقطن المستشفيات وتهاجم رئات المرضى على أجهزة التنفس الاصطناعي، والأشخاص المصابين بالتليف الكيسي، ومن لديهم ضعف في المناعة. تستكشف هذه الدراسة طريقة جديدة لمحاربة هذه العدوى الخطيرة دون الاعتماد على المضادات الحيوية التقليدية: استخدام الحمض الريبي المرسال (mRNA) لتحويل جسم المريض إلى مصنع لصناعة أجسام مضادة صغيرة وموجهة بدقة ضد البكتيريا.
طريقة جديدة لتسليح دفاعات الجسم
بدلاً من حقن المرضى بأجسام مضادة جاهزة — والتي تكون مكلفة وبطيئة التصنيع — وضع الباحثون تعليمات جينية لشظية متخصصة من جسم مضاد داخل جزيئات شحمية نانوية صغيرة، مشابهة لتلك المستخدمة في لقاحات mRNA ضد كوفيد-19. بعد الحقن في مجرى الدم، تنتقل هذه الجزيئات أساساً إلى الكبد والطحال، حيث تقرأ الخلايا الـ mRNA وتبدأ بصنع شظية جسم مضاد أحادية السلسلة تتعرف على بنية رئيسية في P. aeruginosa. تسمى هذه البنية نظام الإفراز من النمط الثالث، وهي إبرة مجهرية تستخدمها البكتيريا لحقن السموم في خلايا الرئة. عن طريق حجب هذه الإبرة، يحيد الجسم المضاد أخطر سلاح للبكتيريا بدلاً من محاولة قتل الميكروب مباشرة. 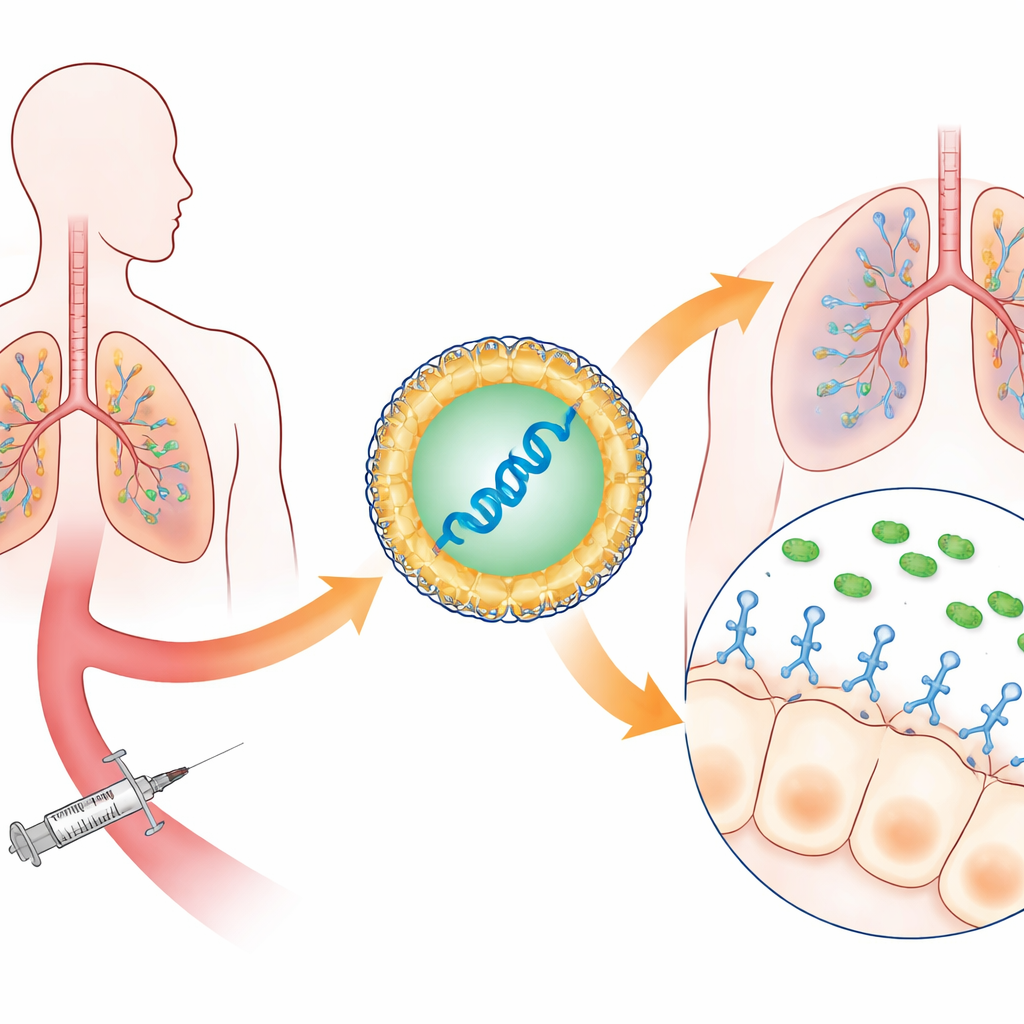
حماية الرئتين قبل وبعد العدوى
اختبر الفريق نهجهم في الفئران التي تعرَّضت لجرعات قاتلة من P. aeruginosa وُضِعت مباشرة في المجاري الهوائية. عندما أُعطي علاج الـ mRNA قبل العدوى بوقت قصير، نجت الفئران التي تلقت تعليمات الجسم المضاد المضاد للبكتيريا بشكل شبه كامل، بينما مات معظم الحيوانات غير المعالجة خلال يوم واحد. أظهرت الفئران المعالجة انخفاضاً في تورم الرئة، وعدداً أقل من البكتيريا في رئتيها ودمها، وانخفاضاً كبيراً في مستويات الجزيئات الالتهابية المرتبطة بإصابة الرئة الحادة. عمل العلاج أيضاً عندما عُطي بعد بدء العدوى، وهو نموذج أكثر واقعية لعلاج المرضى المحتجزين في المستشفى. في هذه التجارب العلاجية، كانت معدلات النجاة مع الجسم المضاد المنتج بواسطة الـ mRNA مساوية أو متفوقة على تلك التي تحققت باستخدام أفضل علاجات بروتينات الأجسام المضادة المتاحة.
تفوق على المضادات الحيوية ضد سلالات المستشفيات الصعبة
غالباً ما تكون P. aeruginosa الموجودة في المستشفيات متنوعة ومقاومة للأدوية أكثر بكثير من السلالات المعيارية المخبرية. لمحاكاة هذه الواقع السريري، جمع الباحثون عشرة سلالات مقاومة من مرضى واختبروها، إلى جانب سلالتين مخبريتين، في فئران أُضعِفت أجهزتها المناعية عمداً. حملت العديد من هذه العينات جين سم خطير يسمى exoU وكانت مقاومة لعدة فئات من المضادات الحيوية، بما في ذلك الكاربابينيمات، والأمينوغليكوزيدات، والفلوروكينولونات. حتى في هذا الوضع القاسي — وعلى جرعات بكتيرية كانت تقتل الحيوانات الضابطة بشكل موثوق — حسّن الجسم المضاد المنتج بواسطة الـ mRNA بشكل كبير معدلات البقاء، وخاصة ضد السلالات الأكثر سمية والمقاومة لعدة أدوية. في حالات معينة، كان أداءه مساوياً أو متفوقاً على الكولستين، وهو مضاد حيوي يُستخدم كملاذ أخير وله آثار جانبية كبيرة. عند الدمج مع الكولستين، أنقذت معالجة الـ mRNA جميع الفئران المعالجة، مما يشير إلى أن مثل هذه الأدوية البيولوجية قد تطيل العمر المفيد للمضادات الحيوية الحالية بدلاً من استبدالها كلياً.
الأجسام المضادة الصغيرة الخالية من Fc تصل إلى السطح المصاب بشكل أفضل
ابتكار رئيسي في هذا العمل هو استخدام شظية جسم مضاد أحادية السلسلة «خالية من Fc»، التي تحتوي على النهاية العاملة فقط التي تتعرف على الهدف البكتيري وتفتقر إلى الذيل الضخم الذي تستخدمه الأجسام المضادة الكاملة للتفاعل مع خلايا المناعة. التقليد السائد يفضل الاحتفاظ بذيل Fc لأنه يطيل زمن الدورة في الدم. هنا قارن الباحثون مباشرةً بين mRNA الذي يشفر الشظية الصغيرة وحدها وبين نسخة أكبر مدموجة مع مجال Fc. وجدوا أنه بينما بقيت النسخة الحاملة لـ Fc لفترة أطول في مجرى الدم والأعضاء، عبرت الشظية الصغيرة بكفاءة أكبر من الدم إلى طبقة السائل الرقيقة التي تغطي الحويصلات الهوائية في الرئة — ساحة المعركة الفعلية حيث تهاجم البكتيريا. أظهرت قياسات السائل المغسول من الممرات الهوائية مستويات أعلى بعدة أضعاف من الشظية الصغيرة مقارنةً بالجسم المضاد المدموج مع Fc، على الرغم من أن مستوياتها في الدم كانت أقل. من المرجح أن يفسر هذا الوصول المتفوق إلى موقع العدوى لماذا أعطت النسخة الخالية من Fc نجاة أفضل في نماذج علاجية متعددة. 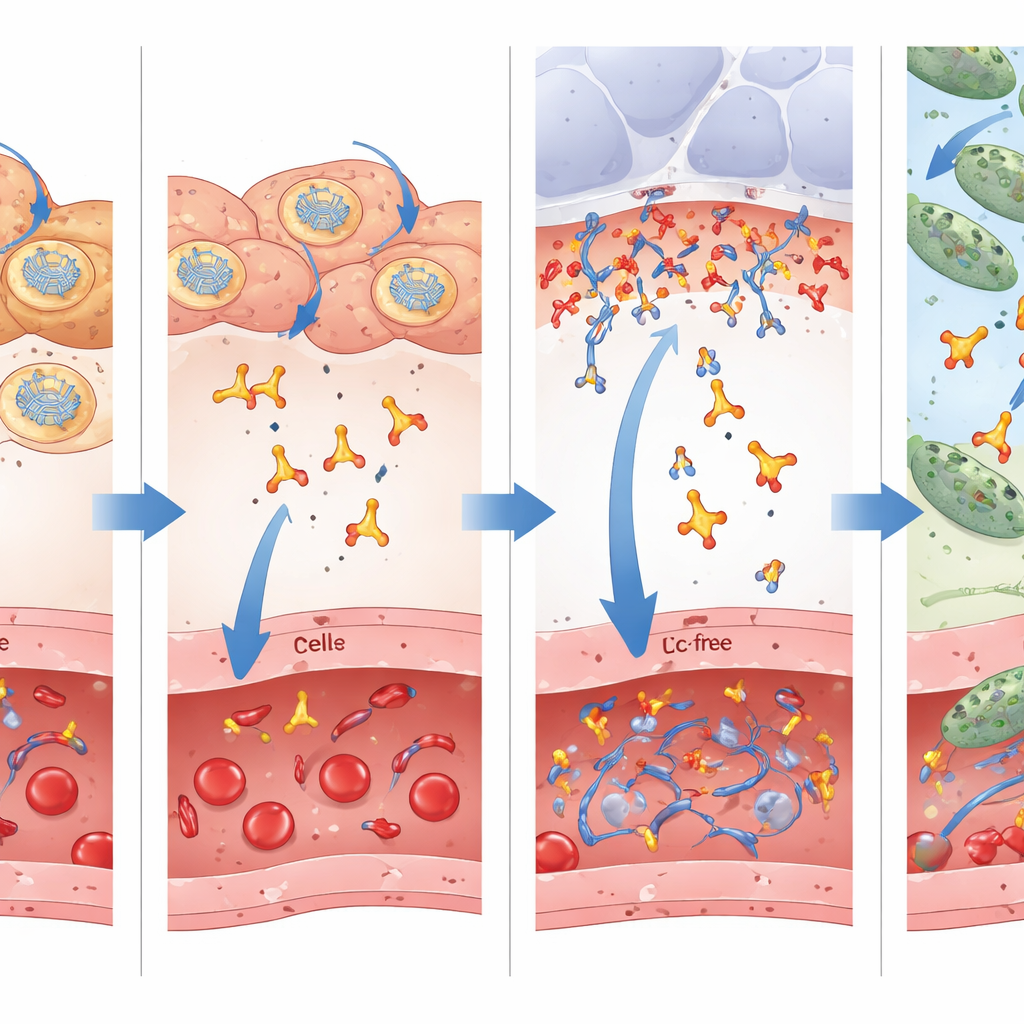
منصة مرنة للعدوى المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أن حقنة واحدة من mRNA يمكنها بسرعة أن تغمر الرئتين الضعيفة بشظايا أجسام مضادة صغيرة وموجهة بدقة تقلل من أكثر حيل البكتيريا المقاومة للأدوية تدميراً. خفّض العلاج الالتهاب، وقلّل انتشار البكتيريا، وأنقذ الحيوانات حتى عندما كانت أجهزتها المناعية مكبوتة وكانت السلالات المسببة مقاومة للمضادات الحيوية القياسية. وبما أن تصنيع الـ mRNA سريع وذو طابع وحدوي، يمكن تكييف الاستراتيجية نفسها من حيث المبدأ مع بكتيريا خطيرة أخرى تستخدم أنظمة توصيل السموم المماثلة. بينما هناك حاجة إلى مزيد من العمل لصقل الجرعات والسلامة وطرق التوصيل للإنسان، تشير هذه النتائج إلى مستقبل يمكن للأطباء فيه «تحميل» جزيئات دفاعية جديدة بسرعة إلى المرضى لمواكبة تطور الميكروبات، مما يوفر أداة قوية ضد الأزمة المتصاعدة لمقاومة العوامل الميكروبية.
الاستشهاد: Kinoshita, M., Kawaguchi, K., Mochida, Y. et al. Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa. Nat Commun 17, 2960 (2026). https://doi.org/10.1038/s41467-026-71040-8
الكلمات المفتاحية: مقاومة العوامل الميكروبية, علاجات mRNA, Pseudomonas aeruginosa, شظايا الأجسام المضادة, التهاب الرئة