Clear Sky Science · ru
Терапия мРНК, кодирующая одноцепочечный антителообразный фрагмент без Fc, при инфекции дыхательных путей мультирезистентным Pseudomonas aeruginosa
Почему это исследование важно для повседневного здоровья
Инфекции, устойчивые к антибиотикам, уже уносят более миллиона жизней в год, и ожидается, что число смертей в ближайшие десятилетия сопоставится или превзойдёт рак. Одним из худших виновников является Pseudomonas aeruginosa — бактериальный обитатель больниц, который поражает лёгкие пациентов на вентиляторах, людей с муковисцидозом и лиц с ослабленным иммунитетом. В этом исследовании рассматривается новый способ борьбы с такими опасными инфекциями без опоры на традиционные антибиотики: использование матричной (м)РНК для превращения организма в фабрику по производству маленьких, строго нацеленных антибактериальных антител.
Новый способ вооружить защиту организма
Вместо инфузии пациентам готовых антител — дорогостоящих и медленно производимых — исследователи упаковали генетические инструкции для специализированного фрагмента антитела в липидные наночастицы, подобные тем, что используются в мРНК-вакцинах от COVID-19. После введения в кровоток эти частицы преимущественно попадают в печень и селезёнку, где клетки считывают мРНК и начинают синтез одноцепочечного фрагмента антитела, распознающего ключевую структуру P. aeruginosa. Эта структура, называемая системой секреции типа III, представляет собой микроскопическую «иглу», которой бактерия инъецирует токсины в клетки лёгких. Блокируя эту «иглу», антитело нейтрализует самое разрушительное орудие бактерии, не пытаясь непосредственно убить микроорганизм. 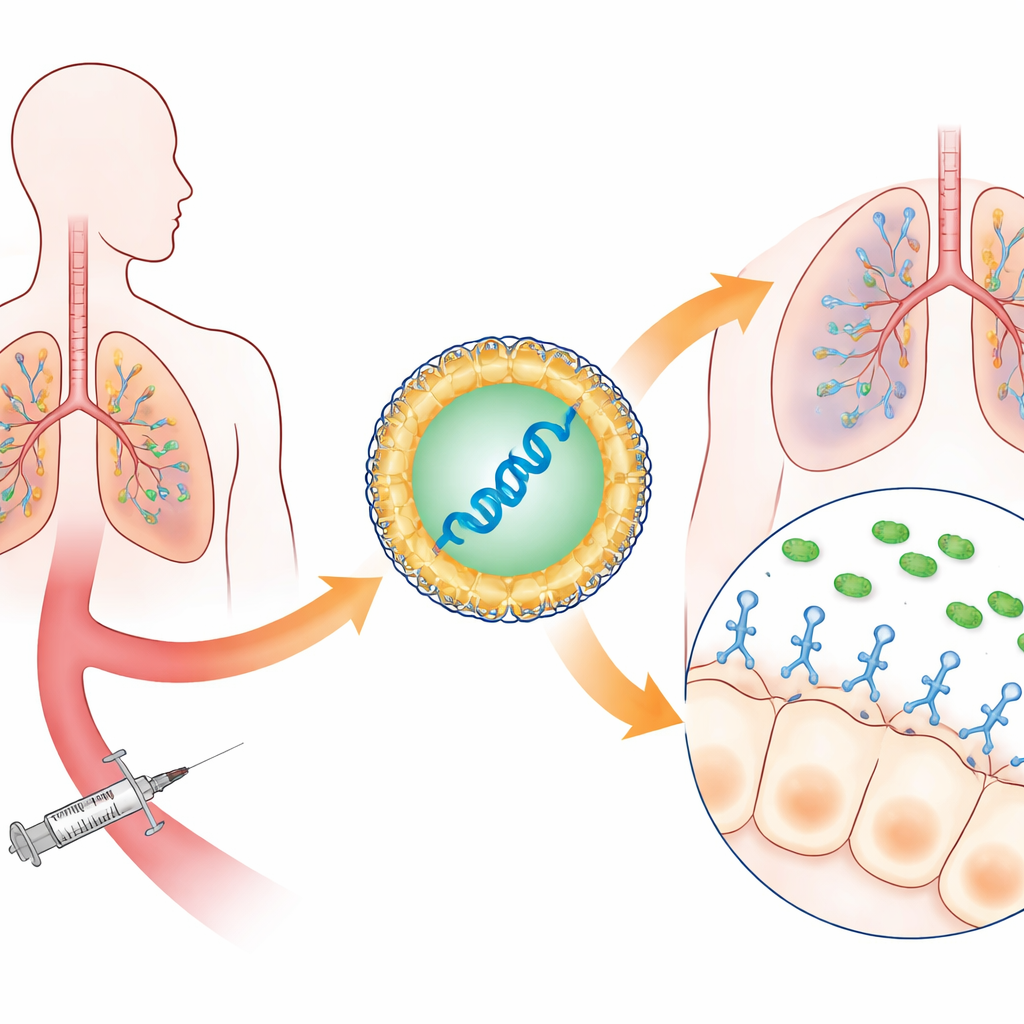
Защита лёгких до и после инфекции
Команда протестировала подход на мышах, которым в дыхательные пути вводили летальные дозы P. aeruginosa. Когда терапию мРНК вводили незадолго до инфицирования, мыши, получившие инструкции для антибактериального антитела, почти все выживали, тогда как большинство нелечённых животных умирали в течение суток. У лечённых мышей отмечалось меньше отёка лёгких, меньше бактерий в лёгких и крови и значительно более низкие уровни воспалительных молекул, ассоциированных с острым повреждением лёгких. Терапия также была эффективна при применении после начала инфекции, что более реалистично для лечения госпитализированных пациентов. В таких лечебных экспериментах показатели выживаемости при использовании мРНК-синтезированного антитела сопоставлялись или превосходили результаты, достигнутые лучшей доступной терапией белковыми антителами.
Превосходство над антибиотиками против тяжёлых госпитальных штаммов
P. aeruginosa, встречающиеся в реальных условиях больниц, часто значительно разнообразнее и устойчивее к лекарствам, чем штаммы лабораторные. Чтобы смоделировать эту клиническую реальность, исследователи собрали десять резистентных штаммов от пациентов и протестировали их вместе с двумя лабораторными штаммами на мышах с искусственно подавленным иммунитетом. Многие из этих изолятов несли особенно разрушительный токсигенный ген exoU и сопротивлялись нескольким классам антибиотиков, включая карбапенемы, аминогликозиды и фторхинолоны. Даже в таких тяжёлых условиях — и при дозах бактерий, которые надёжно убивали контрольных животных — мРНК-синтезированное антитело существенно улучшало выживаемость, особенно против самых токсичных, мультирезистентных штаммов. В некоторых экспериментах оно сравнивалось по эффективности или превосходило колистин, антибиотик последней инстанции с выраженными побочными эффектами. В комбинации с колистином мРНК-терапия спасла всех лечённых мышей, что указывает на то, что такие биологические препараты могут продлить полезность существующих антибиотиков, а не полностью их заменить.
Малые антитела без Fc лучше проникают к месту инфекции
Ключевым новшеством в этой работе является использование одноцепочечного антителообразного фрагмента «без Fc», который содержит лишь функциональную часть, распознающую бактериальную мишень, и лишён массивного хвоста Fc, используемого полными антителами для взаимодействия с иммунными клетками. Традиционная точка зрения отдаёт предпочтение наличию Fc-хвоста, потому что он удлиняет время циркуляции в крови. Здесь исследователи непосредственно сравнили мРНК, кодирующую только маленький фрагмент, с более крупной версией, слитой с доменом Fc. Они обнаружили, что хотя форма с Fc дольше сохранялась в кровотоке и органах, меньший фрагмент эффективнее пересекал барьер из крови в тонкий слой жидкости, покрывающей воздушные мешочки лёгких — фактическую «зону боевых действий», где атакуют бактерии. Измерения жидкости, промытой из дыхательных путей, показали в несколько раз более высокие уровни малого фрагмента по сравнению с Fc-связанным антителом, несмотря на более низкие уровни в крови. Это лучшее проникновение к месту инфекции, вероятно, объясняет, почему версия без Fc обеспечивала лучшую выживаемость в нескольких моделях лечения. 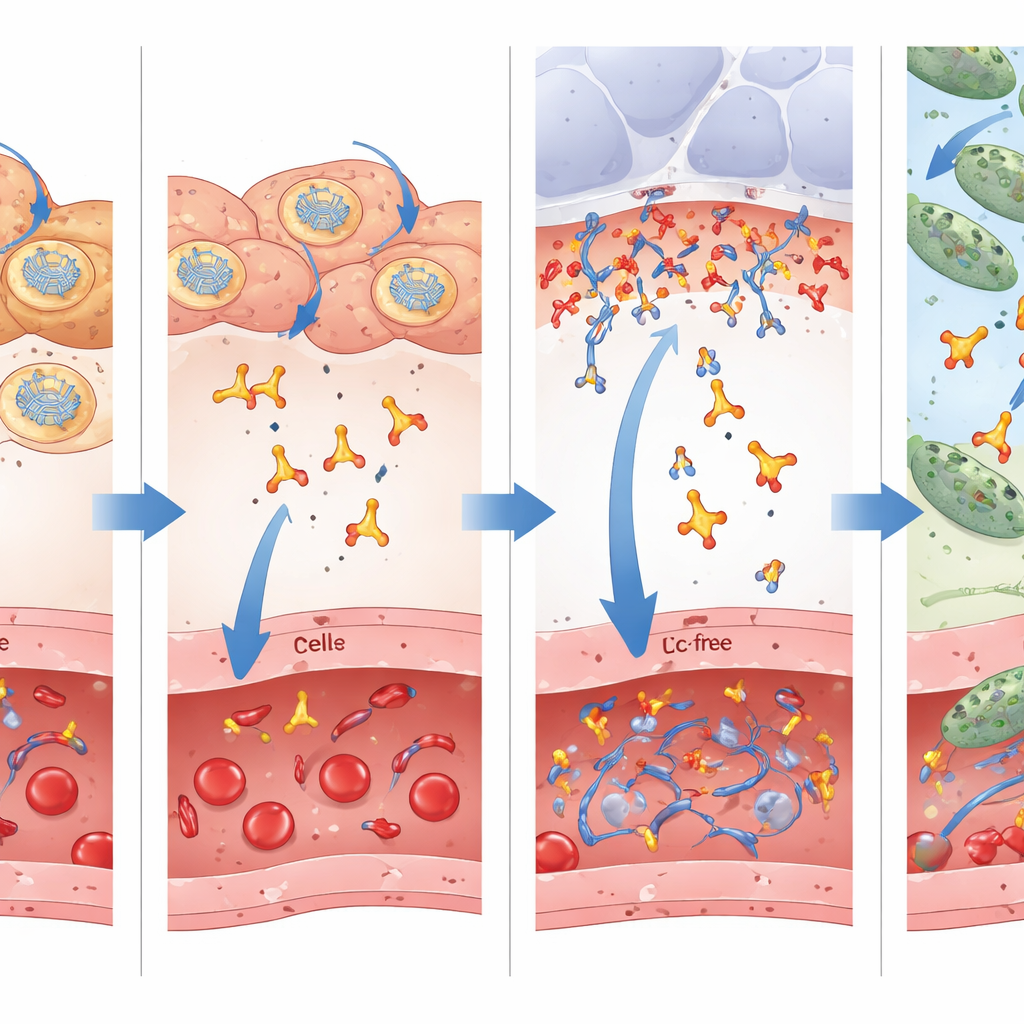
Универсальная платформа для будущих инфекций
Проще говоря, это исследование показывает, что одиночная инъекция мРНК может быстро наполнять уязвимые лёгкие точно нацеленными, малыми фрагментами антител, которые нейтрализуют самые разрушительные приёмы смертельно опасной, лекарственно-устойчивой бактерии. Лечение снижало воспаление, ограничивало распространение бактерий и сохраняло жизнь животным даже при подавленном иммунитете и при штаммах, устойчивых к стандартным антибиотикам. Поскольку производство мРНК быстрое и модульное, ту же стратегию в принципе можно адаптировать к другим опасным бактериям, использующим похожие системы доставки токсинов. Хотя необходимы дальнейшие работы по уточнению дозирования, безопасности и способов доставки для людей, эти результаты указывают на будущее, в котором врачи смогут оперативно «загружать» в организм пациентов новые защитные молекулы, чтобы опережать эволюцию микробов, предоставляя мощный новый инструмент против растущего кризиса антимикробной резистентности.
Цитирование: Kinoshita, M., Kawaguchi, K., Mochida, Y. et al. Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa. Nat Commun 17, 2960 (2026). https://doi.org/10.1038/s41467-026-71040-8
Ключевые слова: антибактериальная резистентность, мРНК-терапевтика, Pseudomonas aeruginosa, фрагменты антител, инфекция лёгких