Clear Sky Science · pl
mRNA-terapia pojedynczego łańcucha przeciwciała bez fragmentu Fc na infekcje dróg oddechowych wywołane wielolekoopornym Pseudomonas aeruginosa
Dlaczego to badanie ma znaczenie dla codziennego zdrowia
Infekcje oporne na antybiotyki już dziś zabijają ponad milion osób rocznie, a prognozy wskazują, że liczba zgonów w ciągu kilku dekad może dorównywać lub przewyższać te wywoływane przez nowotwory. Jednym z najgroźniejszych sprawców jest Pseudomonas aeruginosa — bakteryjny patogen szpitalny atakujący płuca pacjentów poddanych wentylacji mechanicznej, osoby z mukowiscydozą oraz osoby z osłabionym układem odpornościowym. Badanie to przedstawia nowe podejście do zwalczania tych niebezpiecznych infekcji, które nie polega na tradycyjnych antybiotykach: użycie mRNA, by przemienić organizm w fabrykę małych, wysoce ukierunkowanych przeciwbakteryjnych przeciwciał.
Nowy sposób uzbrojenia obrony organizmu
Zamiast podawać pacjentom gotowe przeciwciała — które są drogie i czasochłonne w produkcji — badacze zamknęli instrukcje genetyczne dla wyspecjalizowanego fragmentu przeciwciała w drobnych lipidowych nanocząsteczkach podobnych do tych stosowanych w szczepionkach mRNA przeciw COVID-19. Po wstrzyknięciu do krwiobiegu cząsteczki te trafiają głównie do wątroby i śledziony, gdzie komórki odczytują mRNA i zaczynają produkować fragment przeciwciała jednolancuchowego rozpoznający kluczową strukturę P. aeruginosa. Ta struktura, zwana systemem wydzielania typu III, działa jak mikroskopijna igła, której bakteria używa do wstrzykiwania toksyn do komórek płuc. Blokując tę igłę, przeciwciało unieszkodliwia najbardziej destrukcyjną broń bakterii, zamiast próbować zabić drobnoustrój bezpośrednio. 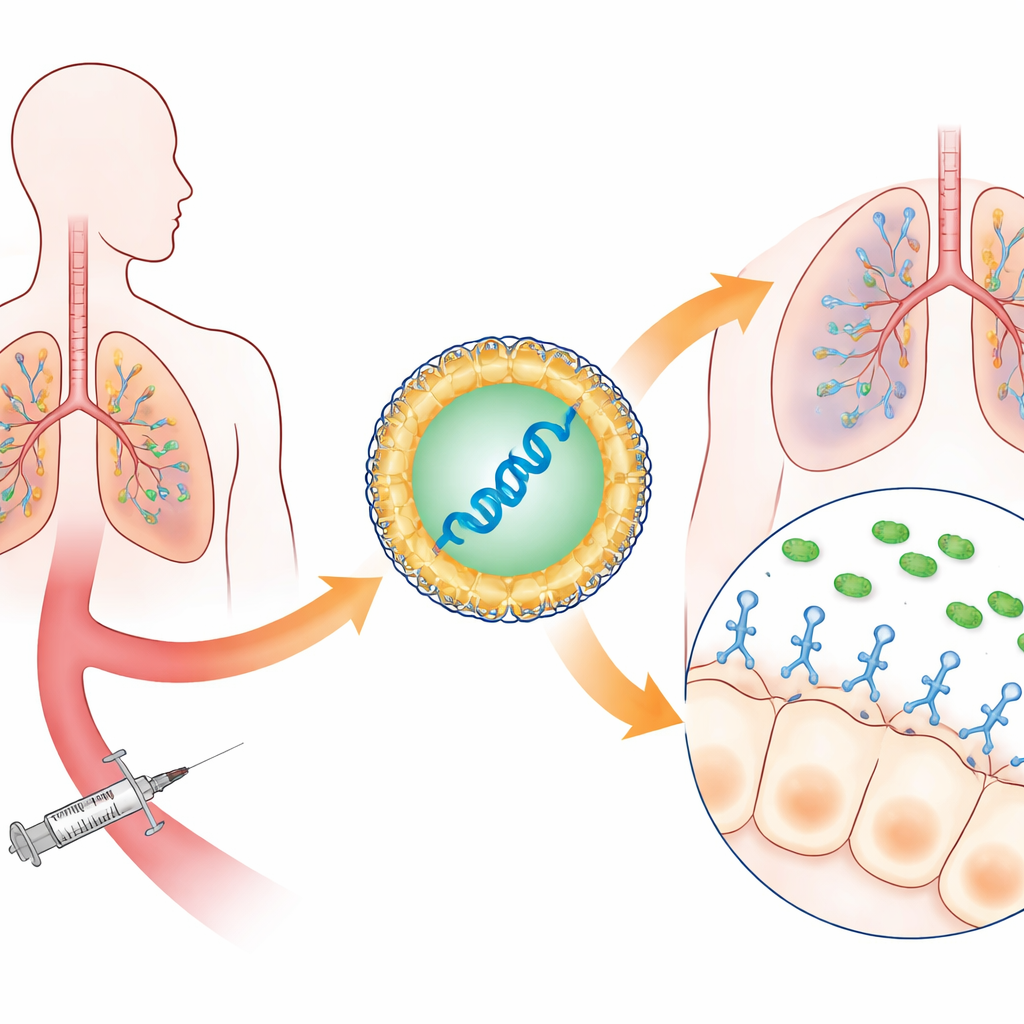
Ochrona płuc przed i po zakażeniu
Zespół przetestował swoje podejście na myszach wystawionych na śmiertelne dawki P. aeruginosa podane bezpośrednio do dróg oddechowych. Kiedy terapię mRNA podano krótko przed zakażeniem, myszy otrzymujące instrukcje do produkcji przeciwbakteryjnego przeciwciała przeżywały niemal w całości, podczas gdy większość zwierząt nieleczonych ginęła w ciągu doby. Leczone myszy miały mniej obrzęku płuc, mniejszą liczbę bakterii w płucach i krwi oraz dramatycznie niższe stężenia cząsteczek zapalnych związanych z ostrym uszkodzeniem płuc. Terapia działała też po rozpoczęciu zakażenia, co jest bardziej realistycznym modelem leczenia pacjentów hospitalizowanych. W tych eksperymentach leczniczych wskaźniki przeżycia dzięki przeciwciału produkowanemu z mRNA dorównywały lub przewyższały te uzyskane przy najlepszych dostępnych terapii białkowymi przeciwciałami.
Przewyższanie antybiotyków wobec opornych szczepów szpitalnych
Szczepy P. aeruginosa występujące w rzeczywistych szpitalach są często znacznie bardziej zróżnicowane i oporne na leki niż standardowe szczepy laboratoryjne. Aby odzwierciedlić tę kliniczną rzeczywistość, badacze zebrali dziesięć szczepów opornych od pacjentów i przetestowali je, wraz z dwoma szczepami laboratoryjnymi, na myszach z celowo osłabionym układem odpornościowym. Wiele z tych izolatów nosiło szczególnie destrukcyjne geny toksyn, takie jak exoU, i wykazywało oporność na kilka klas antybiotyków, w tym karbapenemy, aminoglikozydy i fluorochinolony. Nawet w tym surowym ustawieniu — i przy dawkach bakteryjnych, które niezawodnie zabijały zwierzęta kontrolne — przeciwciało produkowane z mRNA znacząco poprawiało przeżywalność, szczególnie wobec najbardziej toksycznych, wielolekoopornych szczepów. W niektórych przypadkach dorównywało lub przewyższało kolistynę, antybiotyk stosowany w ostateczności, obarczony istotnymi skutkami ubocznymi. W połączeniu z kolistyną terapia mRNA uratowała wszystkie leczone myszy, co sugeruje, że takie biologiczne leki mogą wydłużyć przydatność istniejących antybiotyków, zamiast je całkowicie zastępować.
Małe przeciwciała bez Fc lepiej docierają do zakażonej powierzchni
Kluczową innowacją w tej pracy jest użycie fragmentu przeciwciała jednolancuchowego „bez Fc”, który zawiera jedynie część odpowiedzialną za rozpoznanie celu bakteryjnego i pozbawiony jest masywnego ogona, którego pełne przeciwciała używają do angażowania komórek odpornościowych. Konwencjonalna mądrość przemawia za zachowaniem fragmentu Fc, ponieważ wydłuża on czas krążenia we krwi. Badacze porównali bezpośrednio mRNA kodujące sam mały fragment z większą wersją połączoną z domeną Fc. Stwierdzili, że choć forma z Fc pozostawała dłużej w krwiobiegu i narządach, to mniejszy fragment skuteczniej przechodził z krwi do cienkiej warstwy płynu pokrywającej pęcherzyki płucne — rzeczywistego pola walki, gdzie atakują bakterie. Pomiary płynu zmywanego z dróg oddechowych wykazały wielokrotnie wyższe stężenia małego fragmentu niż przeciwciała z Fc, mimo niższych poziomów we krwi. Lepszy dostęp do miejsca zakażenia prawdopodobnie tłumaczy, dlaczego wersja bez Fc dawała lepsze przeżycie w kilku modelach leczenia. 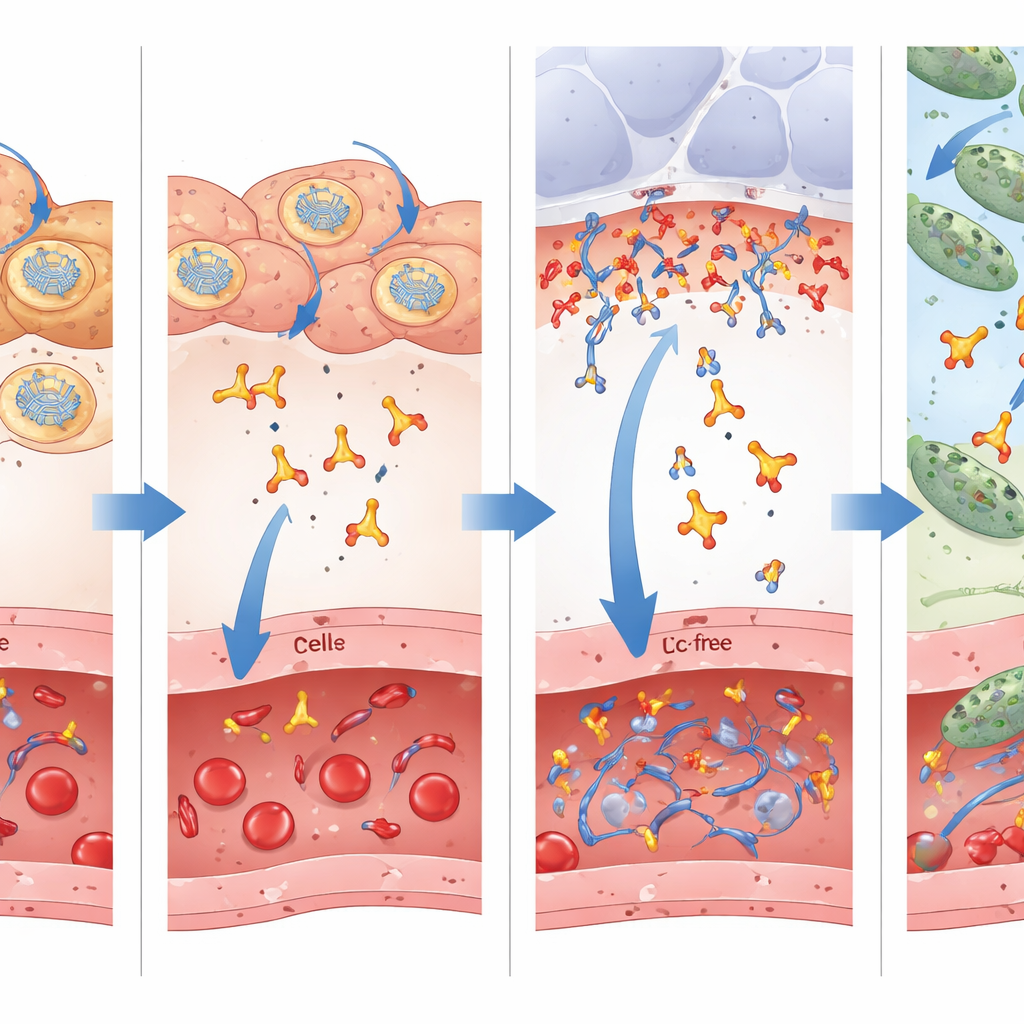
Wszechstronna platforma na przyszłe infekcje
W prostych słowach to badanie pokazuje, że pojedyncze wstrzyknięcie mRNA może szybko nasycić podatne płuca precyzyjnie ukierunkowanymi, małymi fragmentami przeciwciał, które tłumią najbardziej szkodliwe sztuczki śmiertelnie niebezpiecznej, lekoopornej bakterii. Leczenie zmniejszało stan zapalny, ograniczało rozprzestrzenianie się bakterii i ratowało zwierzęta nawet wtedy, gdy ich układ odpornościowy był przytłumiony, a szczepy infekcyjne wykazywały oporność na standardowe antybiotyki. Ponieważ produkcja mRNA jest szybka i modułowa, tę samą strategię w zasadzie można by dostosować do innych groźnych bakterii wykorzystujących podobne systemy dostarczania toksyn. Choć konieczne są dalsze prace nad dawkowaniem, bezpieczeństwem i dostawą u ludzi, wyniki te wskazują na przyszłość, w której lekarze będą mogli szybko „wgrywać” nowe cząsteczki obronne do organizmu pacjenta, by wyprzedzić ewoluujące drobnoustroje — oferując potężne nowe narzędzie przeciw rosnącemu kryzysowi oporności na środki przeciwdrobnoustrojowe.
Cytowanie: Kinoshita, M., Kawaguchi, K., Mochida, Y. et al. Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa. Nat Commun 17, 2960 (2026). https://doi.org/10.1038/s41467-026-71040-8
Słowa kluczowe: oporność na środki przeciwdrobnoustrojowe, terapie mRNA, Pseudomonas aeruginosa, fragmenty przeciwciał, zakażenie płuc