Clear Sky Science · nl
Fc-vrije enkelketen antilichaam-mRNA therapie voor luchtweginfectie door multiresistente Pseudomonas aeruginosa
Waarom dit onderzoek van belang is voor de dagelijkse gezondheid
Antibioticaresistente infecties doden al meer dan een miljoen mensen per jaar, en de sterftecijfers worden naar verwachting binnen enkele decennia vergelijkbaar met of hoger dan die van kanker. Een van de ergste boosdoeners is Pseudomonas aeruginosa, een ziekenhuisbacterie die de longen aanvalt van patiënten aan beademing, mensen met cystische fibrose en mensen met een verzwakt immuunsysteem. Deze studie onderzoekt een nieuwe manier om deze gevaarlijke infecties te bestrijden zonder afhankelijk te zijn van traditionele antibiotica: gebruik van boodschapper-RNA (mRNA) om het lichaam te veranderen in een fabriek voor kleine, hooggerichtte antibacteriële antilichamen.
Een nieuwe manier om de afweer van het lichaam te bewapenen
In plaats van patiënten met kant-en-klare antilichamen te infuseren—die duur zijn en traag te produceren—verpakten de onderzoekers genetische instructies voor een gespecialiseerd antilichaamfragment in kleine lipidenanodeeltjes, vergelijkbaar met die in mRNA-COVID-19-vaccins. Eenmaal in de bloedbaan reizen deze deeltjes vooral naar de lever en de milt, waar cellen het mRNA lezen en beginnen met het produceren van een enkelketen antilichaamfragment dat een sleutelstructuur van P. aeruginosa herkent. Deze structuur, het type III-secretiesysteem, is een microscopische naald die de bacterie gebruikt om toxines in longcellen te injecteren. Door deze naald te blokkeren neutraliseert het antilichaam het meest destructieve wapen van de bacterie in plaats van te proberen de microbe direct te doden. 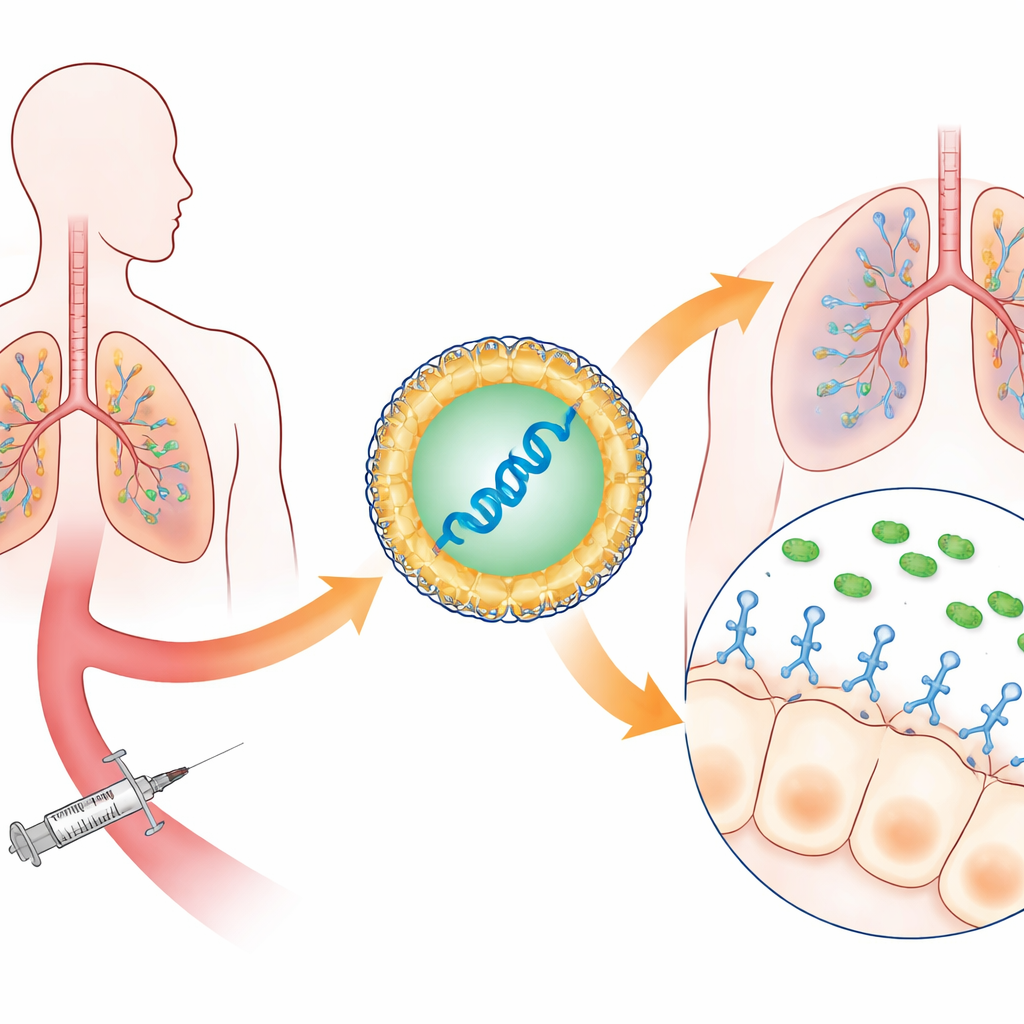
Longen beschermen vóór en na infectie
Het team testte hun aanpak bij muizen die werden blootgesteld aan dodelijke doses P. aeruginosa die rechtstreeks in de luchtwegen werden toegediend. Wanneer de mRNA-therapie kort voor infectie werd gegeven, overleefden de muizen die de instructies voor het antibacteriële antilichaam ontvingen vrijwel volledig, terwijl de meeste onbehandelde dieren binnen een dag stierven. De behandelde muizen hadden minder longzwelling, minder bacteriën in hun longen en bloed, en dramatisch lagere niveaus van ontstekingsmoleculen die geassocieerd worden met acute longaandoening. De therapie werkte ook wanneer ze werd gegeven nadat de infectie al was begonnen, een realistischer model voor de behandeling van opgenomen patiënten. In deze behandelexperimenten waren de overlevingspercentages met het mRNA-geproduceerde antilichaam gelijk aan of beter dan die behaald met de beste beschikbare antilichaamproteïnetherapie.
Beter dan antibiotica tegen hardnekkige ziekenhuisstammen
P. aeruginosa die in echte ziekenhuizen wordt gevonden, is vaak veel diverser en antibioticaresistenter dan standaard laboratoriummodellen. Om deze klinische realiteit na te bootsen verzamelden de onderzoekers tien resistente stammen van patiënten en testten die, samen met twee labstammen, in muizen waarvan het immuunsysteem opzettelijk was onderdrukt. Veel van deze isolaten droegen een bijzonder destructief toxinegen genaamd exoU en waren resistent tegen meerdere antibiotische klassen, waaronder carbapenemen, aminoglycosiden en fluoroquinolonen. Zelfs in deze zware omstandigheden—en bij bacteriële doses die de controledieren betrouwbaar deden sterven—verbeterde het mRNA-geproduceerde antilichaam de overleving aanzienlijk, vooral tegen de meest toxische, multiresistente stammen. In sommige gevallen evenaarde of overtrof het de werking van colistine, een redmiddel-antibioticum met aanzienlijke bijwerkingen. In combinatie met colistine redde de mRNA-therapie alle behandelde muizen, wat suggereert dat dergelijke biologische geneesmiddelen de bruikbare levensduur van bestaande antibiotica kunnen verlengen in plaats van ze volledig te vervangen.
Kleine, Fc-vrije antilichamen bereiken het geïnfecteerde oppervlak beter
Een belangrijke innovatie in dit werk is het gebruik van een “Fc-vrij” enkelketen antilichaamfragment, dat alleen het herkenningsdeel bevat dat het bacteriële doel herkent en niet de omvangrijke staart (Fc) die volledige antilichamen gebruiken om immuuncellen te betrekken. De conventionele opvatting is dat het Fc-deel behouden moet blijven omdat het de circulatietijd in het bloed verlengt. De onderzoekers vergeleken hier direct mRNA dat enkel het kleine fragment codeert met een grotere versie die gefuseerd is met een Fc-domein. Ze ontdekten dat hoewel de Fc-bevattende vorm langer in de bloedbaan en organen bleef, het kleinere fragment efficiënter overstak van bloed naar de dunne vloeistoflaag die de longblaasjes bekleedt—het daadwerkelijke strijdtoneel waar de bacteriën aanvallen. Metingen van vloeistof gewassen uit de luchtwegen toonden meerdere malen hogere niveaus van het kleine fragment dan van het Fc-gefuseerde antilichaam, ook al waren de bloedniveaus lager. Deze superieure toegang tot de infectieplaats verklaart waarschijnlijk waarom de Fc-vrije versie betere overleving gaf in meerdere behandelmodellen. 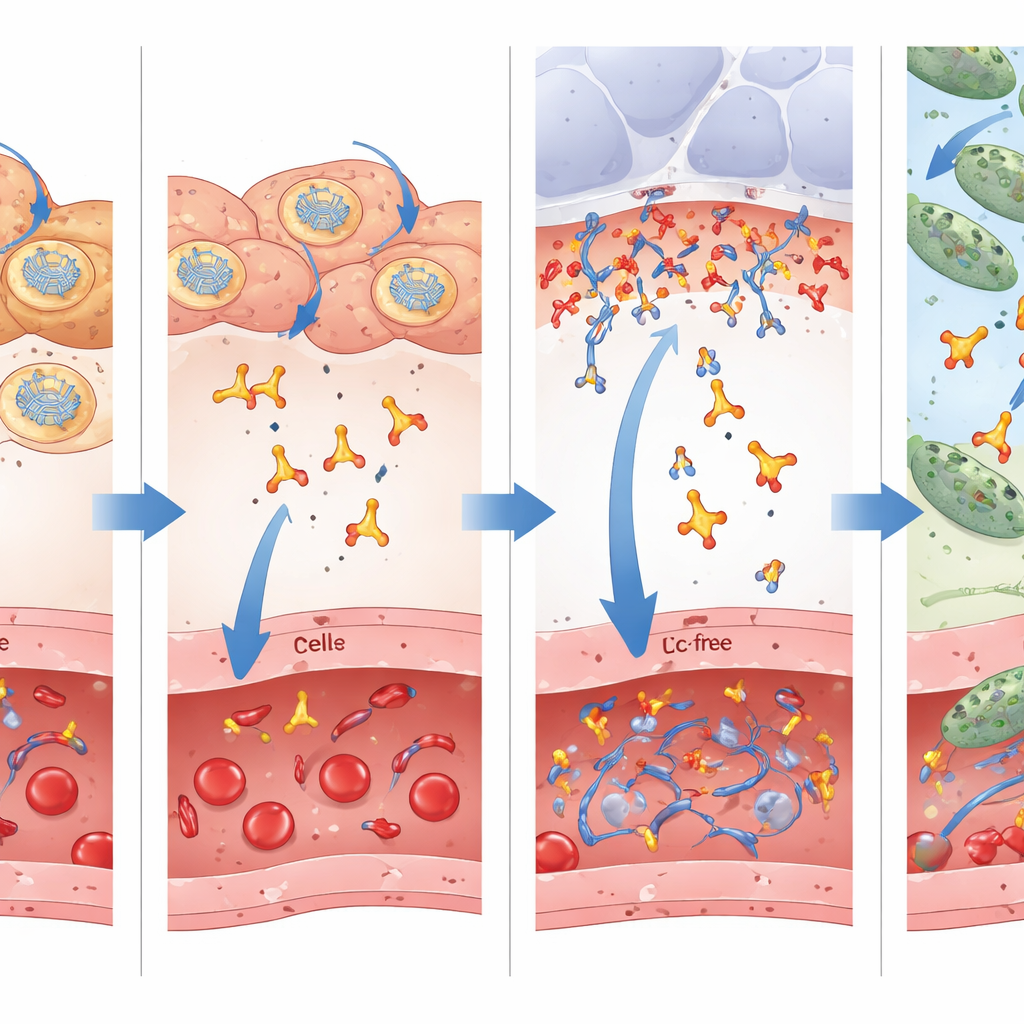
Een veelzijdig platform voor toekomstige infecties
In eenvoudige bewoordingen laat deze studie zien dat een enkele injectie met mRNA kwetsbare longen snel kan vullen met precies gerichte, kleine antilichaamfragmenten die de meest schadelijke trucs van een dodelijke, medicijnresistente bacterie afzwakken. De behandeling verminderde ontsteking, beperkte verspreiding van bacteriën en redde dieren zelfs wanneer hun immuunsystemen onderdrukt waren en de infectieuze stammen resistent waren tegen standaardantibiotica. Omdat mRNA-productie snel en modulair is, zou dezelfde strategie in principe aangepast kunnen worden aan andere gevaarlijke bacteriën die vergelijkbare toxine-afgiftesystemen gebruiken. Hoewel aanvullend werk nodig is om dosissetting, veiligheid en levering voor mensen te verfijnen, wijzen deze resultaten op een toekomst waarin artsen snel nieuwe verdedigingsmoleculen in patiënten kunnen "uploaden" om zich te verzetten tegen evoluerende microben en zo een krachtig nieuw hulpmiddel bieden tegen de groeiende crisis van antimicrobiële resistentie.
Bronvermelding: Kinoshita, M., Kawaguchi, K., Mochida, Y. et al. Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa. Nat Commun 17, 2960 (2026). https://doi.org/10.1038/s41467-026-71040-8
Trefwoorden: antimicrobiële resistentie, mRNA-therapeutica, Pseudomonas aeruginosa, antilichaamfragmenten, longinfectie