Clear Sky Science · de
Fc-freie einzelkettige Antikörper-mRNA-Therapie für Atemwegsinfektionen durch multiresistente Pseudomonas aeruginosa
Warum diese Forschung für die tägliche Gesundheit wichtig ist
Antibiotikaresistente Infektionen töten bereits jetzt mehr als eine Million Menschen pro Jahr, und die Zahl der Todesfälle könnte innerhalb weniger Jahrzehnte mit der von Krebs vergleichbar sein oder diese sogar übertreffen. Einer der schlimmsten Übeltäter ist Pseudomonas aeruginosa, ein Krankenhauskeim, der die Lungen von beatmeten Patientinnen und Patienten, Menschen mit Mukoviszidose und Immunschwächen befällt. Diese Studie untersucht einen neuen Ansatz zur Bekämpfung dieser gefährlichen Infektionen ohne klassische Antibiotika: die Nutzung von Boten-RNA (mRNA), um den Körper zu einer Fabrik für winzige, hochspezifische antibakterielle Antikörper werden zu lassen.
Eine neue Art, die Abwehrkräfte des Körpers zu rüsten
Anstatt Patientinnen und Patienten mit fertigen Antikörpern zu behandeln — die teuer und zeitaufwendig in der Herstellung sind — verpackten die Forschenden die genetische Anleitung für ein spezialisiertes Antikörperfragment in winzige Lipid-Nanopartikel, ähnlich denen in mRNA-COVID-19-Impfstoffen. Nach der Injektion in den Blutkreislauf gelangen diese Partikel hauptsächlich in Leber und Milz, wo Zellen die mRNA ablesen und ein einzelkettiges Antikörperfragment produzieren, das eine Schlüsselstruktur von P. aeruginosa erkennt. Diese Struktur, das Typ-III-Sekretionssystem, ist eine mikroskopische Nadel, mit der das Bakterium Toxine in Lungenzellen injiziert. Indem diese Nadel blockiert wird, neutralisiert der Antikörper die zerstörerischste Waffe des Bakteriums, statt zu versuchen, das Mikroorganismus direkt abzutöten. 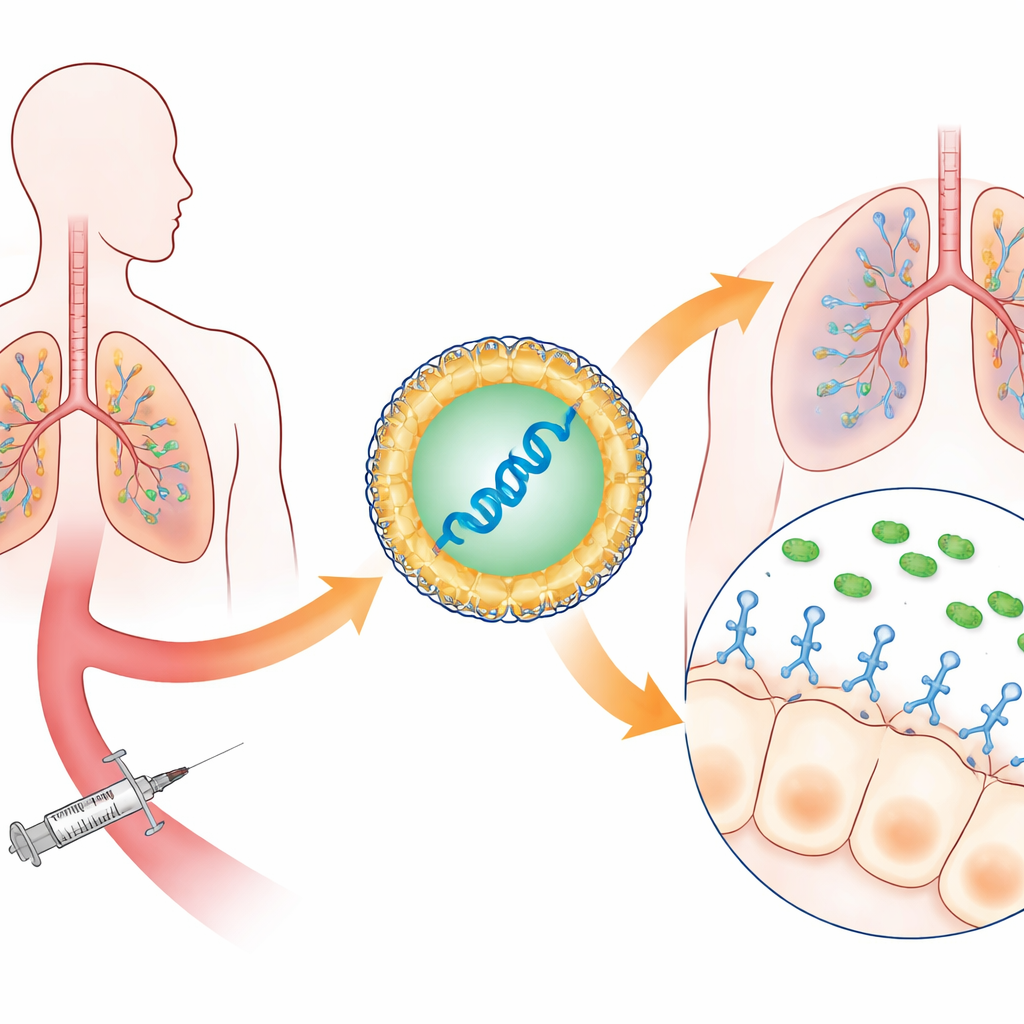
Schutz der Lungen vor und nach der Infektion
Das Team testete seinen Ansatz an Mäusen, denen tödliche Dosen von P. aeruginosa direkt in die Atemwege verabreicht wurden. Wurde die mRNA-Therapie kurz vor der Infektion gegeben, überlebten die Mäuse, die die Anweisungen für den antibakteriellen Antikörper erhielten, nahezu vollständig, während die meisten unbehandelten Tiere innerhalb eines Tages starben. Die behandelten Mäuse zeigten weniger Lungenödem, weniger Bakterien in Lunge und Blut sowie dramatisch niedrigere Spiegel entzündlicher Moleküle, die mit akutem Lungenversagen in Verbindung stehen. Die Therapie wirkte auch, wenn sie nach Beginn der Infektion verabreicht wurde — ein realistischeres Szenario für die Behandlung hospitalisierter Patientinnen und Patienten. In diesen behandlungsähnlichen Experimenten lagen die Überlebensraten mit dem mRNA-produzierten Antikörper auf dem Niveau oder über denen der besten verfügbaren Antikörperprotein-Therapie.
Besser als Antibiotika gegen hartnäckige Krankenhausstämme
In echten Krankenhäusern vorkommende P. aeruginosa-Stämme sind oft deutlich vielfältiger und resistenter gegen Medikamente als Standard-Laborstämme. Um diese klinische Realität nachzubilden, sammelten die Forschenden zehn resistente Stämme von Patientinnen und Patienten und testeten diese zusammen mit zwei Laborstämmen in Mäusen mit gezielt geschwächtem Immunsystem. Viele dieser Isolate trugen ein besonders zerstörerisches Toxin-Gen namens exoU und waren gegen mehrere Antibiotikaklassen resistent, darunter Carbapeneme, Aminoglykoside und Fluorchinolone. Selbst unter diesen harten Bedingungen — und bei bakteriellen Dosen, die Kontrolltiere zuverlässig töteten — verbesserte der mRNA-produzierte Antikörper das Überleben deutlich, insbesondere gegen die toxischsten, multiresistenten Stämme. In einigen Fällen entsprach seine Wirkung der von Colistin oder war sogar überlegen; Colistin ist ein Reserveantibiotikum mit erheblichen Nebenwirkungen. In Kombination mit Colistin rettete die mRNA-Therapie alle behandelten Mäuse, was darauf hindeutet, dass solche biologischen Medikamente die Nutzungsdauer vorhandener Antibiotika verlängern könnten, anstatt sie vollständig zu ersetzen.
Kleine, Fc-freie Antikörper erreichen die infizierte Oberfläche besser
Eine zentrale Innovation dieser Arbeit ist die Verwendung eines „Fc-freien“ einzelkettigen Antikörperfragments, das nur den Erkennungsanteil enthält und den sperrigen Schwanz (Fc-Region) weglässt, mit dem Vollantikörper Immunzellen ansprechen. Konventionelle Auffassung spricht oft dafür, die Fc-Schwanzregion beizubehalten, weil sie die Verweildauer im Blut verlängert. Die Forschenden verglichen hier direkt mRNA, die nur das kleine Fragment kodiert, mit einer größeren Version, die an eine Fc-Domäne fusioniert war. Sie fanden heraus, dass die Fc-tragende Form zwar länger im Blutkreislauf und in Organen verblieb, das kleinere Fragment jedoch effizienter vom Blut in die dünne Flüssigkeitsschicht überging, die die Lungenbläschen auskleidet — der eigentliche Kampfplatz, an dem die Bakterien angreifen. Messungen der aus den Atemwegen gewaschenen Flüssigkeit zeigten mehrere Male höhere Konzentrationen des kleinen Fragments als des Fc-fusionierten Antikörpers, obwohl dessen Blutspiegel höher waren. Dieser bessere Zugang zur Infektionsstelle erklärt wahrscheinlich, warum die Fc-freie Version in mehreren Behandlungsmodellen zu besseren Überlebensraten führte. 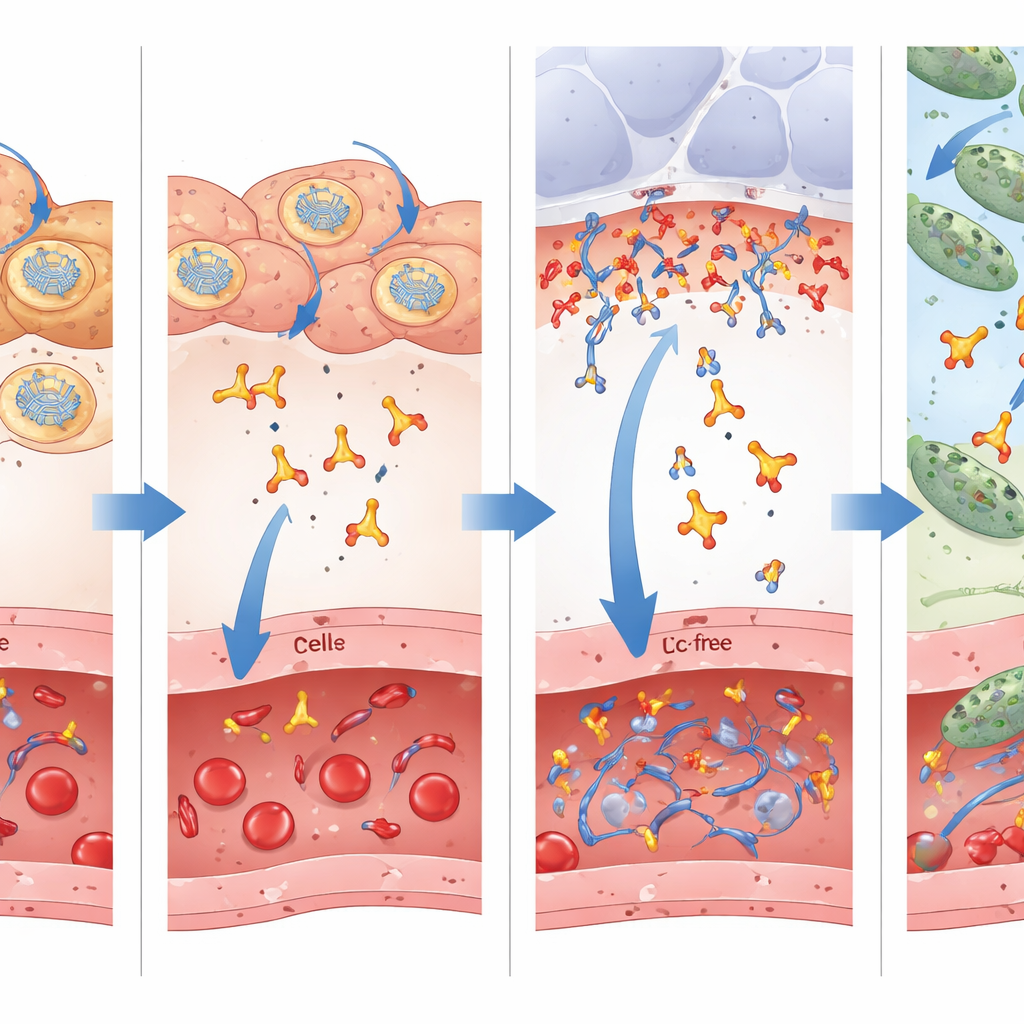
Eine vielseitige Plattform für zukünftige Infektionen
Vereinfacht gesagt zeigt diese Studie, dass eine einzige mRNA-Injektion verletzliche Lungen rasch mit präzise zielgerichteten, kleinen Antikörperfragmenten fluten kann, die die schädlichsten Tricks eines tödlichen, medikamentenresistenten Bakteriums abmildern. Die Behandlung verringerte Entzündungen, begrenzte die Ausbreitung der Bakterien und rettete Tiere selbst bei unterdrücktem Immunsystem und resistenten Stämmen. Da die mRNA-Herstellung schnell und modular ist, könnte die gleiche Strategie prinzipiell auf andere gefährliche Bakterien angewandt werden, die ähnliche Toxin-Übertragungssysteme nutzen. Während weitere Arbeiten nötig sind, um Dosierung, Sicherheit und Verabreichung für den Menschen zu optimieren, deuten diese Ergebnisse auf eine Zukunft hin, in der Ärztinnen und Ärzte neue Abwehrmoleküle rasch in Patientinnen und Patienten „hochladen“ können, um sich entwickelnden Mikroben vorauszueilen — ein mächtiges neues Werkzeug im Kampf gegen die wachsende Krise der antimikrobiellen Resistenz.
Zitation: Kinoshita, M., Kawaguchi, K., Mochida, Y. et al. Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa. Nat Commun 17, 2960 (2026). https://doi.org/10.1038/s41467-026-71040-8
Schlüsselwörter: antimikrobielle Resistenz, mRNA-Therapeutika, Pseudomonas aeruginosa, Antikörperfragmente, Lungeninfektion