Clear Sky Science · sv
Parvis elektrolys möjliggör para-C–H-aminering av fenoler med nitroarenar och mekanistisk visualisering via multifunktionell elektro-kemisk masspektrometri
Att förvandla enkla ringar till användbara molekyler
Kemister förlitar sig på kol–kväve-bindningar för att bygga många av de läkemedel, färgämnen och material vi använder dagligen. Traditionellt kräver dessa kopplingar ädelmetaller, flera reaktionssteg och starka kemikalier. Denna studie introducerar ett mildare, elektricitetdrivet sätt att förena två mycket vanliga byggstenar — fenoler och nitroföreningar — till värdefulla produkter som används i färgämnen, pesticider och bränsleadditiv. Den visar också upp en slags ”direktsändning” av reaktionen på molekylär nivå, fångad med en specialiserad masspektrometrisk uppställning.
Varför denna nya bindningsbildning är viktig
Målmolekylerna i detta arbete, kallade p-hydroxydiphenylaminer, ligger i centrum för många funktionella produkter, från färgämnen till antioxidanter i bränslen. Konventionella vägar till dem börjar ofta från redan reducerade former av nitroföreningar och kräver ofta skyddsgrupper, extra reagenser och metalkatalysatorer. Varje extra steg ökar kostnad, avfall och energianvändning. Författarna sökte en direkt väg att förena en enkel nitroförening med en fenolring i ett enda steg, helst utan dyra metaller eller externa oxiderande och reducerande medel.
Använd elektricitet som den osynliga reagensen
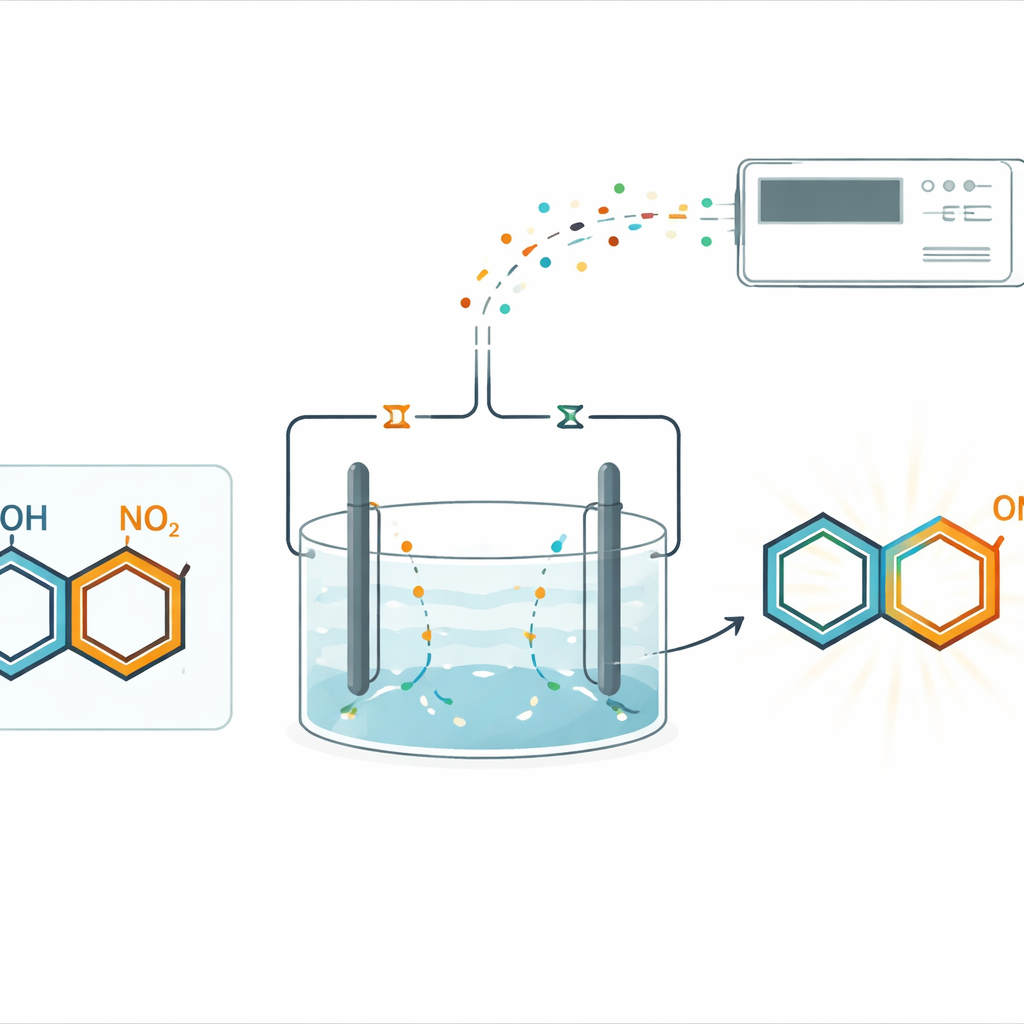
I stället för att förlita sig på flaskade kemikalier för att tillföra eller avlägsna elektroner använde teamet parvis elektrolys i en enda odelad cell. I denna uppställning driver elektrisk ström två kompletterande förändringar samtidigt: reduktion vid en elektrod och oxidation vid den andra. Nitrobärande ringar reduceras försiktigt vid katoden, medan fenoler aktiveras vid anoden. Under noggrant valda förhållanden möts de två aktiverade partnerna och bildar en ny kol–kväve-bindning på en bestämd position på fenolringen, känd som para-stället. Detta tillvägagångssätt undviker metalkatalysatorer och externa reduktionsmedel, men ger ändå de önskade p-hydroxydiphenylaminerna i god avkastning.
Att undersöka vad som händer mellan start och mål
För att förstå och optimera denna reaktion byggde forskarna en automatiserad elektro-kemisk masspektrometri (AIEC-MS) plattform. Reaktionsblandningar som innehåller endast små mängder material matas genom en miniatu-rad flödescell, där de utsätts för applicerad spänning och sedan sprutas direkt in i en masspektrometer. Detta gör det möjligt för teamet att snabbt testa många kombinationer av nitroföreningar och fenoler, samtidigt som kortlivade intermediärer som bara uppträder under elektrolys fångas in. Med detta verktyg visade de att en mängd olika nitroarenar — med halogener, elektronattraherande grupper, deuterium-markeringar och till och med flera nitrogrupper — liksom många substituerade fenoler, alla deltar effektivt i den nya bindningsbildningsprocessen.

Att se en reaktiv ”spöklik” mellanprodukt göra jobbet
Metodens verkliga styrka ligger i dess förmåga att göra synliga de vanligtvis osedda stegen i reaktionen. Med högupplöst och tandem-masspektrometri upptäckte författarna en följd av flyktiga arter som bildas när nitroföreningen färdas nedför den elektro-kemiska ”stegen” vid reduktion. Bland dem finns en mycket reaktiv aryl nitren-liknande mellanprodukt, en kvävehaltig fragment som kan infogas direkt i kolstrukturen hos den aktiverade fenolringen. Ytterligare experiment — inklusive isotopmarkering, kinetiska mätningar, spänningskontroll och fällningsreaktioner med andra partner — stöder en stegvis bild: nitroföreningar reduceras via nitroso och närliggande arter till en nitren; fenoler oxideras till mer reaktiva former; nitrenet införs i para C–H-bindningen hos den fenol-deriverade partnern; och en slutlig uppsättning elektronöverföringar återställer aromatisk stabilitet för att ge produkten.
Från grundläggande insikt till framtida tillämpningar
Genom att kombinera en mild, elektricitetdriven reaktion med en kraftfull in situ-analytisk plattform uppnår detta arbete både praktisk syntes och en klar bild av den underliggande mekanismen. I vardagliga termer har teamet utformat en renare ”ett-uttag”-metod för att sammanfoga användbara kväveinnehållande molekyler från enkla, lättillgängliga ringar, samtidigt som den molekylära koreografin filmas i realtid. Deras strategi med parvis elektrolys visar att direkt användning av nitroföreningar, styrd av realtidsmasspektrometri, kan utöka vad som är möjligt inom organisk syntes. Framöver kan liknande angreppssätt hjälpa kemister att utforma mer effektiva, selektiva och hållbara vägar till en mängd komplexa molekyler viktiga för medicin, jordbruk och materialvetenskap.
Citering: Peng, T., Chen, Z., Cui, X. et al. Paired electrolysis enables para-C–H amination of phenols with nitroarenes and mechanistic visualization via multifunctional electrochemical mass spectrometry. Nat Commun 17, 4143 (2026). https://doi.org/10.1038/s41467-026-70691-x
Nyckelord: elektroorganisk syntes, C–N-bindningsbildning, parvis elektrolys, masspektrometri, nitroarenaminering