Clear Sky Science · pl
Skorelowana elektroliza umożliwia para-C–H aminację fenoli nitroarenami i wizualizację mechanizmu za pomocą wielofunkcyjnej elektrochemicznej spektrometrii mas
Przekształcanie prostych pierścieni w użyteczne molekuły
Chemicy polegają na wiązaniach węgiel–azot, budując wiele leków, barwników i materiałów, z których korzystamy na co dzień. Tradycyjnie łączenie tych atomów wymaga metali szlachetnych, wielu etapów reakcji i agresywnych reagentów. W tym badaniu przedstawiono łagodniejszy, zasilany prądem sposób łączenia dwóch bardzo powszechnych bloków konstrukcyjnych — fenoli i związków nitrowych — w wartościowe produkty stosowane w barwnikach, pestycydach i dodatkach do paliw. Pokazuje ono także swego rodzaju „transmisję na żywo” reakcji na poziomie molekularnym, zarejestrowaną za pomocą specjalistycznego układu spektrometrii mas.
Dlaczego ten nowy sposób budowania wiązań ma znaczenie
Docelowe związki w tej pracy, nazywane p-hydroksydifenyloaminami, stanowią sedno wielu funkcjonalnych produktów — od barwników po antyutleniacze w paliwach. Konwencjonalne drogi syntezy zazwyczaj zaczynają się od już zredukowanych form związków nitrowych i często wymagają grup ochronnych, dodatkowych reagentów oraz katalizatorów metali. Każdy dodatkowy etap zwiększa koszty, ilość odpadów i zużycie energii. Autorzy postanowili znaleźć bezpośredni sposób połączenia prostego związku nitrowego z pierścieniem fenolowym w jednym kroku, najlepiej bez drogich metali i zewnętrznych utleniaczy czy reduktorów.
Wykorzystanie elektryczności jako niewidzialnego reagenta
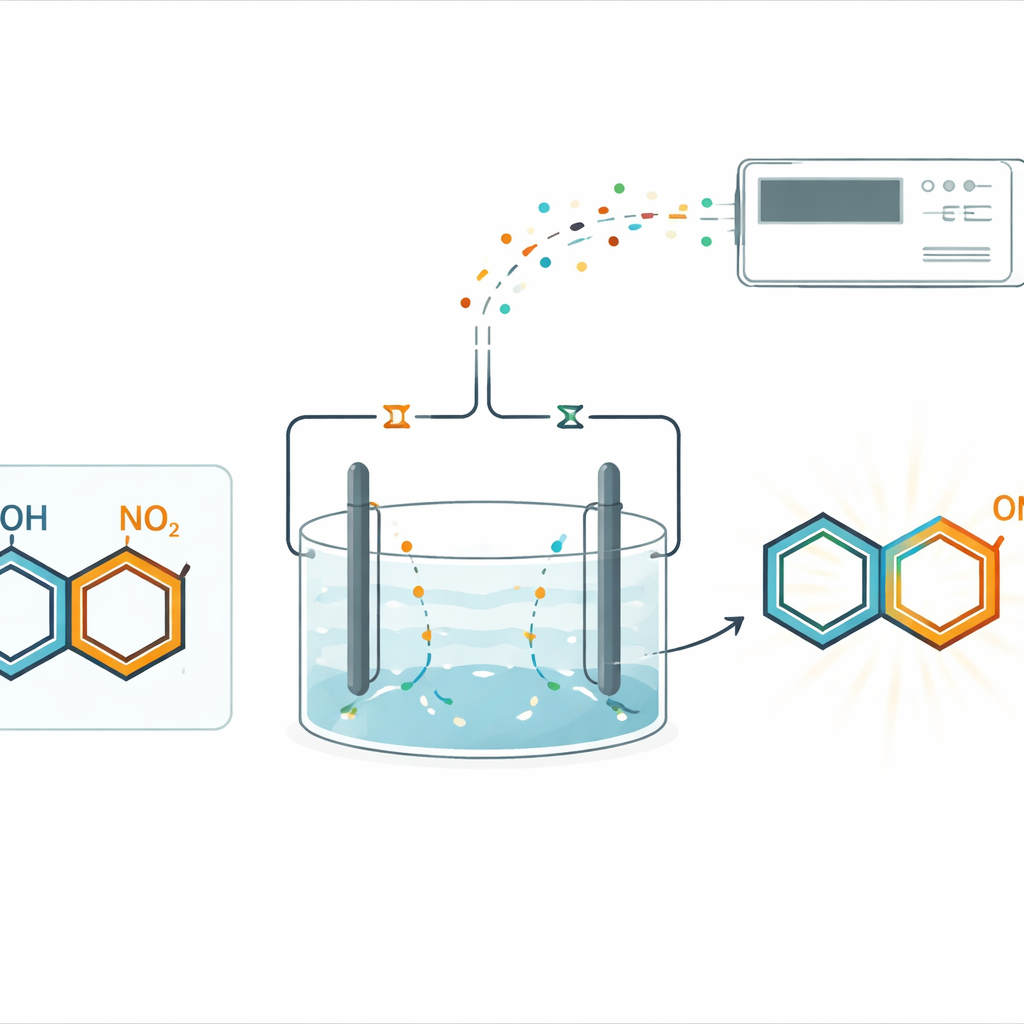
Zamiast polegać na butelkowanych chemikaliach do dodawania lub usuwania elektronów, zespół zastosował skorelowaną elektrolizę w pojedynczej, nierozdzielonej celi. W tym układzie prąd elektryczny napędza jednocześnie dwie komplementarne przemiany: redukcję przy jednej elektrodzie i utlenianie przy drugiej. Pierścienie zawierające grupę nitrową są łagodnie redukowane przy katodzie, podczas gdy fenole są aktywowane przy anodzie. Przy starannie dobranych warunkach dwaj aktywowani partnerzy spotykają się i tworzą nowe wiązanie węgiel–azot w określonym położeniu na pierścieniu fenolowym, zwanym pozycją para. Podejście to unika katalizatorów metali i zewnętrznych reduktorów, a mimo to dostarcza pożądane p-hydroksydifenyloaminy w dobrych wydajnościach.
Badanie tego, co dzieje się między początkiem a końcem
Aby zrozumieć i zoptymalizować tę reakcję, badacze zbudowali zautomatyzowaną platformę elektrochemicznej spektrometrii mas (AIEC-MS). Mieszaniny reakcyjne zawierające jedynie śladowe ilości substancji są przepuszczane przez miniaturową komórkę przepływową, gdzie poddawane są przyłożonemu napięciu, a następnie natryskiwane bezpośrednio do spektrometru mas. Pozwala to zespołowi szybko testować wiele kombinacji nitroarenów i fenoli, jednocześnie wychwytując krótkożyjące pośrednie produkty pojawiające się tylko podczas elektrolizy. Dzięki temu narzędziu wykazali, że szeroka gama nitroarenów — zawierających halogeny, grupy przyciągające elektrony, znaczniki deuterowe, a nawet wiele grup nitrowych — oraz wiele podstawionych fenoli skutecznie uczestniczy w nowym procesie tworzenia wiązania.

Obserwowanie reaktywnego „duszka” w akcji
Prawdziwa siła metody tkwi w zdolności uczynienia widocznymi zwykle niewidocznych etapów reakcji. Dzięki wysokorozdzielczej i tandemowej spektrometrii mas autorzy wykryli sekwencję ulotnych gatunków powstających, gdy związek nitrowy przechodzi przez elektrochemiczne „schody” redukcji. Wśród nich znajduje się wysoce reaktywny, przypominający arylowy nitren, fragment zawierający azot, który może wprost wstawiać się w szkielet węglowy aktywowanego pierścienia fenolowego. Dodatkowe eksperymenty — w tym znakowanie izotopowe, pomiary kinetyczne, kontrola napięcia oraz reakcje łapczywe z innymi partnerami — wspierają obraz krokowego mechanizmu: związki nitrowe są redukowane poprzez nitroso i pokrewne gatunki do nitrenu; fenole są utleniane do bardziej reaktywnych form; nitren wstawia się w wiązanie para C–H partnera pochodzącego od fenolu; a końcowy zestaw transferów elektronów przywraca aromatyczną stabilność, prowadząc do produktu.
Od podstawowego wglądu do przyszłych zastosowań
Łącząc łagodną, napędzaną elektrycznością reakcję z potężną platformą analityczną in situ, praca ta osiąga jednocześnie praktyczną syntezę i jasny obraz leżącego u podstaw mechanizmu. Mówiąc obrazowo, zespół opracował czystszą „metodę na jedno gniazdko” do składania użytecznych związków zawierających azot z prostych, łatwo dostępnych pierścieni, jednocześnie filmując molekularną choreografię w miarę jej rozwijania. Ich strategia skorelowanej elektrolizy pokazuje, że bezpośrednie wykorzystanie związków nitrowych, kierowane spektrometrią mas w czasie rzeczywistym, może rozszerzyć możliwości syntezy organicznej. Patrząc w przyszłość, podobne podejścia mogą pomóc chemikom projektować bardziej wydajne, selektywne i zrównoważone drogi do szeregu złożonych molekuł ważnych dla medycyny, rolnictwa i nauki o materiałach.
Cytowanie: Peng, T., Chen, Z., Cui, X. et al. Paired electrolysis enables para-C–H amination of phenols with nitroarenes and mechanistic visualization via multifunctional electrochemical mass spectrometry. Nat Commun 17, 4143 (2026). https://doi.org/10.1038/s41467-026-70691-x
Słowa kluczowe: synteza elektroorganiczna, tworzenie wiązań C–N, skorelowana elektroliza, spektrometria mas, aminacja nitroarenów