Clear Sky Science · fr
L’électrolyse appariée permet l’amination para-C–H des phénols avec des nitroarènes et la visualisation mécanistique via une spectrométrie de masse électrochimique multifonctionnelle
Transformer des cycles simples en molécules utiles
Les chimistes s’appuient sur les liaisons carbone–azote pour construire nombre des médicaments, colorants et matériaux que nous utilisons quotidiennement. Traditionnellement, établir ces liaisons nécessite des métaux précieux, plusieurs étapes réactionnelles et des réactifs agressifs. Cette étude présente une méthode plus douce, alimentée par l’électricité, pour relier deux blocs de construction très courants — les phénols et les composés nitro — afin d’obtenir des produits de valeur employés dans les colorants, les pesticides et les additifs pour carburants. Elle met également en scène une sorte de « flux vidéo » moléculaire de la réaction, capté par une configuration spécialisée de spectrométrie de masse.
Pourquoi cette nouvelle astuce de construction de liaison est importante
Les molécules ciblées dans ce travail, appelées p-hydroxy-diphénylamines, sont au cœur de nombreux produits fonctionnels, des colorants aux antioxydants pour carburants. Les voies conventionnelles partent généralement d’une forme déjà réduite des composés nitro et nécessitent souvent des groupes protecteurs, des réactifs supplémentaires et des catalyseurs métalliques. Chaque étape ajoutée augmente le coût, les déchets et la consommation d’énergie. Les auteurs ont cherché à trouver une manière directe d’unir un composé nitro simple à un noyau phénolique en une seule opération, idéalement sans métaux coûteux ni agents oxydants ou réducteurs externes.
Utiliser l’électricité comme réactif invisible
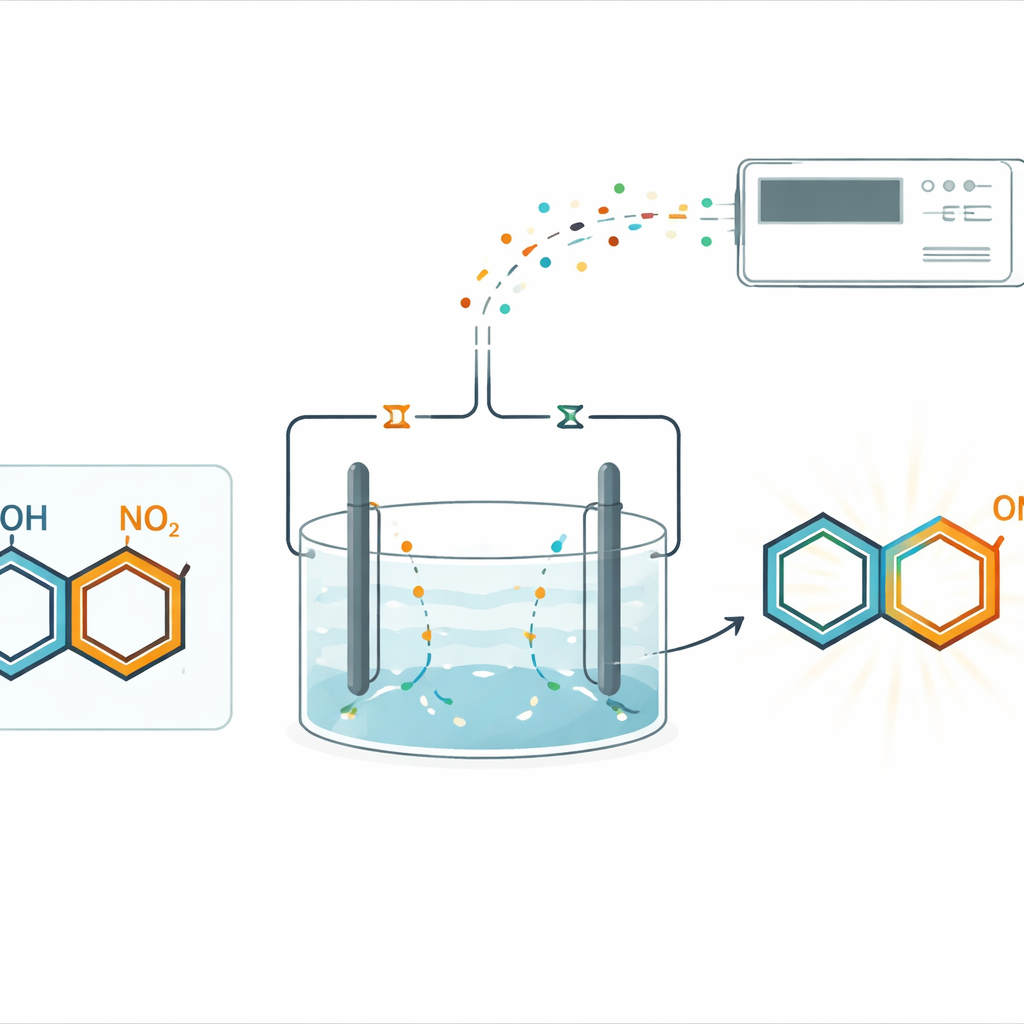
Plutôt que de s’appuyer sur des produits chimiques conditionnés pour ajouter ou retirer des électrons, l’équipe a utilisé l’électrolyse appariée dans une cellule unique et non divisée. Dans ce montage, le courant électrique provoque simultanément deux transformations complémentaires : réduction à une électrode et oxydation à l’autre. Les cycles porteurs de nitro sont doucement réduits du côté cathode, tandis que les phénols sont activés du côté anode. Dans des conditions soigneusement choisies, les deux partenaires activés se rencontrent et forment une nouvelle liaison carbone–azote en une position spécifique du noyau phénolique, dite para. Cette approche évite les catalyseurs métalliques et les agents réducteurs externes, tout en donnant les p-hydroxy-diphénylamines souhaitées avec de bons rendements.
Examiner ce qui se passe entre le début et la fin
Pour comprendre et optimiser cette réaction, les chercheurs ont conçu une plateforme automatisée de spectrométrie de masse électrochimique (AIEC-MS). De très petites quantités de mélange réactionnel sont alimentées à travers une cellule d’écoulement miniature, où elles subissent une tension appliquée puis sont pulvérisées directement dans un spectromètre de masse. Cela permet à l’équipe de tester rapidement de nombreuses combinaisons de nitrocomposés et de phénols, tout en capturant des intermédiaires éphémères qui n’apparaissent que pendant l’électrolyse. Grâce à cet outil, ils ont montré qu’une grande variété de nitroarènes — portant des halogènes, des groupes attracteurs d’électrons, des marquages au deutérium, et même plusieurs groupes nitro — ainsi que de nombreux phénols substitués, participent efficacement au nouveau processus de formation de liaison.

Observer un « fantôme » réactif à l’œuvre
La véritable force de la méthode tient à sa capacité à rendre visibles des étapes habituellement invisibles de la réaction. À l’aide d’une spectrométrie de masse haute résolution et en tandem, les auteurs ont détecté une séquence d’espèces fugitives formées lorsque le composé nitro descend l’« échelle » électrochimique de réduction. Parmi elles se trouve un intermédiaire fortement réactif de type nitrène aryle, un fragment azoté qui peut s’insérer directement dans le squelette carboné du noyau phénolique activé. Des expériences complémentaires — incluant des marquages isotopiques, des mesures cinétiques, le contrôle de la tension et des réactions de piégeage avec d’autres partenaires — soutiennent un scénario par étapes : les composés nitro sont réduits via des espèces nitroso et apparentées jusqu’à un nitrène ; les phénols sont oxydés en formes plus réactives ; le nitrène s’insère dans la liaison C–H para du partenaire dérivé du phénol ; et une dernière série de transferts électroniques restaure la stabilité aromatique pour donner le produit.
Des connaissances fondamentales aux applications futures
En combinant une réaction douce, conduite par l’électricité, avec une puissante plateforme analytique in situ, ce travail réalise à la fois une synthèse pratique et une vue claire du mécanisme sous-jacent. En termes simples, l’équipe a mis au point une méthode plus propre, « tout-en-un », pour assembler des molécules azotées utiles à partir de cycles simples et facilement disponibles, tout en filmant simultanément la chorégraphie moléculaire au fur et à mesure. Leur stratégie d’électrolyse appariée démontre que l’emploi direct de composés nitro, guidé par une spectrométrie de masse en temps réel, peut élargir les possibilités en synthèse organique. À l’avenir, des approches similaires pourraient aider les chimistes à concevoir des voies plus efficaces, sélectives et durables vers de nombreuses molécules complexes importantes pour la médecine, l’agriculture et la science des matériaux.
Citation: Peng, T., Chen, Z., Cui, X. et al. Paired electrolysis enables para-C–H amination of phenols with nitroarenes and mechanistic visualization via multifunctional electrochemical mass spectrometry. Nat Commun 17, 4143 (2026). https://doi.org/10.1038/s41467-026-70691-x
Mots-clés: synthèse électro-organique, formation de liaison C–N, électrolyse appariée, spectrométrie de masse, amination de nitroarènes