Clear Sky Science · de
Gepaartes Elektrolyse ermöglicht para-C–H-Aminierung von Phenolen mit Nitroarenen und mechanistische Visualisierung durch multifunktionelle elektrochemische Massenspektrometrie
Einfache Ringe in nützliche Moleküle verwandeln
Chemiker bauen auf Kohlenstoff–Stickstoff-Bindungen, um viele der Arzneimittel, Farbstoffe und Materialien herzustellen, die wir täglich verwenden. Traditionell erfordert das Verbinden dieser Atome teure Metalle, mehrere Reaktionsschritte und aggressive Chemikalien. Diese Studie stellt eine schonendere, elektrisch betriebene Methode vor, um zwei sehr verbreitete Bausteine – Phenole und Nitroverbindungen – in wertvolle Produkte zu überführen, die in Farbstoffen, Pestiziden und Kraftstoffzusätzen Anwendung finden. Außerdem zeigt sie eine Art „Live-Video“ der Reaktion auf molekularer Ebene, aufgezeichnet mit einer spezialisierten Massenspektrometrie-Anordnung.
Warum dieser neue Bindungsbildungs-Trick wichtig ist
Die Zielmoleküle dieser Arbeit, sogenannte p-Hydroxy-Diphenylamine, bilden das Herzstück vieler funktionaler Produkte, von Farbstoffen bis zu Antioxidantien in Kraftstoffen. Konventionelle Wege zu ihnen starten meist von bereits reduzierten Nitroverbindungen und erfordern häufig Schutzgruppen, zusätzliche Reagenzien und Metallkatalysatoren. Jeder zusätzliche Schritt erhöht Kosten, Abfall und Energieaufwand. Die Autoren suchten daher nach einem direkten Weg, eine einfache Nitroverbindung mit einem Phenolring in einem einzigen Schritt zu verbinden, idealerweise ohne teure Metalle oder externe Oxidations- und Reduktionsmittel.
Elektrizität als unsichtbares Reagenz nutzen
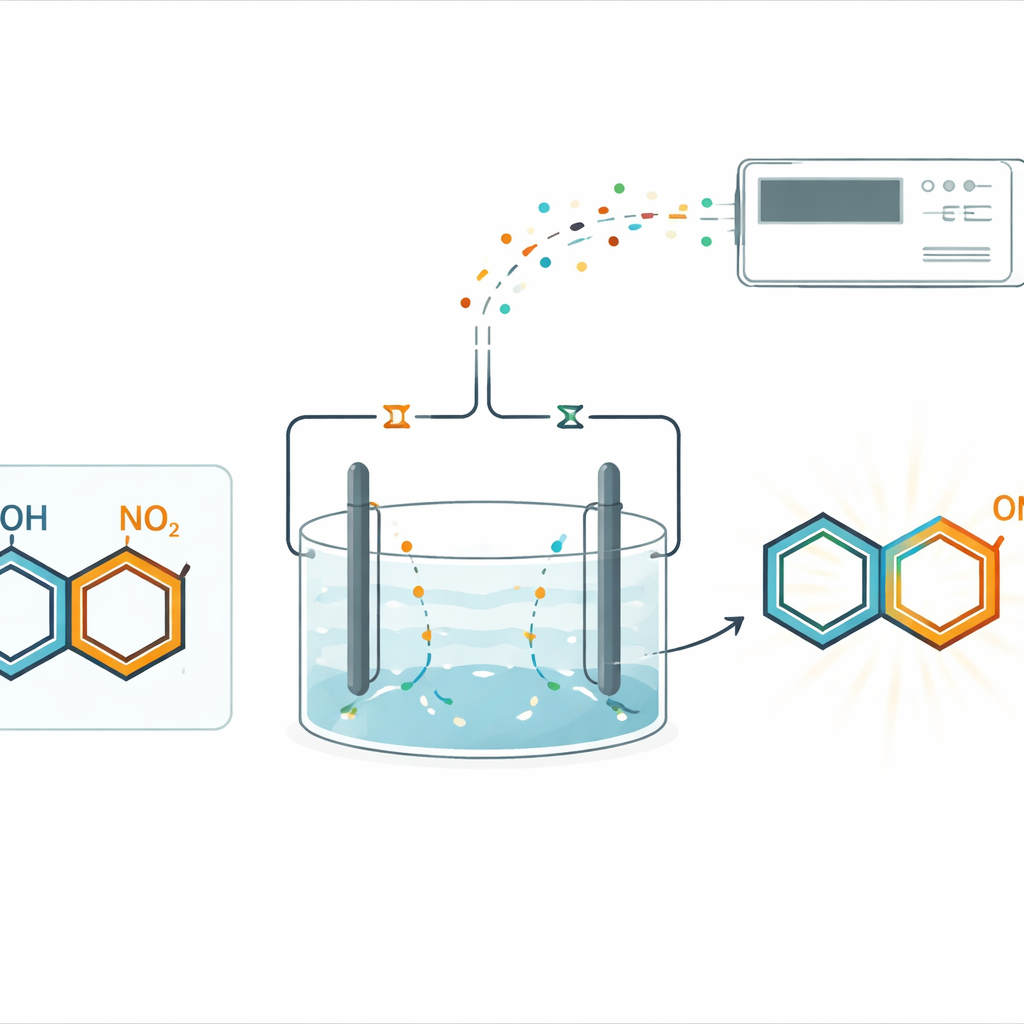
Anstatt sich auf abgefüllte Chemikalien zum Hinzufügen oder Entfernen von Elektronen zu verlassen, nutzte das Team gepaarte Elektrolyse in einer einzigen, undividierten Zelle. In diesem Aufbau treibt elektrischer Strom zwei komplementäre Umwandlungen gleichzeitig an: Reduktion an einer Elektrode und Oxidation an der anderen. Nitrohaltige Ringe werden schonend an der Kathode reduziert, während Phenole an der Anode aktiviert werden. Unter sorgfältig gewählten Bedingungen treffen die beiden aktivierten Partner aufeinander und bilden eine neue Kohlenstoff–Stickstoff-Bindung an einer spezifischen Position des Phenolrings, dem para-Standort. Dieser Ansatz vermeidet Metallkatalysatoren und externe Reduktionsmittel und liefert dennoch die gewünschten p-Hydroxy-Diphenylamine in guten Ausbeuten.
Untersuchen, was zwischen Anfang und Ende passiert
Um die Reaktion zu verstehen und zu optimieren, bauten die Forscher eine automatisierte elektrochemische Massenspektrometrie-Plattform (AIEC-MS). Reaktionsmischungen mit nur winzigen Materialmengen werden durch eine Miniatur-Flowzelle geleitet, wo sie einer angelegten Spannung ausgesetzt und dann direkt in eine Massenspektrometrie eingesprüht werden. So kann das Team schnell viele Kombinationen aus Nitroverbindungen und Phenolen testen und zugleich kurzlebige Zwischenstufen erfassen, die nur während der Elektrolyse auftreten. Mit diesem Werkzeug zeigten sie, dass eine große Vielfalt von Nitroarenen – mit Halogenen, elektronenziehenden Gruppen, Deuterium-Markierungen und sogar mehreren Nitrogruppen – sowie viele substituierte Phenole wirksam an dem neuen Bindungsbildungsprozess teilnehmen.

Wenn ein reaktiver „Geist“ die Arbeit macht
Die eigentliche Stärke der Methode liegt in der Fähigkeit, die sonst unsichtbaren Reaktionsschritte sichtbar zu machen. Mit hochauflösender und tandem Massenspektrometrie detektierten die Autoren eine Abfolge flüchtiger Spezies, die entstehen, während die Nitroverbindung die elektrochemische „Treppe“ der Reduktion hinabsteigt. Darunter befindet sich ein hochreaktives, nitrenähnliches aryles Zwischenprodukt, ein Stickstoff-haltiger Fragmenttyp, der direkt in das Kohlenstoffgerüst des aktivierten Phenolrings einfügen kann. Zusätzliche Experimente – einschließlich Isotopenmarkierung, kinetischen Messungen, Spannungssteuerung und Einkapselungsreaktionen mit anderen Partnern – stützen ein schrittweises Bild: Nitroverbindungen werden über Nitroso- und verwandte Spezies zu einem Nitren reduziert; Phenole werden zu reaktiveren Formen oxidiert; das Nitren fügt sich in die para C–H-Bindung des phenolabgeleiteten Partners ein; und eine abschließende Serie von Elektronentransfers stellt die aromatische Stabilität wieder her und liefert das Produkt.
Von grundlegenden Erkenntnissen zu künftigen Anwendungen
Durch die Kombination einer milden, elektrisch angetriebenen Reaktion mit einer leistungsfähigen in-situ-Analytik-Plattform erreicht diese Arbeit sowohl praktische Synthese als auch einen klaren Einblick in den zugrunde liegenden Mechanismus. Einfach gesagt hat das Team eine sauberere „Ein-Stecker“-Methode entwickelt, um nützliche stickstoffhaltige Moleküle aus einfachen, leicht verfügbaren Ringen zusammenzusetzen – und gleichzeitig die molekulare Choreografie beim Ablauf zu filmen. Ihre Strategie der gepaarten Elektrolyse zeigt, dass die direkte Nutzung von Nitroverbindungen, geleitet durch Echtzeit-Massenspektrometrie, das Mögliche in der organischen Synthese erweitern kann. Blickt man nach vorn, könnten ähnliche Ansätze Chemikern helfen, effizientere, selektivere und nachhaltigere Wege zu einer Vielzahl komplexer Moleküle zu entwerfen, die für Medizin, Landwirtschaft und Materialwissenschaften wichtig sind.
Zitation: Peng, T., Chen, Z., Cui, X. et al. Paired electrolysis enables para-C–H amination of phenols with nitroarenes and mechanistic visualization via multifunctional electrochemical mass spectrometry. Nat Commun 17, 4143 (2026). https://doi.org/10.1038/s41467-026-70691-x
Schlüsselwörter: elektroorganische Synthese, C–N-Bindungsbildung, gepaarte Elektrolyse, Massenspektrometrie, Nitroarender Aminierung