Clear Sky Science · it
L’elettrolisi accoppiata consente l’amminazione para-C–H dei fenoli con nitroarenici e la visualizzazione meccanicistica tramite spettrometria di massa elettrochimica multifunzionale
Trasformare anelli semplici in molecole utili
I chimici fanno affidamento sui legami carbonio–azoto per costruire molti dei farmaci, dei coloranti e dei materiali che usiamo ogni giorno. Tradizionalmente, unire questi atomi richiede metalli preziosi, più fasi di reazione e sostanze chimiche aggressive. Questo studio introduce un modo più delicato, alimentato dall’elettricità, per collegare due mattoncini molto comuni — fenoli e composti nitro — in prodotti di valore impiegati in coloranti, pesticidi e additivi per carburanti. Mostra inoltre una sorta di “video in diretta” della reazione a livello molecolare, catturato da un dispositivo di spettrometria di massa specializzato.
Perché questo nuovo trucco per formare legami è importante
Le molecole obiettivo in questo lavoro, chiamate p-idrossi difenilammine, stanno al centro di molti prodotti funzionali, dai coloranti agli antiossidanti per i carburanti. Le vie convenzionali per ottenerle di solito partono da forme già ridotte dei composti nitro e spesso richiedono gruppi protettivi, reagenti addizionali e catalizzatori metallici. Ogni passaggio aggiuntivo aumenta i costi, i rifiuti e il consumo energetico. Gli autori si sono posti l’obiettivo di trovare un modo diretto per unire in un solo passaggio un semplice composto nitro con un anello fenolico, idealmente senza metalli costosi né agenti ossidanti o riducenti esterni.
Usare l’elettricità come reagente invisibile
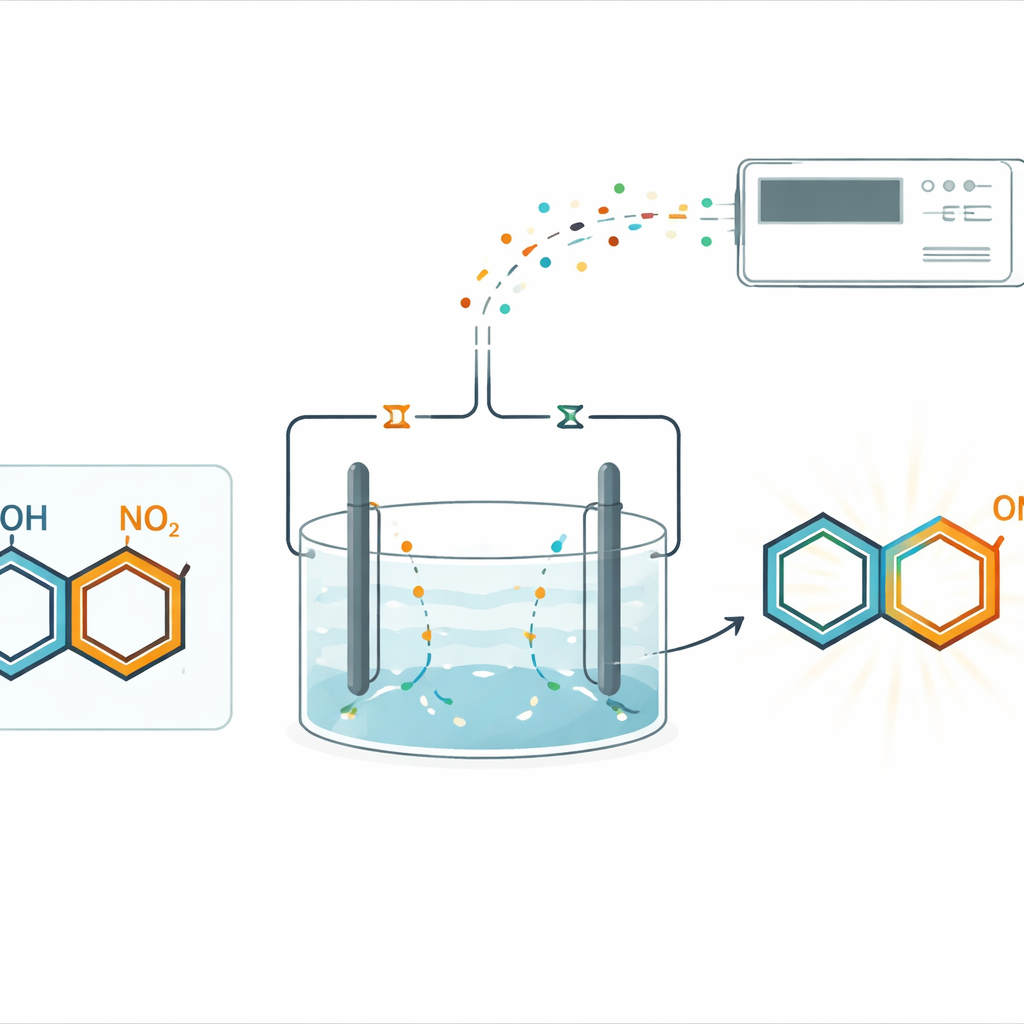
Invece di affidarsi a reagenti in bombole per aggiungere o rimuovere elettroni, il gruppo ha utilizzato l’elettrolisi accoppiata in una singola cella indivisa. In questo allestimento, la corrente elettrica guida due cambiamenti complementari contemporaneamente: riduzione a un elettrodo e ossidazione all’altro. Gli anelli contenenti nitro vengono delicatamente ridotti al catodo, mentre i fenoli vengono attivati all’anodo. In condizioni accuratamente scelte, i due partner attivati si incontrano e formano un nuovo legame carbonio–azoto in una posizione specifica sull’anello fenolico, nota come sito para. Questo approccio evita catalizzatori metallici e agenti riducenti esterni, pur fornendo le p-idrossi difenilammine desiderate con rese soddisfacenti.
Indagare cosa succede tra inizio e fine
Per comprendere e ottimizzare la reazione, i ricercatori hanno costruito una piattaforma automatizzata di spettrometria di massa elettrochimica (AIEC-MS). Miscele reattive contenenti solo piccole quantità di materiale vengono fatte scorrere attraverso una microcella a flusso, dove è applicata una tensione e poi nebulizzate direttamente in uno spettrometro di massa. Ciò permette al gruppo di testare rapidamente molte combinazioni di composti nitro e fenoli, catturando allo stesso tempo intermedi di vita brevissima che appaiono solo durante l’elettrolisi. Con questo strumento hanno mostrato che una vasta gamma di nitroarenici — contenenti alogeni, gruppi elettron-attrattori, marcature con deuterio e persino più gruppi nitro — così come molti fenoli sostituiti, partecipano efficacemente al nuovo processo di formazione del legame.

Vedere un “fantasma” reattivo fare il lavoro
Il vero punto di forza del metodo risiede nella sua capacità di rendere visibili i passaggi della reazione normalmente non osservabili. Utilizzando spettrometria di massa ad alta risoluzione e tandem, gli autori hanno rilevato una sequenza di specie fugaci formatesi mentre il composto nitro scende lungo la “scala” elettrochimica della riduzione. Tra queste figura un intermedio altamente reattivo simile a un aril-nitrene, un frammento contenente azoto che può inserirsi direttamente nello scheletro carbonioso dell’anello fenolico attivato. Esperimenti supplementari — inclusi marcaggi isotopici, misure cinetiche, controllo della tensione e reazioni di intrappolamento con altri partner — supportano un quadro passo-passo: i composti nitro vengono ridotti attraverso specie nitroso e correlate fino a un nitrene; i fenoli vengono ossidati in forme più reattive; il nitrene si inserisce nel legame C–H para del partner derivato dal fenolo; e un ultimo insieme di trasferimenti elettronici ripristina la stabilità aromatica per dare il prodotto.
Dall’intuizione fondamentale alle applicazioni future
Combinando una reazione blanda guidata dall’elettricità con una potente piattaforma analitica in situ, questo lavoro ottiene sia una sintesi pratica sia una visione chiara del meccanismo sottostante. In termini pratici, il gruppo ha ideato un metodo più pulito e “a spina unica” per assemblare molecole azotate utili a partire da anelli semplici e facilmente reperibili, filmando al contempo la coreografia molecolare mentre si svolge. La loro strategia di elettrolisi accoppiata dimostra che l’uso diretto di composti nitro, guidato dalla spettrometria di massa in tempo reale, può ampliare le possibilità nella sintesi organica. Guardando avanti, approcci analoghi potrebbero aiutare i chimici a progettare vie più efficienti, selettive e sostenibili per una serie di molecole complesse importanti per la medicina, l’agricoltura e la scienza dei materiali.
Citazione: Peng, T., Chen, Z., Cui, X. et al. Paired electrolysis enables para-C–H amination of phenols with nitroarenes and mechanistic visualization via multifunctional electrochemical mass spectrometry. Nat Commun 17, 4143 (2026). https://doi.org/10.1038/s41467-026-70691-x
Parole chiave: sintesi elettroorganica, formazione di legami C–N, elettrolisi accoppiata, spettrometria di massa, amminazione di nitroarenici