Clear Sky Science · es
La electrólisis pareada permite la aminação para-C–H de fenoles con nitroarenos y visualización mecanística mediante espectrometría de masas electroquímica multifuncional
Convertir anillos simples en moléculas útiles
Los químicos dependen de los enlaces carbono–nitrógeno para construir muchos de los medicamentos, colorantes y materiales que usamos a diario. Tradicionalmente, unir estos átomos requiere metales preciosos, múltiples pasos de reacción y reactivos agresivos. Este estudio presenta una forma más suave, impulsada por electricidad, de conectar dos bloques de construcción muy comunes —fenoles y compuestos nitro— en productos valiosos utilizados en colorantes, pesticidas y aditivos para combustibles. También muestra una especie de “transmisión en vivo” de la reacción a nivel molecular, captada por una configuración especializada de espectrometría de masas.
Por qué importa este nuevo truco para formar enlaces
Las moléculas objetivo de este trabajo, llamadas p-hidroxi difenilaminas, están en el centro de muchos productos funcionales, desde colorantes hasta antioxidantes en combustibles. Las rutas convencionales hacia ellas suelen partir de una forma ya reducida de los compuestos nitro y a menudo requieren grupos protectores, reactivos adicionales y catalizadores metálicos. Cada paso añadido aumenta el coste, los residuos y el consumo de energía. Los autores se propusieron encontrar una manera directa de unir un compuesto nitro simple con un anillo fenólico en una sola etapa, idealmente sin metales caros ni agentes oxidantes o reductores externos.
Usar la electricidad como reactivo invisible
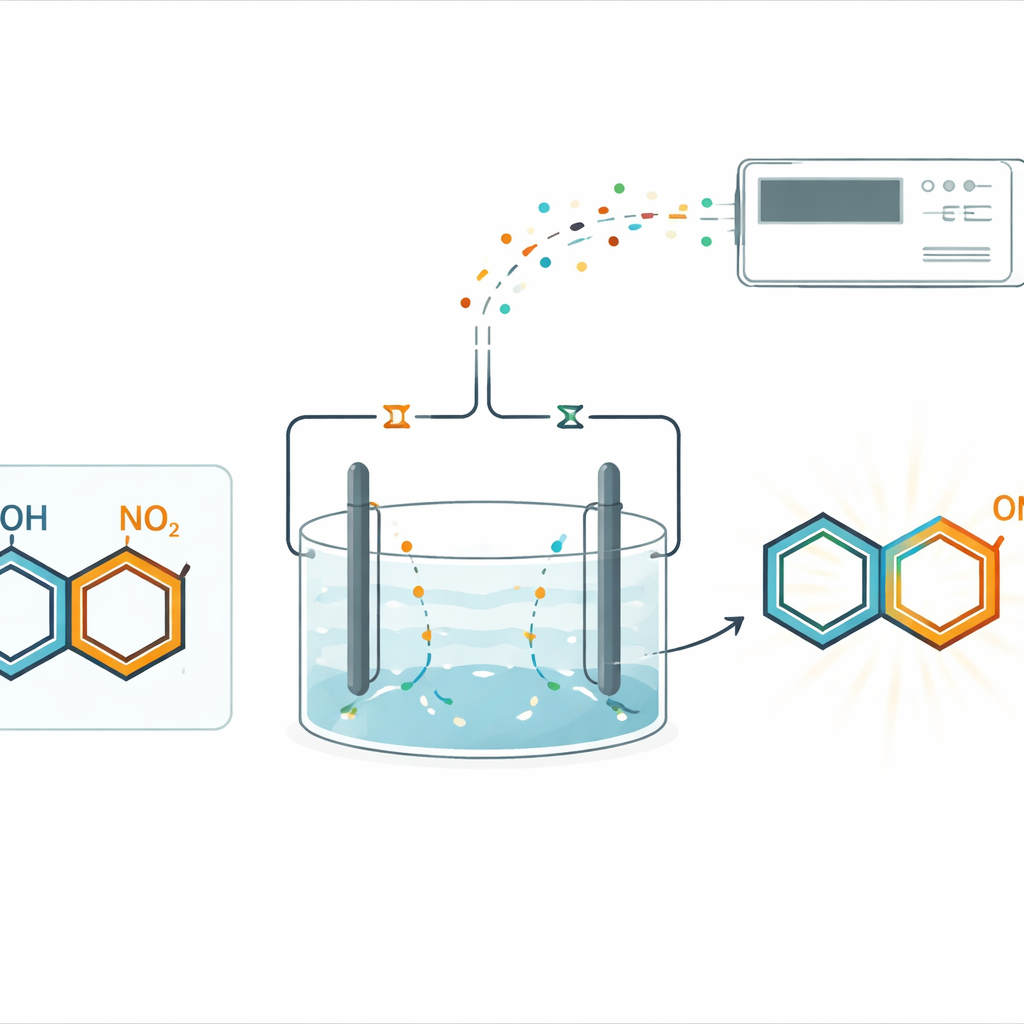
En lugar de confiar en productos químicos en botella para añadir o quitar electrones, el equipo utilizó electrólisis pareada en una celda única no dividida. En este montaje, la corriente eléctrica impulsa dos cambios complementarios a la vez: reducción en un electrodo y oxidación en el otro. Los anillos que contienen nitro se reducen suavemente en el cátodo, mientras que los fenoles se activan en el ánodo. Bajo condiciones cuidadosamente escogidas, las dos especies activadas se encuentran y forman un nuevo enlace carbono–nitrógeno en una posición específica del anillo fenólico, conocida como sitio para (para). Este enfoque evita catalizadores metálicos y agentes reductores externos, y aun así obtiene las p-hidroxi difenilaminas deseadas con buenos rendimientos.
Sondeando lo que ocurre entre el inicio y el final
Para entender y optimizar esta reacción, los investigadores construyeron una plataforma automatizada de espectrometría de masas electroquímica (AIEC-MS). Mezclas de reacción que contienen solo trazas de material se hacen pasar por una celda de flujo en miniatura, donde se aplica un voltaje y luego se pulverizan directamente hacia un espectrómetro de masas. Esto permite al equipo probar rápidamente muchas combinaciones de compuestos nitro y fenoles, al tiempo que captura intermedios de corta vida que sólo aparecen durante la electrólisis. Con esta herramienta, mostraron que una amplia variedad de nitroarenos —con halógenos, grupos electrono-atrayentes, etiquetas de deuterio e incluso múltiples grupos nitro— así como muchos fenoles sustituidos, participan eficazmente en el nuevo proceso de formación de enlaces.

Observando a un “fantasma” reactivo hacer el trabajo
El verdadero poder del método radica en su capacidad para hacer visibles los pasos de la reacción que normalmente son invisibles. Usando espectrometría de masas de alta resolución y en tándem, los autores detectaron una secuencia de especies fugaces formadas a medida que el compuesto nitro desciende por la “escalera” electroquímica de reducción. Entre ellas figura un intermedio altamente reactivo similar a un aril nitreno, un fragmento con nitrógeno que puede insertarse directamente en el entramado carbonado del anillo fenólico activado. Experimentos adicionales —incluyendo marcado isotópico, medidas cinéticas, control de voltaje y reacciones de trampa con otros socios— respaldan una imagen por pasos: los compuestos nitro se reducen pasando por especies nitroso y afines hasta llegar a un nitreno; los fenoles se oxidan a formas más reactivas; el nitreno se inserta en el enlace C–H para de la porción fenólica en posición para; y una serie final de transferencias electrónicas restablece la aromaticidad para dar el producto.
De la comprensión fundamental a aplicaciones futuras
Combinando una reacción suave impulsada por electricidad con una potente plataforma analítica in situ, este trabajo logra tanto una síntesis práctica como una visión clara del mecanismo subyacente. Dicho en términos cotidianos, el equipo ha ideado un método más limpio de “enchufar y listo” para ensamblar moléculas nitrogenadas útiles a partir de anillos simples y fácilmente disponibles, mientras filman simultáneamente la coreografía molecular conforme se desarrolla. Su estrategia de electrólisis pareada demuestra que el uso directo de compuestos nitro, guiado por espectrometría de masas en tiempo real, puede ampliar lo posible en la síntesis orgánica. Mirando hacia adelante, enfoques similares pueden ayudar a los químicos a diseñar rutas más eficientes, selectivas y sostenibles hacia una gran variedad de moléculas complejas importantes para la medicina, la agricultura y la ciencia de materiales.
Cita: Peng, T., Chen, Z., Cui, X. et al. Paired electrolysis enables para-C–H amination of phenols with nitroarenes and mechanistic visualization via multifunctional electrochemical mass spectrometry. Nat Commun 17, 4143 (2026). https://doi.org/10.1038/s41467-026-70691-x
Palabras clave: síntesis electroorgánica, formación de enlaces C–N, electrólisis pareada, espectrometría de masas, aminación de nitroarenos