Clear Sky Science · sv
Massivt parallell kvantifiering av mutational påverkan på IAPP-amyloidbildning
Varför detta betyder något för vardagshälsan
Typ 2-diabetes drabbar hundratals miljoner människor, men vi förstår fortfarande inte fullt ut varför vissa individer är mer sårbara än andra. Ett litet hormon kallat IAPP, som produceras av samma celler som insulin, kan klumpa ihop sig till skadliga fibrer som förstör dessa celler. Denna studie testar systematiskt nästan tvåtusen små förändringar i IAPP för att visa vilka som förvärrar klumpning, vilka som gör den säkrare, och varför denna kunskap så småningom kan hjälpa till att utforma bättre behandlingar och verktyg för riskbedömning.
Hur ett litet hormon blir skadligt
IAPP (även kallat amylin) är ett kort proteinhormon som frisätts av pankreas beta-celler tillsammans med insulin för att hjälpa till att reglera blodsocker. Hos många personer med typ 2-diabetes staplas IAPP-molekyler upp i styva fibrer, så kallade amyloider, som skadar eller dödar de celler som utsöndrar dem. Intressant nog bildar nära besläktade versioner av IAPP hos djur som möss och björnar nästan aldrig dessa fibrer, och dessa djur utvecklar sällan typ 2-diabetes. Denna kontrast tyder på att små förändringar i IAPP:s byggstenar starkt kan påverka om den klumpar eller inte, vilket gör IAPP till ett idealiskt mål för ett systematiskt ”stress-test” av dess sekvens.
Ett massivt test av tusentals små förändringar
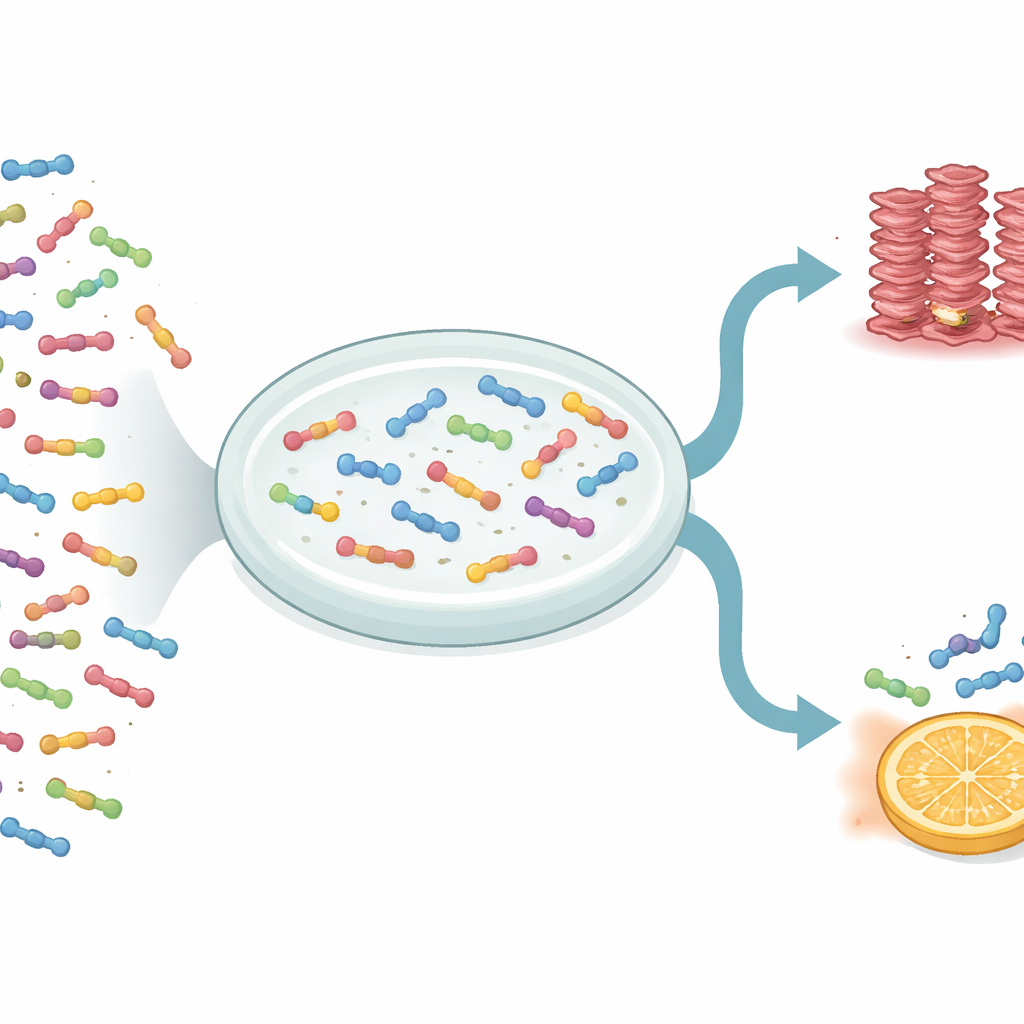
Forskarna använde en höggenomströmningsmetod kallad deep mutational scanning för att undersöka 1 916 olika varianter av IAPP. Dessa varianter inkluderade att byta ut en byggsten (aminosyra) mot en annan, infoga extra aminosyror, ta bort vissa, och korta av ändar. För att mäta hur varje variant uppträdde fäste de IAPP vid ett jästprotein som bildar amyloidliknande aggregat inuti jästceller. Om en viss IAPP-variant var bra på att starta klumpningen överlevde jästen som bar den bättre under specifika odlingsförhållanden. Genom att sekvensera jästpopulationens DNA före och efter selektionen kvantifierade teamet hur starkt varje förändring påskyndade eller fördröjde det initiala steget i fiberbildningen, kallat nukleation.
En sårbar kärna och en gömd säkerhetsfunktion
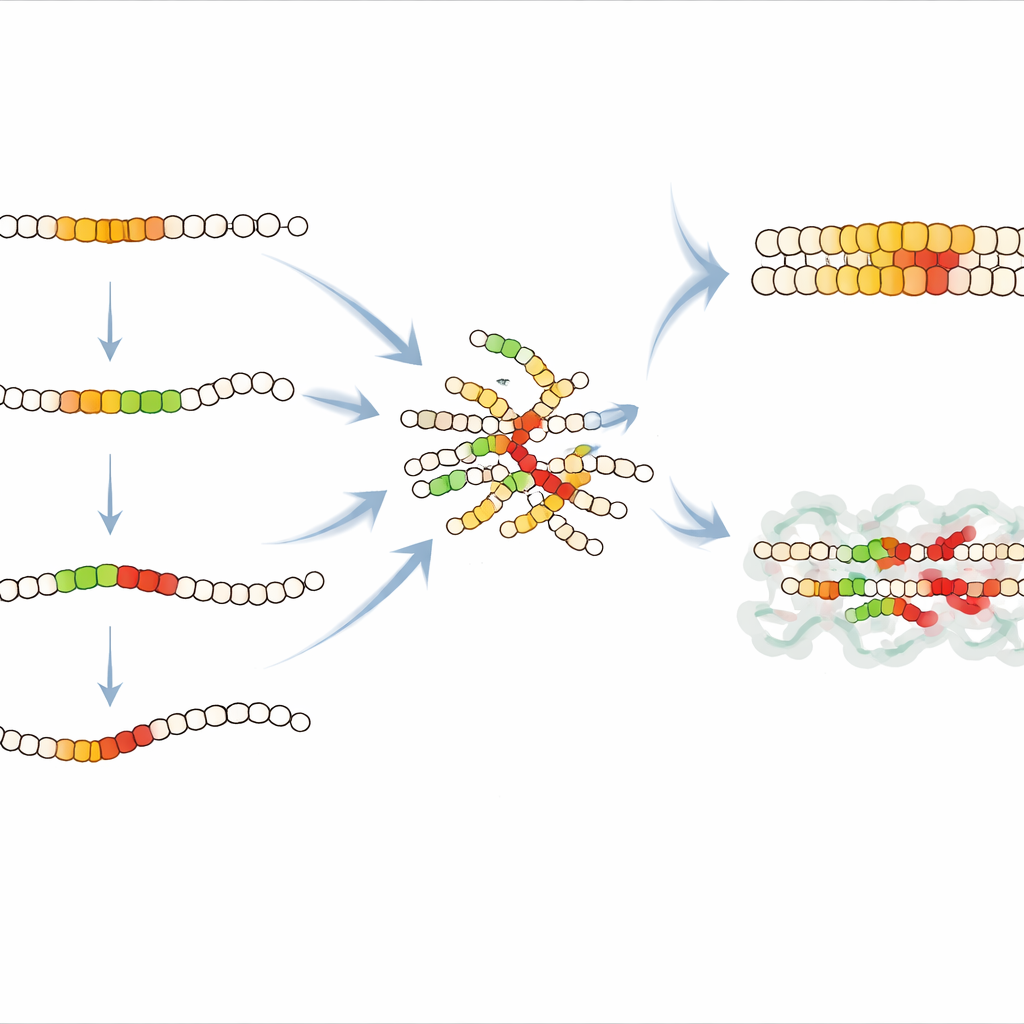
Kartan över mutationseffekter avslöjade ett avgörande avsnitt i mitten av IAPP, som spänner över positionerna 15 till 32, som är särskilt känsligt för förändringar. De flesta förändringar här försvagade klumpning, vilket tyder på att denna region bildar en strukturerad kärna i det tidiga fibret. Inom ett inre segment, positionerna 21 till 27, saktade nästan varje förändring (förutom vid en position) nukleationen dramatiskt, vilket bekräftar att denna korta motiv fungerar som hjärtat i amyloidkärnan. Studien upptäckte också en oväntad ”portvakt”-region tidigare i sekvensen, runt positionerna 11 till 21. Infogning av extra aminosyror här gjorde ofta klumpning snabbare, vilket antyder att detta segment i den naturliga sekvensen hjälper till att hålla enskilda IAPP-molekyler i en säkrare form som motstår aggregation. Att störa denna region verkar öppna upp för snabbare nukleation, vilket pekar på en möjlig målplats för läkemedel eller chaperonproteiner att binda och stabilisera IAPP.
Olika vägar till problem i närbesläktade hjärn- och pankreassjukdomar
Teamet jämförde sin IAPP-dataset med en tidigare, lika detaljerad karta för amyloid beta, peptiden som bildar plack vid Alzheimers sjukdom. Trots att det rör sig om olika organ och sjukdomar delar IAPP och amyloid beta liknande kärnstrukturer när de bildar fibrer och visar till och med måttlig sekvenslikhet. Forskarna fann att mutationer som stör fiberbildning tenderar att påverka båda peptiderna på liknande sätt, vilket tyder på en gemensam störningsmekanism i amyloidkärnan. Däremot betedde sig mutationer som accelererar klumpning mycket olika mellan de två proteinerna. Med andra ord följer fördröjning av dessa amyloider gemensamma regler, men att påskynda dem verkar vara starkt specifikt för varje peptid, vilket gör det svårt att använda en dataset för att förutsäga skadliga funktionsökande förändringar i en annan.
Kopplingar till mänsklig genetik och framtida terapier
Författarna granskade naturligt förekommande IAPP-varianter som finns i offentliga genombaser, inklusive UK Biobank. Många sällsynta mänskliga varianter saktade ner nukleationen och verkade mindre vanliga bland individer med typ 2-diabetes eller höga långvariga blodsockernivåer, vilket antyder att sådana förändringar kan ge ett visst skydd mot sjukdomen. Varianter som ökade nukleationen var för sällsynta för att dra definitiva slutsatser om risk, men förblir viktiga kandidater för framtida genetiska och kliniska studier. Mer allmänt ger arbetet en detaljerad atlas över hur olika mutationer påverkar IAPP-aggregation, vilket erbjuder en rationell vägledning för att utforma nya IAPP-baserade läkemedel som bibehåller hormonfunktionen men motstår bildandet av skadliga fibrer. Det understryker också ett större budskap: för att förstå och förutsäga skadlig proteinaggregering vid mänskliga sjukdomar kommer vi sannolikt att behöva liknande, kvantitativa kartor för varje amyloidbildande protein, snarare än att förlita oss på universella regler.
Citering: Badia, M., Batlle, C. & Bolognesi, B. Massively parallel quantification of mutational impact on IAPP amyloid formation. Nat Commun 17, 4076 (2026). https://doi.org/10.1038/s41467-026-70611-z
Nyckelord: typ 2-diabetes, amyloid, IAPP, proteinmutationer, aggregation