Clear Sky Science · he
כימות מקבילי נרחב של השפעת מוטציות על היווצרות עמילואיד של IAPP
מדוע זה חשוב לבריאות היומיומית
סוכרת סוג 2 משפיעה על מאות מיליוני אנשים, ובכל זאת איננו מבינים במלואו מדוע חלק מהאנשים פגיעים יותר מאחרים. הורמון קטן בשם IAPP, המיוצר על ידי אותן תאים שמפרישים אינסולין, עלול להצטבר לסיבים מזיקים שפוגעים בתאים אלה. המחקר הזה בודק באופן שיטתי כמעט אלפיים שינויים זעירים ב‑IAPP כדי לחשוף אילו מהם מחריפים את ההצטברות, אילו מהם מפחיתים אותה, ולמה הידע הזה עשוי בסופו של דבר לסייע בעיצוב טיפולים טובים יותר וכלים לחיזוי סיכון.
כיצד הורמון זעיר הופך למסוכן
IAPP (המכונה גם אמילין) הוא חלבון קצר שמשתחרר מתאים בטא בלבלב יחד עם אינסולין כדי לסייע בבקרת רמת הסוכר בדם. אצל רבים עם סוכרת סוג 2, מולקולות IAPP נערמות לסיבים קשיחים, הידועים כעמילואידים, שפוגעים או הורגים את התאים שמפרישים אותן. מעניין כי גרסאות קרובות של IAPP בבעלי חיים כמו עכברים ודובים כמעט שלא יוצרות סיבים כאלה, ובאותם בעלי חיים נדיר להתפתח סוכרת סוג 2. הניגוד הזה מרמז ששינויים זעירים בבסיסי הבניין של IAPP יכולים להשפיע באופן חזק על הנטייה להצטבר, מה שהופך את IAPP למטרה אידיאלית ל"מבחן עומס" שיטתי של רצף החלבון.
מבחן עצום של אלפי שינויים זעירים
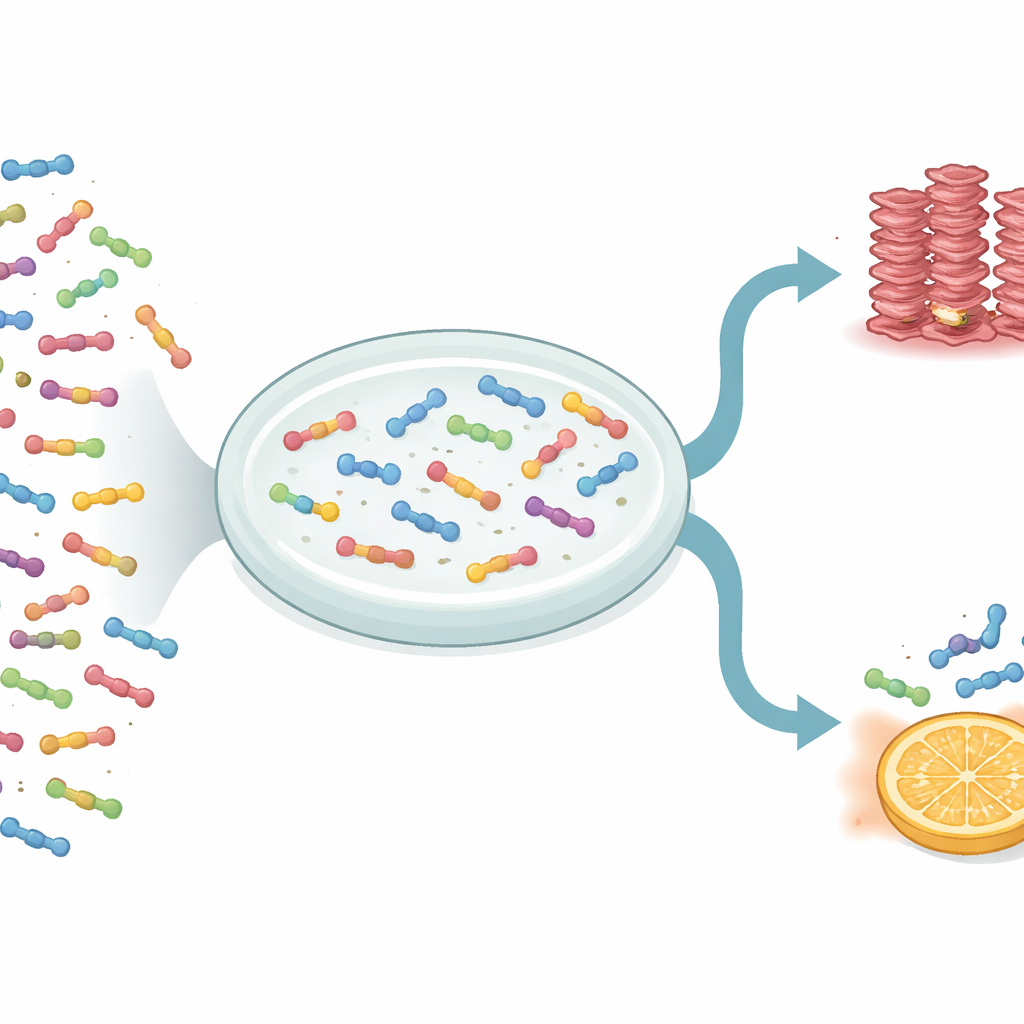
החוקרים השתמשו בגישה פרודוקטיבית גבוהה בשם סריקת מוטציות מעמיקה (deep mutational scanning) כדי לבחון 1,916 וריאנטים שונים של IAPP. הווריאציה כללה החלפת חומצת אמינו באחרת, הכנסת חומצות נוספות, הסרת חלקים וגזירה מקצוות הרצף. למדידת התנהגות כל גרסה חיברו את IAPP לחלבון שבשמרים יוצר מבנים דמויי עמילואיד בתוך תאים. אם וריאנט מסוים של IAPP היה טוב בהשקת ההצטברות, השמרים שנשאו אותו שרדו טוב יותר בתנאי גידול מסוימים. על‑ידי ריצוף ה‑DNA של אוכלוסיית השמרים לפני ואחרי הבחירה, קבעה הקבוצה עד כמה כל שינוי האיץ או האט את השלב ההתחלתי של יצירת הסיבים, שנקרא נוקלאציה.
גרעין פגיע ותכונה מוסתרת של בטיחות
מפת ההשפעות של המוטציות גילתה מקטע מכריע במרכז ה‑IAPP, המשתרע על עמדות 15 עד 32, שנמצא רגיש במיוחד לשינויים. רוב ההחלפות כאן החלישו את ההצטברות, מה שמרמז שמקטע זה יוצר ליבה מובנית בשלבים המוקדמים של הסיב. בתוך מקטע פנימי, בעמדות 21 עד 27, כמעט כל שינוי (למעט בעמדה אחת) האט באופן דרמטי את הנוקלאציה, ואישר שמוטיב קצר זה פועל כגרעין ליבת העמילואיד. המחקר גם גילה אזור "שומר סף" בלתי צפוי מוקדם יותר ברצף, סביב עמדות 11 עד 21. הכנסת חומצות כאן לעתים האיצה את ההצטברות, מה שמרמז שבגרסה הטבעית מקטע זה מסייע לשמור על מולקולות IAPP במצב בטוח יותר שמתנגד להצטברות. פגיעה באזור הזה נראית כשרשרת שמזמנת נוקלאציה מהירה יותר, ורומזת על אתר אפשרי לקשירת תרופות או חלבוני צ'פרון שייצבו את IAPP.
דרכים שונות לצרות במחלות הקשורות למוח וללבלב
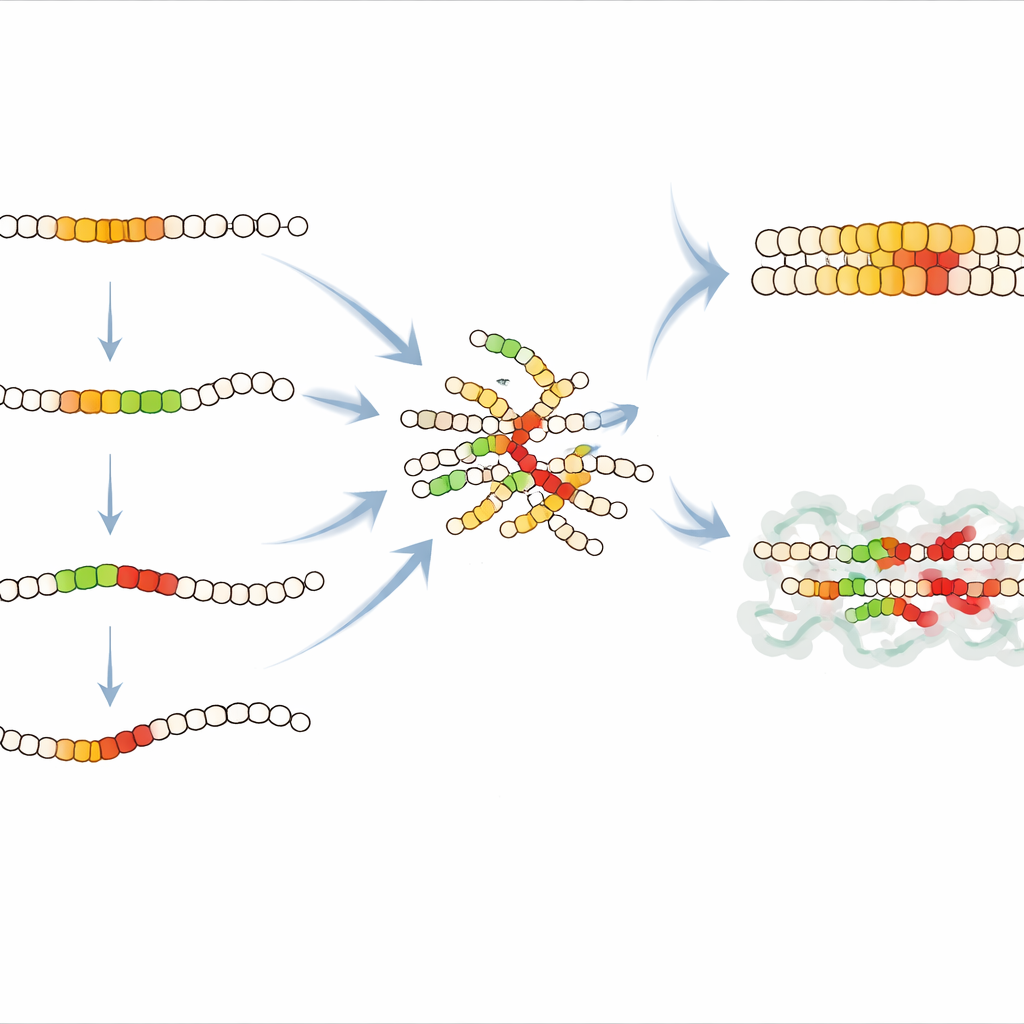
הצוות השווה את ערכת הנתונים של IAPP למפה קודמת, באותה רמת פירוט, עבור עמילואיד β, הפפטיד שיוצר פלאקיות במחלת האלצהיימר. למרות שמדובר באיברים ומחלות בלתי קשורים, ל‑IAPP ולעמילואיד β יש מבני ליבה דומים כשמייצרים סיבים ואף קיימת דמיון מתון ברצף. החוקרים מצאו שמוטציות שמפריעות ליצירת סיבים נוטות להשפיע בשיטות דומות על שני הפפטידים, דבר שמעיד על מצב משותף של שיבוש ליבת העמילואיד. עם זאת, מוטציות שמאיצות את ההצטברות התנהגו שונה מאוד בין שני החלבונים. במילים אחרות, האטת העמילואידים עוקבת כללים משותפים, אך האצתם היא ממוקדת במיוחד לכל פפטיד, ומקשה על שימוש במפה אחת כדי לחזות שינויים מרחיבי־תפקוד מזיקים באחרת.
קישורים לגנטיקה אנושית וטיפולים עתידיים
המחברים בחנו וריאנטים טבעיים של IAPP שנמצאו במאגרי גנומים ציבוריים, כולל UK Biobank. וריאנטים אנושיים נדירים רבים האטו את הנוקלאציה והיו נדירים יותר בקרב אנשים עם סוכרת סוג 2 או רמות סוכר גבוהות לאורך זמן, מה שמרמז שינויים כאלה עשויים להעניק מעט הגנה מפני המחלה. וריאנטים שהגבירו את הנוקלאציה היו נדירים מדי כדי להסיק מסקנות מוצקות לגבי סיכון, אך הם נשארים מועמדים חשובים למחקרים גנטיים וקליניים עתידיים. באופן רחב יותר, העבודה מספקת אטלס מפורט של האופן שבו מוטציות שונות משפיעות על הצטברות IAPP, ומציעה מדריך מושכל לעיצוב תרופות מבוססות IAPP שישמרו על תפקוד ההורמון אך יתנגדו ליצירת סיבים מזיקים. המחקר גם מדגיש מסר רחב יותר: כדי להבין ולחזות הצטברות חלבונים מזיקה במחלות אנושיות, סביר שנצטרך מפות כמותיות דומות לכל חלבון יוצר‑עמילואיד, במקום להסתמך על כללים כלליים יחידים.»
ציטוט: Badia, M., Batlle, C. & Bolognesi, B. Massively parallel quantification of mutational impact on IAPP amyloid formation. Nat Commun 17, 4076 (2026). https://doi.org/10.1038/s41467-026-70611-z
מילות מפתח: סוכרת סוג 2, עמילואיד, IAPP, מוטציות בחלבונים, הצטברות