Clear Sky Science · it
Quantificazione su larga scala dell’impatto mutazionale sulla formazione di amiloidi di IAPP
Perché questo conta per la salute quotidiana
Il diabete di tipo 2 colpisce centinaia di milioni di persone, eppure non comprendiamo ancora completamente perché alcuni individui siano più vulnerabili di altri. Un piccolo ormone chiamato IAPP, prodotto dalle stesse cellule che sintetizzano l’insulina, può aggregarsi in fibre dannose che danneggiano queste cellule. Questo studio testa in modo sistematico quasi duemila piccole modifiche all’IAPP per rivelare quali peggiorano l’aggregazione, quali la rendono più sicura e perché questa conoscenza potrebbe in futuro aiutare a progettare terapie migliori e strumenti di previsione del rischio.
Come un ormone minuscolo diventa dannoso
L’IAPP (detto anche amilina) è una proteina breve rilasciata dalle cellule beta pancreatiche insieme all’insulina per contribuire al controllo della glicemia. In molte persone con diabete di tipo 2, le molecole di IAPP si impilano in fibre rigide, note come amiloidi, che danneggiano o uccidono le stesse cellule che le secernono. È interessante che versioni strettamente correlate di IAPP in animali come topi e orsi quasi mai formino queste fibre, e quegli animali sviluppano raramente il diabete di tipo 2. Questo contrasto suggerisce che piccole modifiche nei mattoni dell’IAPP possono influenzare fortemente la tendenza all’aggregazione, rendendo l’IAPP un bersaglio ideale per un “test di stress” sistematico della sua sequenza.
Un test massiccio di migliaia di piccole modifiche
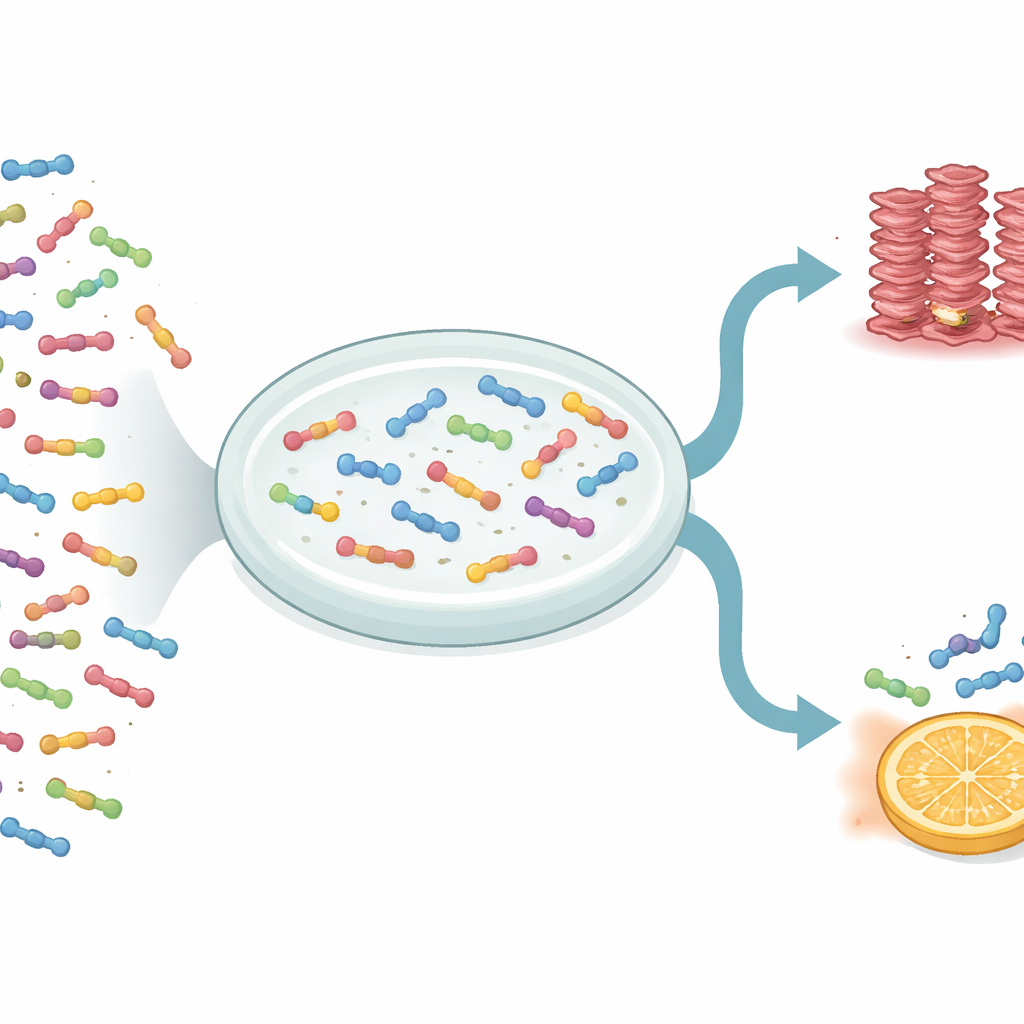
I ricercatori hanno usato un approccio ad alto rendimento chiamato deep mutational scanning per esaminare 1.916 versioni diverse di IAPP. Questi varianti includevano la sostituzione di un singolo mattoncino (amminoacido) con un altro, l’inserimento di residui aggiuntivi, l’eliminazione di alcuni e il troncamento dalle estremità. Per misurare il comportamento di ciascuna variante, hanno fuso l’IAPP a una proteina di lievito che forma assemblee simili a amiloidi all’interno delle cellule di lievito. Se una particolare variante di IAPP favoriva l’innesco dell’aggregazione, il lievito che la portava sopravviveva meglio in condizioni di crescita specifiche. Sequenziando il DNA della popolazione di lievito prima e dopo la selezione, il team ha quantificato quanto ciascuna modifica accelerasse o rallentasse il passo iniziale della formazione delle fibre, chiamato nucleazione.
Un nucleo vulnerabile e una caratteristica di sicurezza nascosta
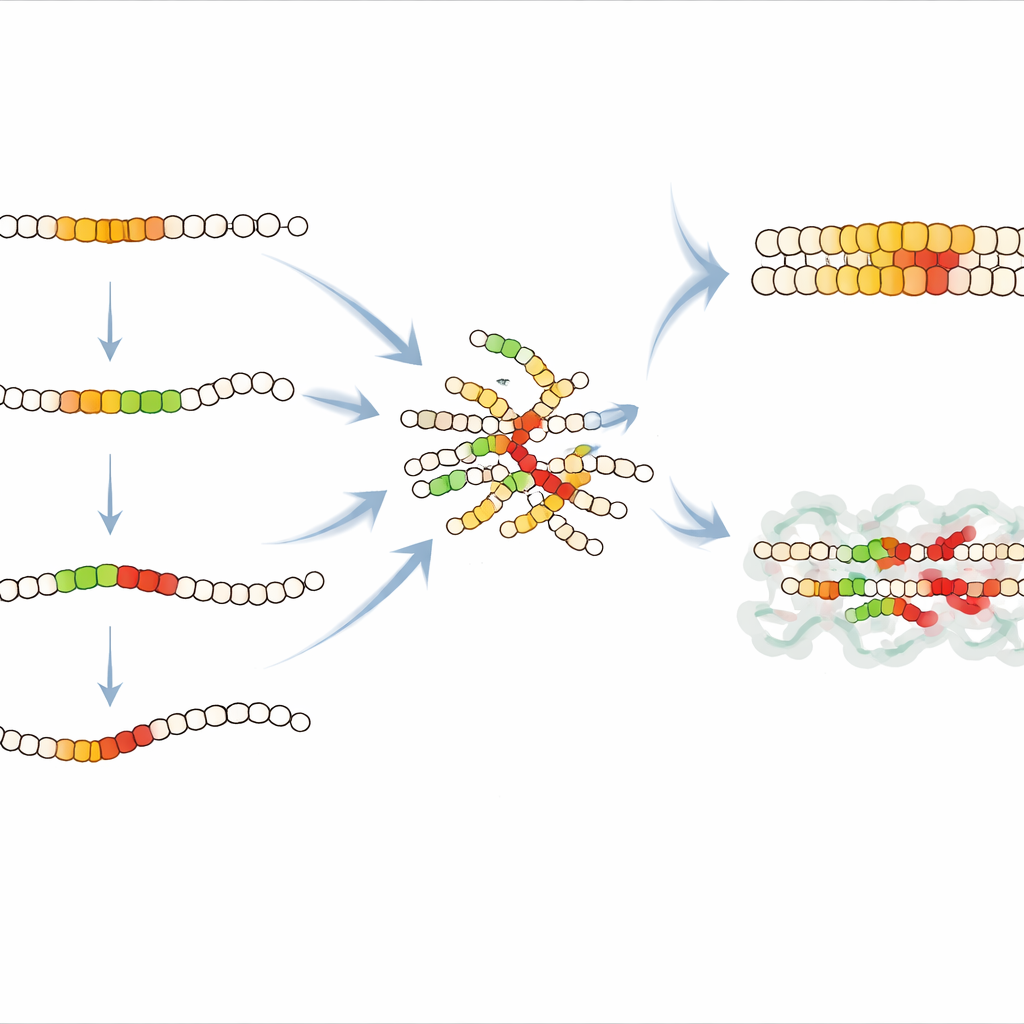
La mappa degli effetti mutazionali ha rivelato una porzione cruciale al centro dell’IAPP, che comprende le posizioni dalla 15 alla 32, particolarmente sensibile alle modifiche. La maggior parte delle alterazioni in questa regione indeboliva l’aggregazione, indicando che questa sequenza forma un nucleo strutturato nelle fasi iniziali della fibra. All’interno di un segmento interno, nelle posizioni dalla 21 alla 27, quasi qualsiasi cambiamento (tranne che in una posizione) rallentava drasticamente la nucleazione, confermando che questo breve motivo funge da cuore del nucleo amiloide. Lo studio ha inoltre scoperto una inaspettata regione “guardiana” all’inizio della sequenza, intorno alle posizioni 11–21. L’inserimento di amminoacidi qui spesso accelerava l’aggregazione, suggerendo che, nella sequenza naturale, questo segmento aiuta a mantenere le singole molecole di IAPP in una conformazione più sicura e resistente all’aggregazione. La sua perturbazione sembra sbloccare una nucleazione più rapida, indicando un possibile sito dove farmaci o proteine chaperon potrebbero legarsi e stabilizzare l’IAPP.
Vie diverse verso il danno in malattie correlate di cervello e pancreas
Il team ha confrontato il proprio dataset su IAPP con una mappa precedente, altrettanto dettagliata, per l’amiloide beta, il peptide che forma le placche nella malattia di Alzheimer. Nonostante organi e malattie diversi, IAPP e amiloide beta condividono strutture del nucleo simili quando formano fibre e mostrano persino una somiglianza moderata di sequenza. I ricercatori hanno trovato che le mutazioni che interferiscono con la formazione delle fibre tendono ad avere effetti analoghi su entrambi i peptidi, suggerendo una modalità comune di perturbazione del nucleo amiloide. Tuttavia, le mutazioni che accelerano l’aggregazione si comportano in modo molto diverso tra le due proteine. In altre parole, rallentare questi amiloidi segue regole comuni, ma accelerarli sembra essere altamente specifico per ciascun peptide, rendendo difficile usare un dataset per prevedere guadagni di funzione dannosi in un altro.
Collegamenti con la genetica umana e terapie future
Gli autori hanno esaminato varianti naturali di IAPP presenti in banche dati genomiche pubbliche, incluso l’UK Biobank. Molte varianti umane rare rallentavano la nucleazione e risultavano meno comuni tra gli individui con diabete di tipo 2 o con livelli glicemici elevati a lungo termine, suggerendo che tali cambiamenti potrebbero proteggere lievemente dalla malattia. Le varianti che aumentavano la nucleazione erano troppo rare per trarre conclusioni solide sul rischio, ma restano candidati importanti per futuri studi genetici e clinici. Più in generale, il lavoro fornisce un atlante dettagliato di come diverse mutazioni influenzano l’aggregazione dell’IAPP, offrendo una guida razionale per progettare nuovi farmaci basati su IAPP che mantengano la funzione ormonale ma resistano alla formazione di fibre dannose. Sottolinea inoltre un messaggio più ampio: per comprendere e prevedere l’aggregazione proteica dannosa nelle malattie umane, probabilmente avremo bisogno di mappe quantitative simili per ciascuna proteina che forma amiloidi, invece di fare affidamento su regole universali.
Citazione: Badia, M., Batlle, C. & Bolognesi, B. Massively parallel quantification of mutational impact on IAPP amyloid formation. Nat Commun 17, 4076 (2026). https://doi.org/10.1038/s41467-026-70611-z
Parole chiave: diabete di tipo 2, amiloide, IAPP, mutazioni proteiche, aggregazione