Clear Sky Science · ja
IAPPのアミロイド形成に対する変異の影響を大規模並列で定量化
日常の健康にとっての意義
2型糖尿病は何億人もの人々に影響を与えますが、なぜ個人差が生じるのかは完全には解明されていません。インスリンと同じ細胞で作られる小さなホルモン、IAPPは有害な線維に凝集してこれらの細胞を傷つけることがあります。本研究はIAPPに対する約2,000の小さな変化を体系的に検査し、どの変化が凝集を悪化させ、どれが抑えるのか、そしてこの知見が将来的に治療法やリスク予測ツールの設計にどう役立つ可能性があるかを明らかにします。
小さなホルモンが有害になる仕組み
IAPP(アミリンとも呼ばれる)は、血糖を制御するために膵β細胞からインスリンとともに分泌される短いタンパク質です。多くの2型糖尿病患者では、IAPP分子が剛直な線維(アミロイド)として積み重なり、それらを分泌する細胞自体を傷害・死滅させます。興味深いことに、マウスやクマなどの動物に見られる類縁のIAPPはほとんどこれらの線維を形成せず、そのような動物では2型糖尿病が稀です。この対比は、IAPPの構成要素の小さな変化が凝集性に強く影響することを示唆しており、IAPPが配列の系統的“ストレステスト”に理想的な標的であることを示しています。
数千の小さな変化に対する大規模なテスト
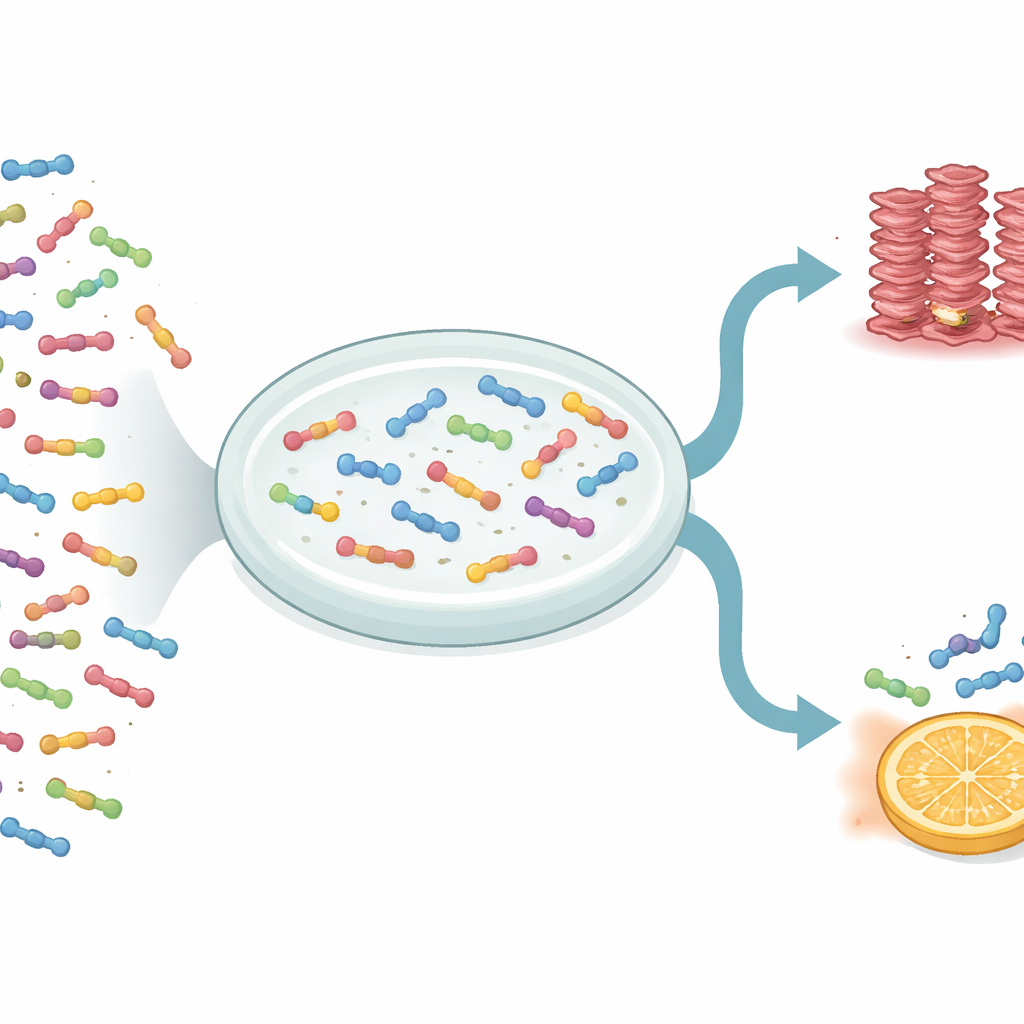
研究者らはディープ・ミューテーショナル・スキャンニングと呼ばれるハイスループット手法を用いて、1,916種類のIAPPバリアントを調べました。これらの変異は、アミノ酸の置換、挿入、欠失、および末端の切り詰めを含みます。各バリアントの挙動を測定するために、IAPPを酵母内でアミロイド様集合を形成する酵母タンパク質に融合しました。あるIAPP変異体が凝集の開始をよく促進する場合、その変異体を持つ酵母は特定の成長条件下でよりよく生き残りました。選択前後の酵母集団のDNAをシーケンシングすることで、各変化が重合の初期段階である核生成(ヌクレーション)をどの程度促進または抑制するかを定量化しました。
脆弱なコアと隠れた安全機構
変異効果のマップは、特に変化に敏感なIAPPの中間領域(位置15から32)を明らかにしました。ここでの大部分の変化は凝集を弱め、この領域が初期線維における構造化されたコアを形成することを示しています。内側の短いセグメント(位置21から27)では、ある一箇所を除いてほとんどの変化が核生成を劇的に遅らせ、この短いモチーフがアミロイドコアの心臓部として機能することを裏付けました。研究はまた、配列のやや前方(位置11から21付近)に予期せぬ“ゲートキーパー”領域を発見しました。ここへのアミノ酸の挿入はしばしば凝集を加速させ、自然配列ではこの領域が単一のIAPP分子を凝集しにくい安全な形に保つ役割を果たしていることを示唆します。これを乱すと核生成が促進されるため、薬剤やシャペロンタンパク質が結合してIAPPを安定化する標的になり得る可能性があります。
関連する脳や膵臓の疾患での異なるトラブル経路
研究チームは、アルツハイマー病でプラークを形成するペプチドであるアミロイドβについての同様に詳細な既存データとIAPPのデータセットを比較しました。器官や疾患は異なるにもかかわらず、IAPPとアミロイドβは線維形成時に類似したコア構造を持ち、配列にも中程度の類似性が見られます。研究者らは、線維形成を妨げる変異は両ペプチドに対して類似の影響を及ぼす傾向があることを見出し、アミロイドコアの破壊に共通のモードが存在することを示唆しました。しかし、凝集を加速する変異の振る舞いは両者で大きく異なりました。言い換えれば、これらのアミロイドを遅らせる仕組みには共通ルールがある一方で、加速させる経路は各ペプチドに特有であり、あるデータセットから別のペプチドの有害な機能獲得変化を予測するのは難しいことが示されました。
ヒト遺伝学との関連と将来の治療法
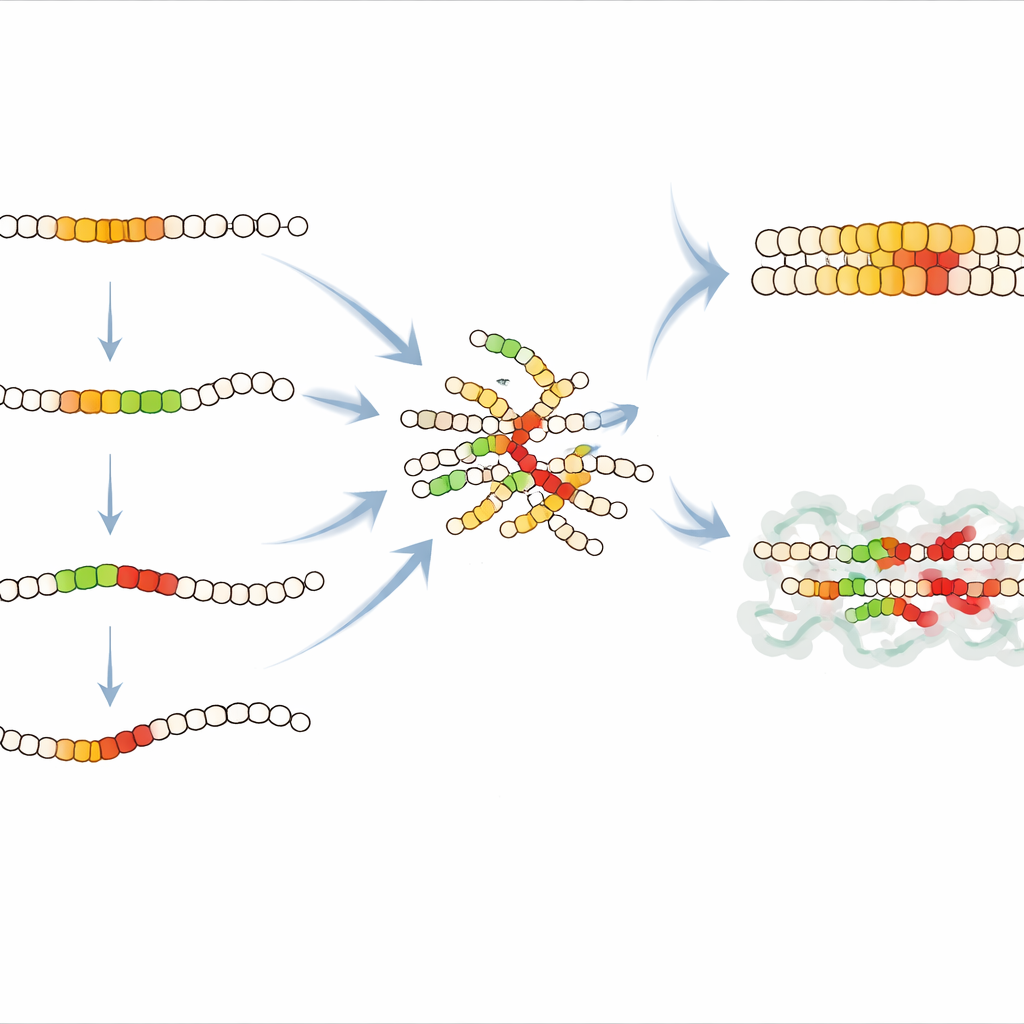
著者らはUKバイオバンクを含む公開ゲノムデータベースで見つかる自然発生のIAPP変異を検討しました。多くの稀なヒト変異は核生成を遅らせ、2型糖尿病や長期的な高血糖のある個人であまり見られない傾向があり、そのような変化がわずかに疾患から保護している可能性を示唆しています。核生成を増加させる変異はあまりに稀でリスクについて確固たる結論は出せませんが、今後の遺伝学的・臨床的研究の重要な候補として残ります。より広く見れば、この研究は異なる変異がIAPPの凝集にどのように影響するかの詳細なアトラスを提供し、ホルモン機能を保ちながら有害な線維化を避ける新しいIAPPベースの薬剤設計の合理的指針を与えます。また、人の疾患における有害なタンパク質凝集を理解し予測するには、汎用のルールに頼るのではなく、各アミロイド形成タンパク質について同様の定量的マップが必要になるだろうというより大きな教訓を強調しています。
引用: Badia, M., Batlle, C. & Bolognesi, B. Massively parallel quantification of mutational impact on IAPP amyloid formation. Nat Commun 17, 4076 (2026). https://doi.org/10.1038/s41467-026-70611-z
キーワード: 2型糖尿病, アミロイド, IAPP, タンパク質変異, 凝集