Clear Sky Science · pl
Masowo równoległa ilościowa ocena wpływu mutacji na tworzenie amyloidu IAPP
Dlaczego to ma znaczenie dla codziennego zdrowia
Cukrzyca typu 2 dotyka setek milionów ludzi, a mimo to wciąż nie rozumiemy w pełni, dlaczego niektórzy są bardziej podatni niż inni. Mały hormon zwany IAPP, wytwarzany przez te same komórki, które produkują insulinę, może zlepiać się w szkodliwe włókna, które uszkadzają te komórki. W tym badaniu systematycznie przetestowano prawie dwa tysiące drobnych zmian w IAPP, aby ustalić, które pogarszają zlepianie, które je łagodzą, oraz dlaczego ta wiedza może w przyszłości pomóc w projektowaniu lepszych terapii i narzędzi do przewidywania ryzyka.
Jak malutki hormon staje się szkodliwy
IAPP (znany też jako amylina) to krótki peptyd uwalniany przez komórki beta trzustki razem z insuliną, by pomagać w kontroli poziomu cukru we krwi. U wielu osób z cukrzycą typu 2 cząsteczki IAPP układają się w sztywne włókna, zwane amyloidami, które uszkadzają lub zabijają komórki je wydzielające. Co ciekawe, blisko spokrewnione wersje IAPP u zwierząt, takich jak myszy czy niedźwiedzie, niemal nigdy nie tworzą tych włókien, a te gatunki rzadko rozwijają cukrzycę typu 2. Ten kontrast sugeruje, że niewielkie zmiany w budulcu IAPP mogą silnie wpływać na tendencję do zlepiania, co czyni IAPP idealnym celem do systematycznego „testu obciążeniowego” sekwencji.
Ogromny test tysięcy drobnych zmian
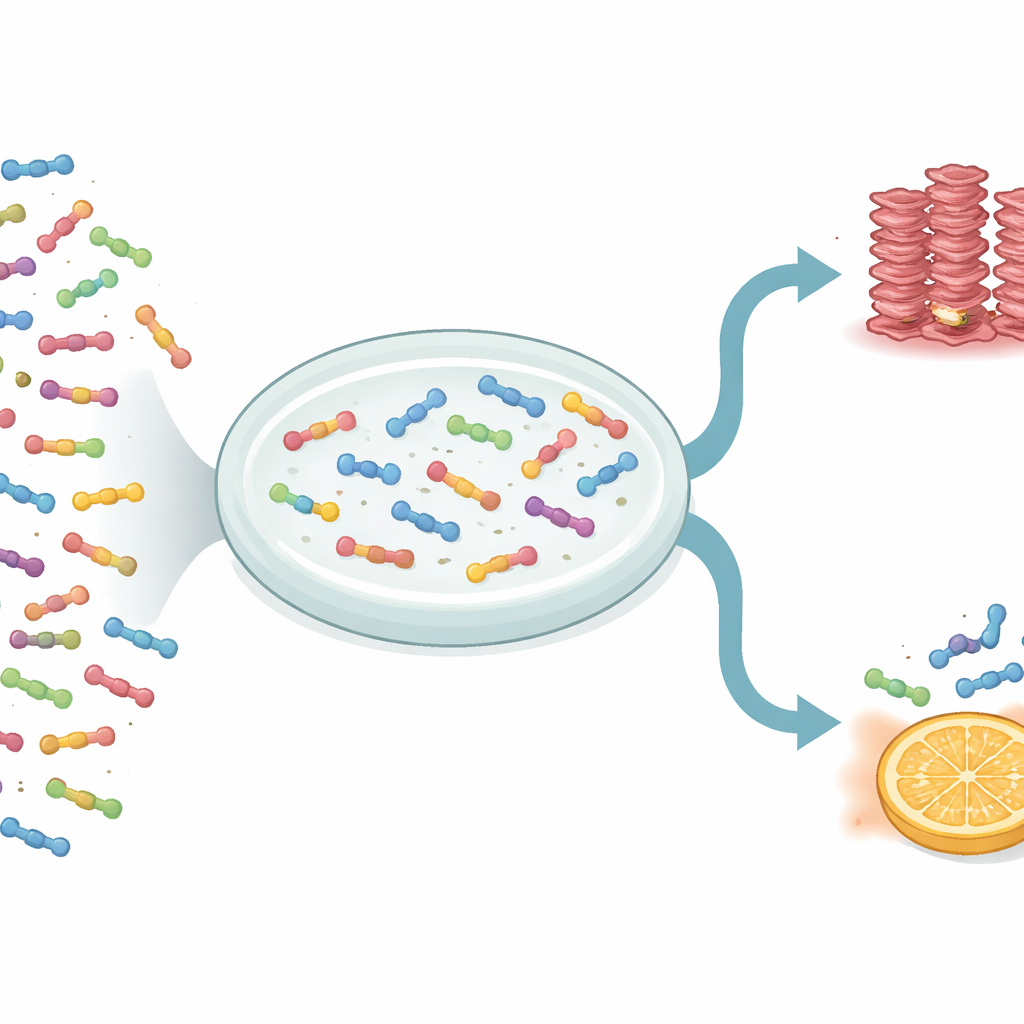
Naukowcy zastosowali metodę wysokoprzepustową zwaną deep mutational scanning, aby zbadać 1 916 różnych wariantów IAPP. Warianty obejmowały zamianę jednego aminokwasu na inny, wstawianie dodatkowych, usuwanie niektórych oraz obcinanie końców. Aby zmierzyć zachowanie każdego wariantu, połączyli IAPP z białkiem drożdżowym, które tworzy struktury podobne do amyloidów wewnątrz komórek drożdży. Jeśli dany wariant IAPP sprzyjał inicjacji zlepiania, drożdże go noszące lepiej przeżywały w określonych warunkach hodowli. Poprzez sekwencjonowanie DNA populacji drożdży przed i po selekcji zespół zmierzył, jak silnie każda zmiana przyspieszała lub opóźniała początkowy etap tworzenia włókien, zwany nukleacją.
Wrażliwe jądro i ukryte zabezpieczenie
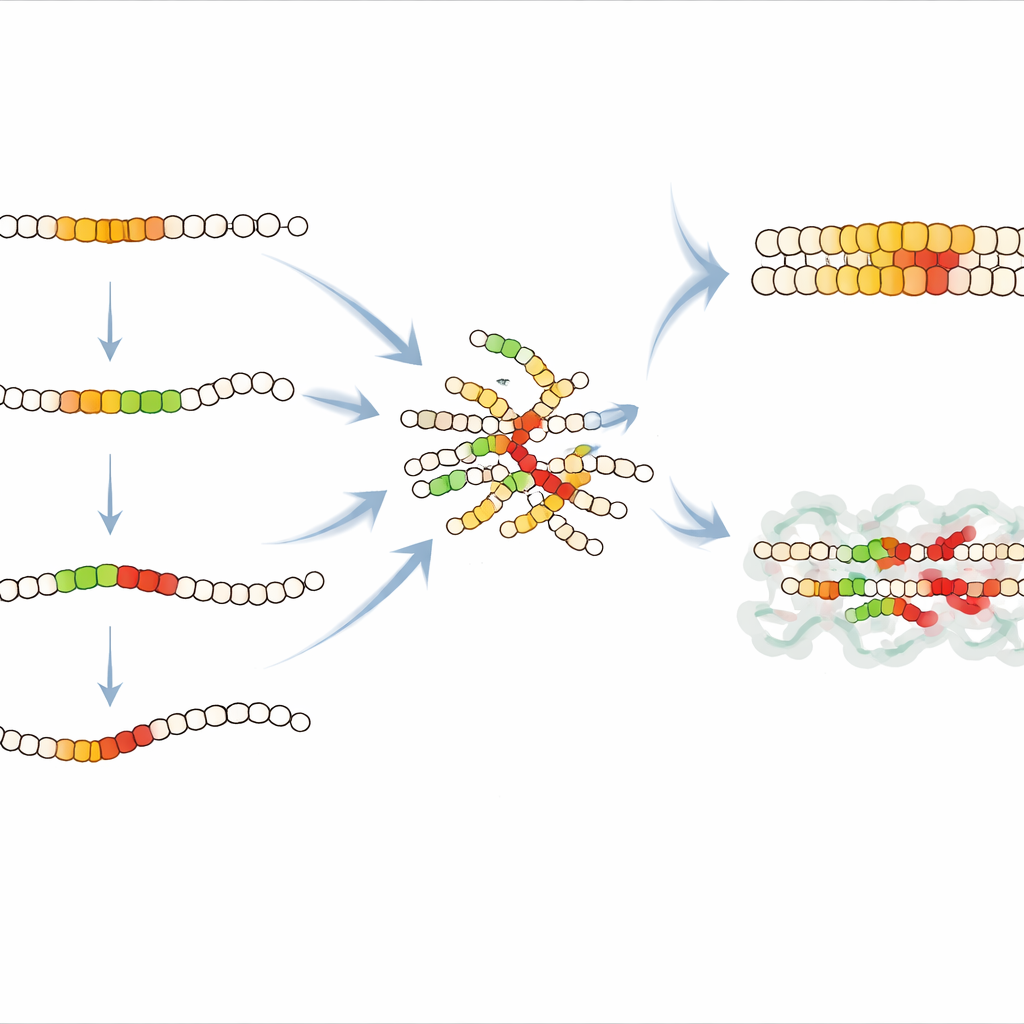
Mapa efektów mutacji ujawniła kluczowy fragment w środkowej części IAPP, obejmujący pozycje 15–32, który jest szczególnie wrażliwy na zmiany. Większość modyfikacji w tym obszarze osłabiała zlepianie, co wskazuje, że region ten tworzy uporządkowane jądro we wczesnych włóknach. W wewnętrznym segmencie, na pozycjach 21–27, niemal każda zmiana (z wyjątkiem jednej pozycji) dramatycznie spowalniała nukleację, potwierdzając, że ten krótki motyw działa jako serce rdzenia amyloidu. Badanie odkryło także nieoczekiwany „strażnik” wcześniej w sekwencji, w rejonie pozycji 11–21. Wstawianie dodatkowych aminokwasów w tym miejscu często przyspieszało zlepianie, co sugeruje, że w naturalnej sekwencji segment ten pomaga utrzymać pojedyncze cząsteczki IAPP w bezpieczniejszym kształcie odpornym na agregację. Jego naruszenie wydaje się odblokowywać szybszą nukleację, co wskazuje potencjalne miejsce wiązania dla leków lub białek opiekuńczych stabilizujących IAPP.
Różne drogi do problemów w pokrewnych chorobach mózgu i trzustki
Zespół porównał swoje dane dotyczące IAPP z wcześniejszą, równie szczegółową mapą dla amyloidu beta, peptydu tworzącego blaszki w chorobie Alzheimera. Pomimo że dotyczą różnych narządów i chorób, IAPP i amyloid beta mają podobne struktury rdzenia przy tworzeniu włókien i wykazują umiarkowane podobieństwo sekwencji. Badacze odkryli, że mutacje zakłócające tworzenie włókien zwykle wpływają na oba peptydy w podobny sposób, co sugeruje wspólny mechanizm destabilizacji rdzenia amyloidu. Natomiast mutacje przyspieszające zlepianie zachowywały się bardzo różnie między tymi dwoma białkami. Innymi słowy, spowalnianie tych amyloidów podlega wspólnym regułom, ale przyspieszanie jest wysoce specyficzne dla każdego peptydu, co utrudnia użycie jednego zestawu danych do przewidywania szkodliwych zysków funkcji w innym.
Powiązania z genetyką ludzi i przyszłymi terapiami
Autorzy przeanalizowali naturalnie występujące warianty IAPP znalezione w publicznych bazach genomowych, w tym w UK Biobank. Wiele rzadkich wariantów ludzkich spowalniało nukleację i wydawało się mniej powszechnych wśród osób z cukrzycą typu 2 lub z wyższymi długoterminowymi poziomami glukozy, co sugeruje, że takie zmiany mogą nieco chronić przed chorobą. Warianty zwiększające nukleację były zbyt rzadkie, by wyciągać pewne wnioski o ryzyku, ale pozostają istotnymi kandydatami do przyszłych badań genetycznych i klinicznych. Szerzej rzecz biorąc, praca dostarcza szczegółowej mapy wpływu różnych mutacji na agregację IAPP, oferując racjonalny przewodnik do projektowania nowych leków opartych na IAPP, które zachowują funkcję hormonu, ale opierają się tworzeniu szkodliwych włókien. Podkreśla też szerszy wniosek: aby rozumieć i przewidywać szkodliwe zlepianie białek w chorobach ludzkich, prawdopodobnie potrzebne będą podobne, ilościowe mapy dla każdego białka tworzącego amyloid, zamiast polegać na uniwersalnych regułach.
Cytowanie: Badia, M., Batlle, C. & Bolognesi, B. Massively parallel quantification of mutational impact on IAPP amyloid formation. Nat Commun 17, 4076 (2026). https://doi.org/10.1038/s41467-026-70611-z
Słowa kluczowe: cukrzyca typu 2, amyloid, IAPP, mutacje białek, agregacja