Clear Sky Science · fr
Quantification massivement parallèle de l’impact des mutations sur la formation d’amyloïde d’IAPP
Pourquoi cela compte pour la santé quotidienne
Le diabète de type 2 touche des centaines de millions de personnes, et pourtant nous ne comprenons pas entièrement pourquoi certains individus sont plus vulnérables que d’autres. Une petite hormone appelée IAPP, produite par les mêmes cellules qui sécrètent l’insuline, peut s’agglomérer en fibres nocives qui endommagent ces cellules. Cette étude teste systématiquement près de deux mille petites modifications d’IAPP pour révéler lesquelles aggravent l’agrégation, lesquelles la rendent plus sûre, et pourquoi ces connaissances pourraient à terme aider à concevoir de meilleurs traitements et outils de prédiction du risque.
Comment une petite hormone devient dangereuse
L’IAPP (appelée aussi amyline) est une courte protéine libérée par les cellules bêta du pancréas avec l’insuline pour aider à réguler la glycémie. Chez de nombreuses personnes atteintes de diabète de type 2, les molécules d’IAPP s’empilent en fibres rigides, appelées amyloïdes, qui blessent ou tuent les cellules qui les sécrètent. Fait intéressant, des versions étroitement apparentées d’IAPP chez des animaux comme les souris ou les ours forment presque jamais ces fibres, et ces animaux développent rarement un diabète de type 2. Ce contraste suggère que de petites modifications des constituants d’IAPP peuvent fortement influencer sa tendance à s’agréger, faisant d’IAPP une cible idéale pour un « test de résistance » systématique de sa séquence.
Un test massif de milliers de petites modifications
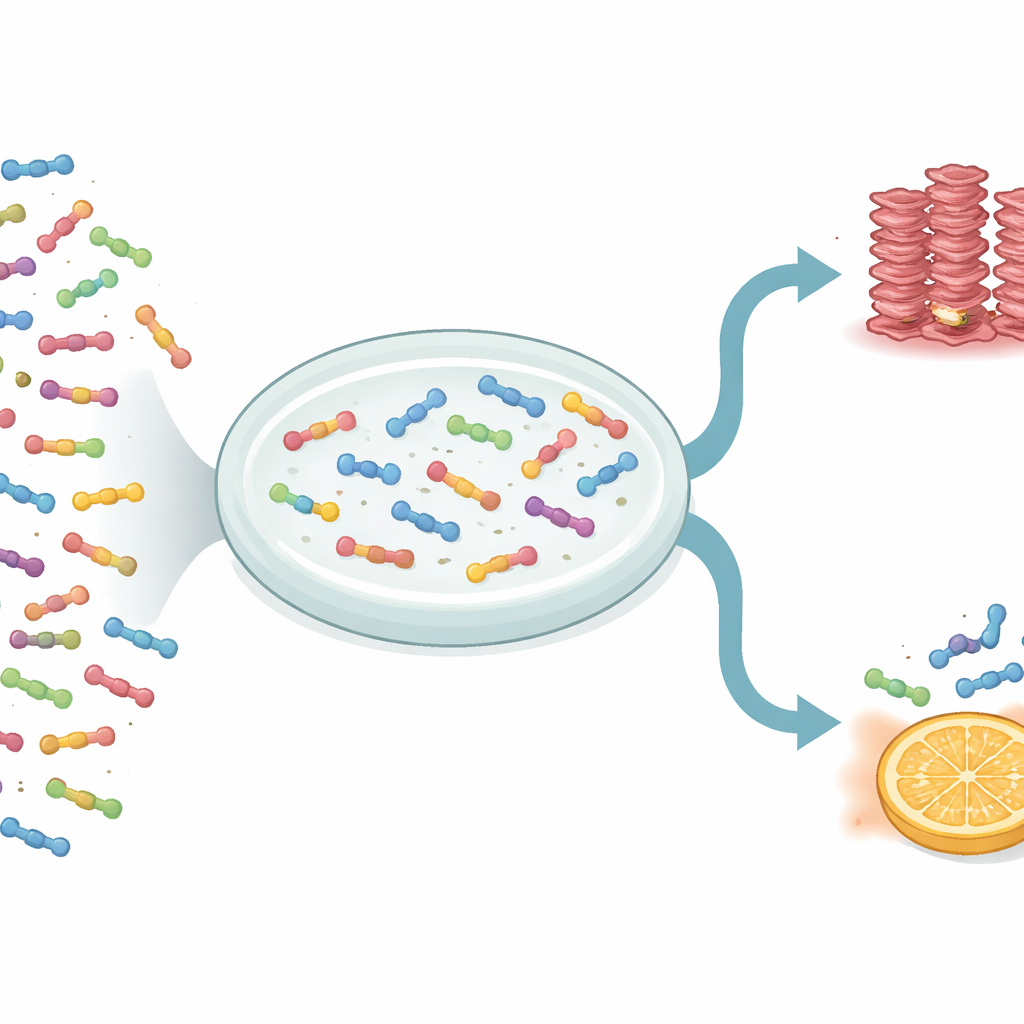
Les chercheurs ont utilisé une approche à haut débit appelée deep mutational scanning pour examiner 1 916 versions différentes d’IAPP. Ces variantes comprenaient le remplacement d’un constituant (acide aminé) par un autre, l’insertion d’acides aminés supplémentaires, la suppression de certains, et l’élagage d’extrémités. Pour mesurer le comportement de chaque version, ils ont fusionné l’IAPP à une protéine de levure qui forme des assemblages de type amyloïde à l’intérieur des cellules de levure. Si une variante d’IAPP favorisait le démarrage de l’agrégation, la levure la portant survivait mieux dans des conditions de croissance spécifiques. En séquençant l’ADN de la population de levures avant et après sélection, l’équipe a quantifié dans quelle mesure chaque changement accélère ou ralentit l’étape initiale de formation des fibres, appelée nucléation.
Un noyau vulnérable et un dispositif de sécurité caché
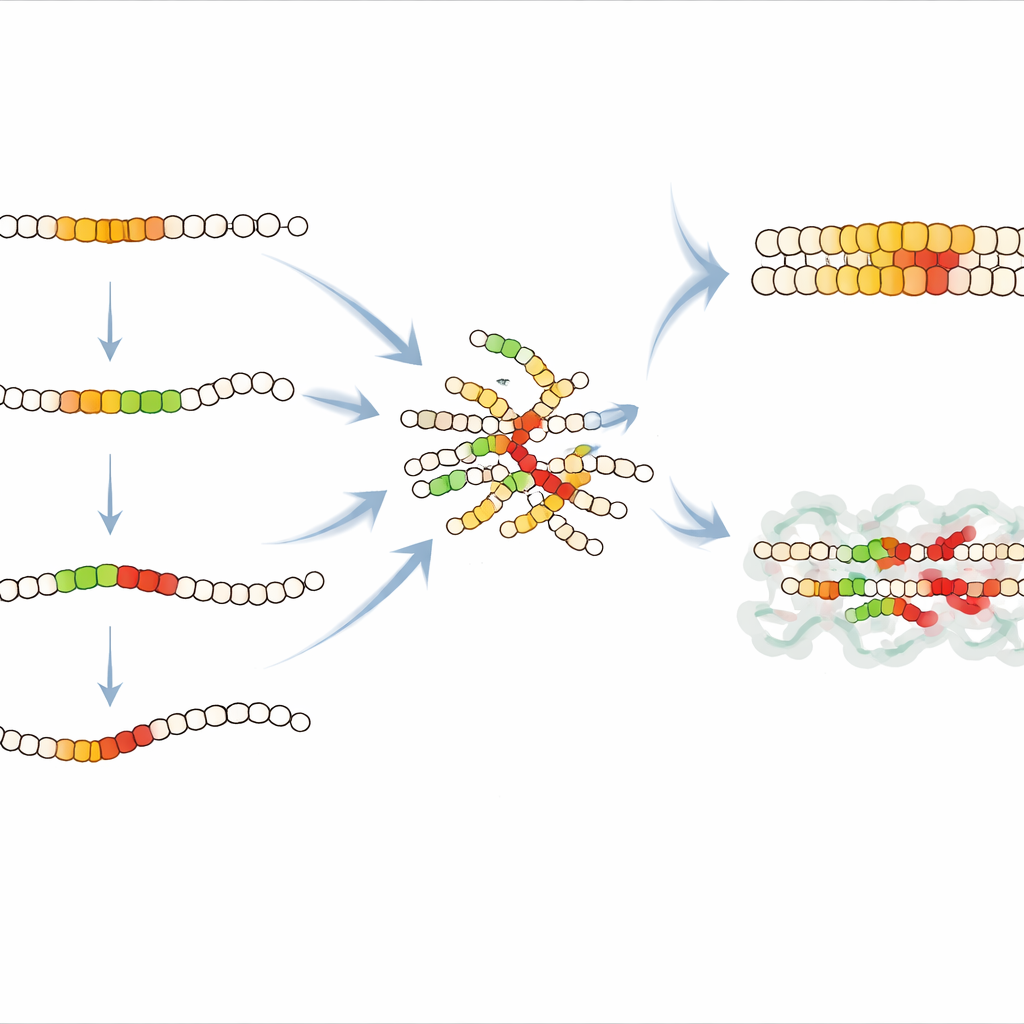
La carte des effets des mutations a révélé une portion cruciale au centre d’IAPP, couvrant les positions 15 à 32, particulièrement sensible aux modifications. La plupart des altérations dans cette région affaiblissaient l’agrégation, indiquant que ce segment forme un noyau structuré lors des premières étapes de la fibre. Dans un segment interne, positions 21 à 27, presque toute modification (sauf à une position) ralentissait dramatiquement la nucléation, confirmant que ce court motif constitue le cœur du noyau amyloïde. L’étude a également mis au jour une région « gardienne » inattendue plus en amont de la séquence, autour des positions 11 à 21. L’insertion d’acides aminés dans cette zone accélère souvent l’agrégation, ce qui implique que, dans la séquence naturelle, ce segment aide à maintenir les molécules d’IAPP dans une conformation plus sûre qui résiste à l’agrégation. La perturbation de cette région semble libérer une nucléation plus rapide, suggérant un site possible pour des médicaments ou des protéines chaperonnes visant à se lier et stabiliser l’IAPP.
Différents chemins vers la pathologie dans les maladies apparentées du cerveau et du pancréas
L’équipe a comparé son jeu de données sur l’IAPP à une carte précédente, tout aussi détaillée, pour la bêta-amyloïde, le peptide qui forme les plaques dans la maladie d’Alzheimer. Malgré des organes et des maladies distincts, l’IAPP et la bêta-amyloïde partagent des structures de noyau similaires lorsqu’elles forment des fibres et présentent même une similarité modérée de séquence. Les chercheurs ont constaté que les mutations qui perturbent la formation des fibres tendent à affecter les deux peptides de manière similaire, suggérant un mode commun d’altération du noyau amyloïde. En revanche, les mutations qui accélèrent l’agrégation se comportent très différemment entre les deux protéines. Autrement dit, ralentir ces amyloïdes obéit à des règles communes, mais les accélérer semble très spécifique à chaque peptide, rendant difficile l’utilisation d’un jeu de données pour prédire des gains de fonction nocifs dans un autre.
Liens avec la génétique humaine et perspectives thérapeutiques
Les auteurs ont examiné des variantes naturelles d’IAPP présentes dans des bases de données génomiques publiques, dont l’UK Biobank. De nombreuses variantes humaines rares ralentissaient la nucléation et semblaient moins fréquentes chez les personnes atteintes de diabète de type 2 ou présentant une hyperglycémie chronique, laissant penser que de telles modifications pourraient conférer une petite protection contre la maladie. Les variantes augmentant la nucléation étaient trop rares pour tirer des conclusions solides sur le risque, mais elles restent des candidates importantes pour de futures études génétiques et cliniques. Plus largement, ce travail fournit un atlas détaillé de l’influence des différentes mutations sur l’agrégation d’IAPP, offrant une boussole rationnelle pour concevoir de nouveaux médicaments basés sur l’IAPP qui conservent la fonction hormonale tout en résistant à la formation de fibres délétères. Il souligne aussi un message plus large : pour comprendre et prédire l’agrégation protéique pathogène dans les maladies humaines, il faudra probablement des cartes quantitatives similaires pour chaque protéine formant des amyloïdes, plutôt que de s’appuyer sur des règles universelles.
Citation: Badia, M., Batlle, C. & Bolognesi, B. Massively parallel quantification of mutational impact on IAPP amyloid formation. Nat Commun 17, 4076 (2026). https://doi.org/10.1038/s41467-026-70611-z
Mots-clés: diabète de type 2, amyloïde, IAPP, mutations protéiques, agrégation