Clear Sky Science · sv
En hierarkisk theranostisk nanoagent för multimodal avbildning och riktad intervention mot skumceller vid åderförkalkning
Varför tilltäppta artärer spelar roll
Åderförkalkning — den gradvisa tilltäppningen och försvagningen av våra artärer — är den dolda drivkraften bakom hjärtinfarkter och stroke. Djup inne i artärväggarna sväller immunceller av fett och förvandlas till så kallade skumceller, som hjälper plack att växa och bli sköra. Läkare kan se stora, sena plack med dagens skannrar, men de har svårt att upptäcka och behandla farliga plack i ett tidigt skede, när insatser skulle kunna förebygga katastrof. Denna studie presenterar en smart, flerlager nanopartikel som både kan belysa dessa riskfyllda områden med flera avbildningsmetoder och direkt dämpa och reparera dem i sjuka artärer hos möss.
Se problem i artärerna från flera vinklar
Forskarna designade först en särskild färgämnesmolekyl som fungerar som ett tre‑i‑ett-sändare. Den lyser i ett djupt nära‑infrarött ljus, ger upphov till ultraljudssignaler när den pulseras med en laser (fotoakustisk avbildning), och förbättrar magnetisk resonansavbildning (MRI). Var och en av dessa metoder ser kroppen på olika sätt: den infraröda glöden är mycket känslig och snabb, fotoakustik ger skarpa strukturella detaljer några centimeter djupt, och MRI kartlägger anatomin i hela kroppen utan joniserande strålning. Genom att noggrant ställa in färgämnets struktur och koppla på en gadoliniumenhet som används i MRI, skapade teamet en enda molekyl som ger starka signaler i alla tre systemen och förblir stabil även under krävande biologiska förhållanden.
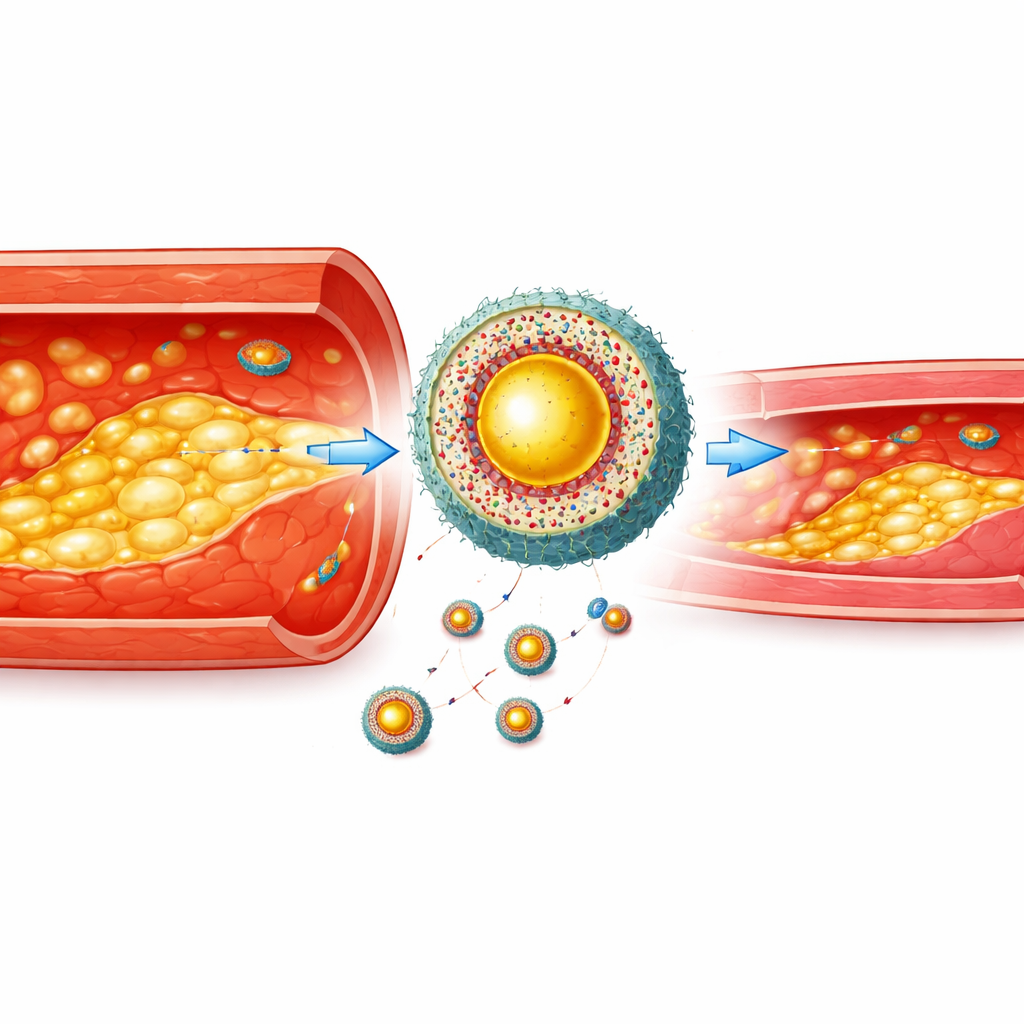
Bygga ett målinriktat hölje för sjuka celler
En lysande avbildningsmarkör räcker inte i sig — den måste nå rätt plats och stanna där. Forskarna inkapslade den multimodala färgämnet och kolesterolsänkande läkemedlet atorvastatin inne i ett polymerskal som faller sönder i närvaro av höga nivåer av reaktiva syreradikaler, ett kemiskt kännetecken för inflammerade skumceller. För att hjälpa partiklarna att smita igenom inflammerade kärlväggar och rikta in sig på skumceller svepte de partiklarna i äkta makrofag (immuncell)membran och lade till en kort peptid som binder till en ”ät mig”-signal som exponeras på skumcellernas yta. Detta skapade en hierarkisk nanoagent: först lockas den till inflammerade artärväggar, sedan mer precist till skumceller gömda i placket, och slutligen aktiveras den av den stressade kemiska miljön inne i dessa celler.
Testa säkerhet, precision och effekt i celler
I cellkulturer visade nanoagenten sig vara skonsam mot friska celler och gav liten toxicitet eller membranskada. När den utsattes för skumceller togs partiklarna däremot upp långt mer effektivt än enklare varianter som saknade membranklädseln eller målinriktande peptiden. Väl inne i dessa sjuka celler utlöstes nedbrytning av polymerskalet av den oxidativa miljön och atorvastatin frisattes. Detta minskade skadliga nivåer av reaktiva syreföreningar, dämpade upptaget av fetthaltiga partiklar och ökade utsöndringen av kolesterol genom att slå på kroppens egna transportproteiner. Samtidigt sänkte behandlingen nivåerna av CD47, ett ytmolekyl som normalt signalerar till immunceller ”rör mig inte”, vilket gjorde skumcellerna lättare för makrofager att avlägsna.
Avslöja och reparera plack i levande djur
I möss som genetiskt är benägna att utveckla åderförkalkning och som fick en fettrik kost cirkulerade nanoagenten i blodomloppet i timmar och ackumulerades starkt i artärplack. Teamet visade att infraröda, fotoakustiska och MRI‑signaler alla ökade parallellt i plackrika regioner och stämde väl överens med vävnadsmätningar av plackstorlek, inflammation och skörhet. Mer avancerade, instabila plack gav starkare signaler än mildare sådana, vilket tyder på att plattformen kan gradera sjukdomens svårighetsgrad. När den användes upprepade gånger som behandling minskade den riktade nanoagenten den totala plackbördan betydligt mer än fri atorvastatin eller mindre sofistikerade nanopartikelvarianter. Den reducerade oxidativ stress, sänkte nivåer av inflammatoriska budbärare och försköt immuncellspopulationerna mot en lugnare, mer skyddande balans.
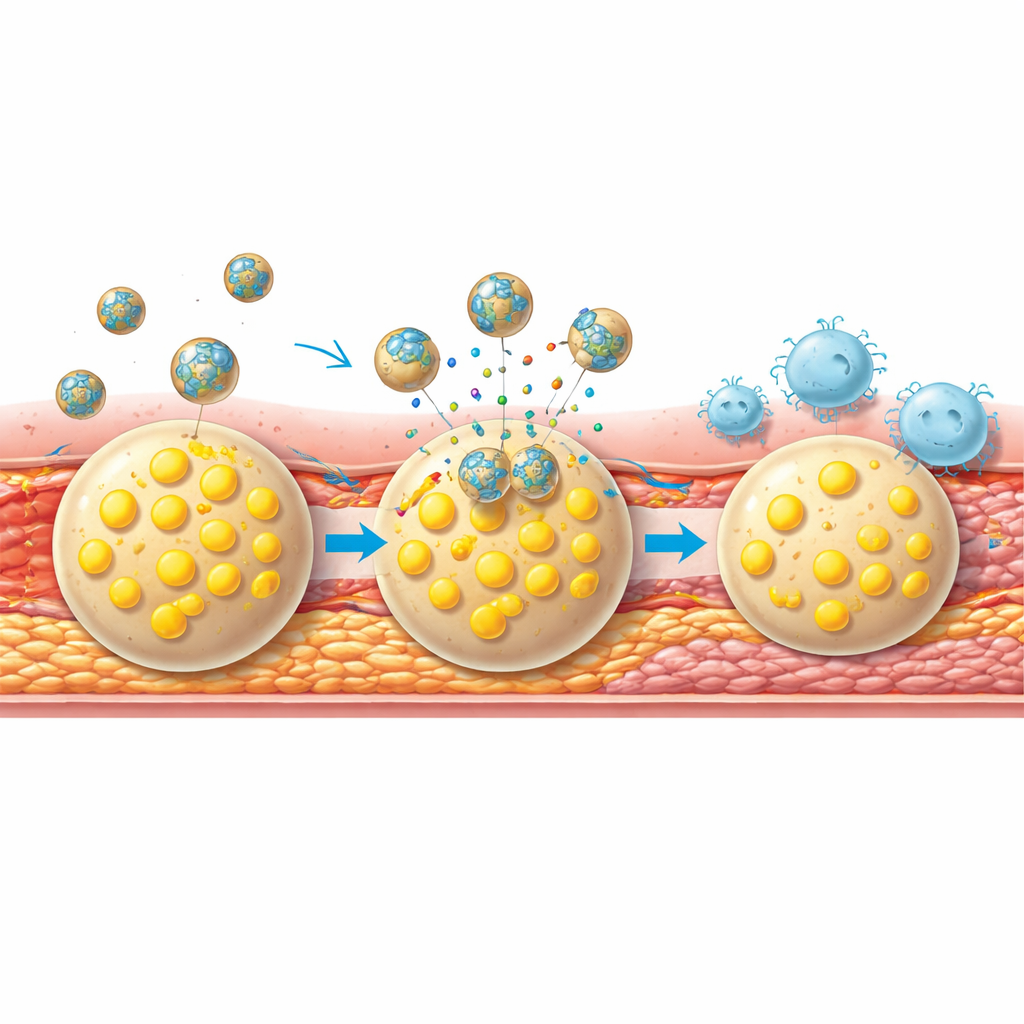
Göra plack tåligare och följa framsteg
Utöver att krympa plack gjorde terapin dem svårare att brista. Behandlade möss visade lägre nivåer av ett enzym som eroderar det fibrösa locket över placket, mer kollagen och fler glatta muskelceller som stärker detta lock, samt färre sköra nybildade blodkärl som kan läcka och destabilisera lesionen. Viktigt är att samma nanopartiklar som användes för behandling också fungerade som realtidsindikatorer på framgång: efter veckors terapi visade upprepade avbildningssessioner mycket svagare multimodala signaler i halsartärerna, vilket speglade den friskare plackstrukturen som sågs i mikroskopet.
Vad detta kan betyda för patienter
För en lekman pekar detta arbete mot framtida ”smarta kontrastmedel” som gör mycket mer än att bara hjälpa radiologer att se förträngningar. Denna flerlager‑nanoagent hittar de farligaste, inflammerade placken, levererar läkemedel exakt där det behövs, hjälper kroppen att rensa bort skadliga skumceller och rapporterar sedan tillbaka om hur väl behandlingen fungerar — utan operation. Medan dessa resultat är i möss och övergången till människa kräver noggranna prövningar, beskriver studien en kraftfull strategi för att förvandla tysta, instabila artärplack till bättre uppförande, stadigare strukturer innan de orsakar hjärtinfarkt eller stroke.
Citering: Song, J., Kang, X., Yang, S. et al. A hierarchical theranostic nanoagent for multimodal imaging and targeted foam cell intervention in atherosclerosis. Nat Commun 17, 3794 (2026). https://doi.org/10.1038/s41467-026-70463-7
Nyckelord: åderförkalkning, nanopartiklar, multimodal avbildning, skumceller, plackstabilisering