Clear Sky Science · it
Un nanoagente teranostico gerarchico per imaging multimodale e intervento mirato sulle cellule schiumose nell’aterosclerosi
Perché le arterie intasate sono importanti
L’aterosclerosi — il progressivo intasamento e indebolimento delle nostre arterie — è il motore nascosto dietro infarti e ictus. Nel profondo delle pareti arteriose, le cellule immunitarie si gonfiano di grasso e si trasformano nelle cosiddette cellule schiumose, che favoriscono la crescita delle placche e ne aumentano la fragilità. I medici riescono a vedere le grandi placche in fase tardiva con gli scanner attuali, ma faticano a individuare e trattare precocemente le placche pericolose, quando l’intervento potrebbe prevenire la catastrofe. Questo studio presenta una nanoparticella intelligente e stratificata che può sia mettere in luce queste aree a rischio con più tecniche di imaging sia calmarle e ripararle direttamente nelle arterie malate di topi.
Vedere i problemi nelle arterie da più angolazioni
Gli autori hanno prima progettato una molecola colorante speciale che funge da segnale “tre in uno”. Essa emette luce nel vicino infrarosso profondo, genera segnali ultrasonici quando pulsata con un laser (imaging fotoacustico) e potenzia la risonanza magnetica (MRI). Ognuno di questi metodi osserva il corpo in modo diverso: la fluorescenza infrarossa è molto sensibile e rapida, la fotoacustica fornisce dettagli strutturali nitidi a pochi centimetri di profondità, e la MRI mappa l’anatomia in tutto il corpo senza radiazioni. Regolando con cura la struttura del colorante e collegando un’unità di gadolinio usata per la MRI, il team ha creato una singola molecola che dà segnali forti in tutti e tre i sistemi, rimanendo stabile anche in condizioni biologiche aggressive.
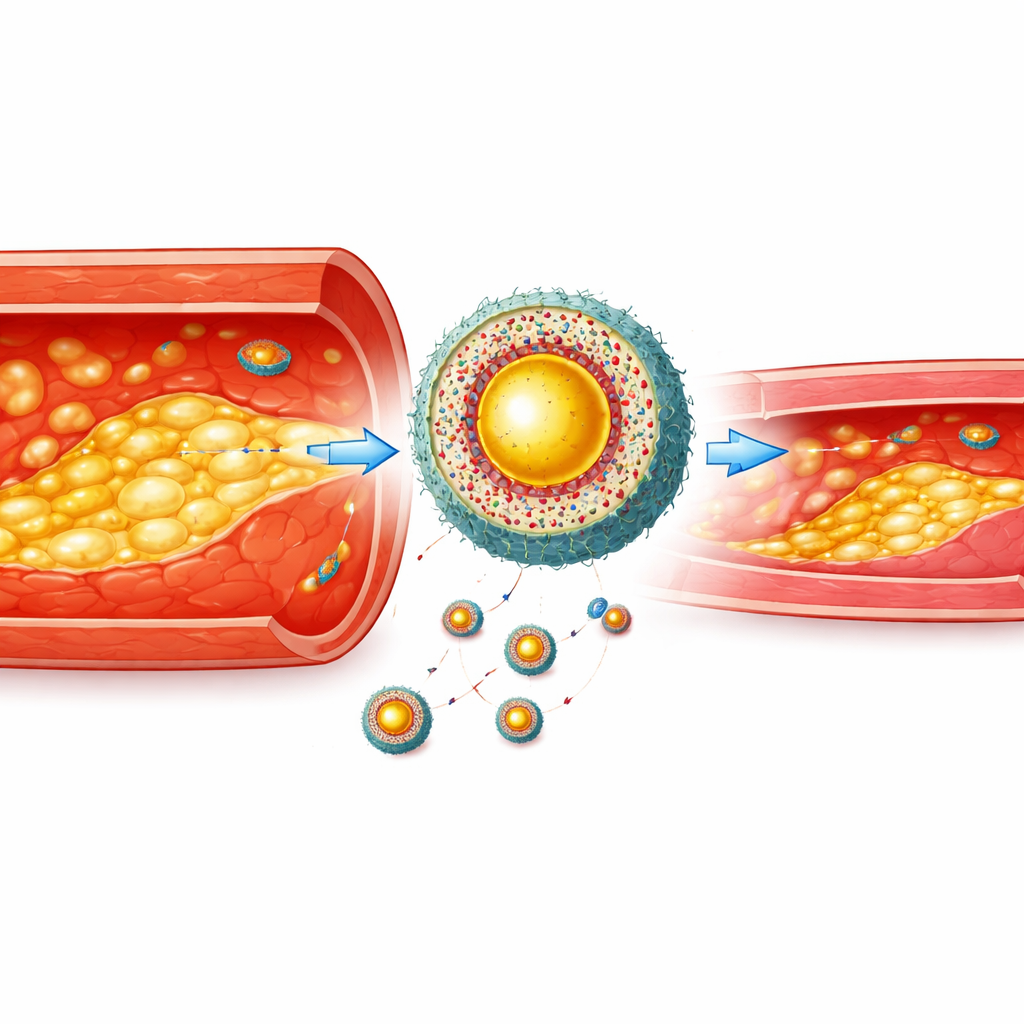
Costruire una capsula “homing” per le cellule malate
Da sola, una sonda di imaging brillante non basta: deve raggiungere il posto giusto e lì rimanere. Gli scienziati hanno incapsulato il colorante multimodale e il farmaco ipocolesterolemizzante atorvastatina all’interno di un rivestimento polimerico che si disintegra in presenza di alti livelli di specie reattive dell’ossigeno, un marcatore chimico delle cellule schiumose infiammate. Per aiutare le particelle a attraversare le pareti vascolari infiammate e indirizzarsi verso le cellule schiumose, hanno ricoperto le particelle con membrane di macrofagi reali (cellule immunitarie) e aggiunto un breve peptide che si lega a un segnale “mangiami” esposto sulla superficie delle cellule schiumose. Ne è nato un nanoagente gerarchico: prima attratto dalle pareti arteriose infiammate, poi più precisamente verso le cellule schiumose sepolte nella placca, e infine attivato dall’ambiente chimico stressato all’interno di quelle cellule.
Testare sicurezza, precisione e impatto nelle cellule
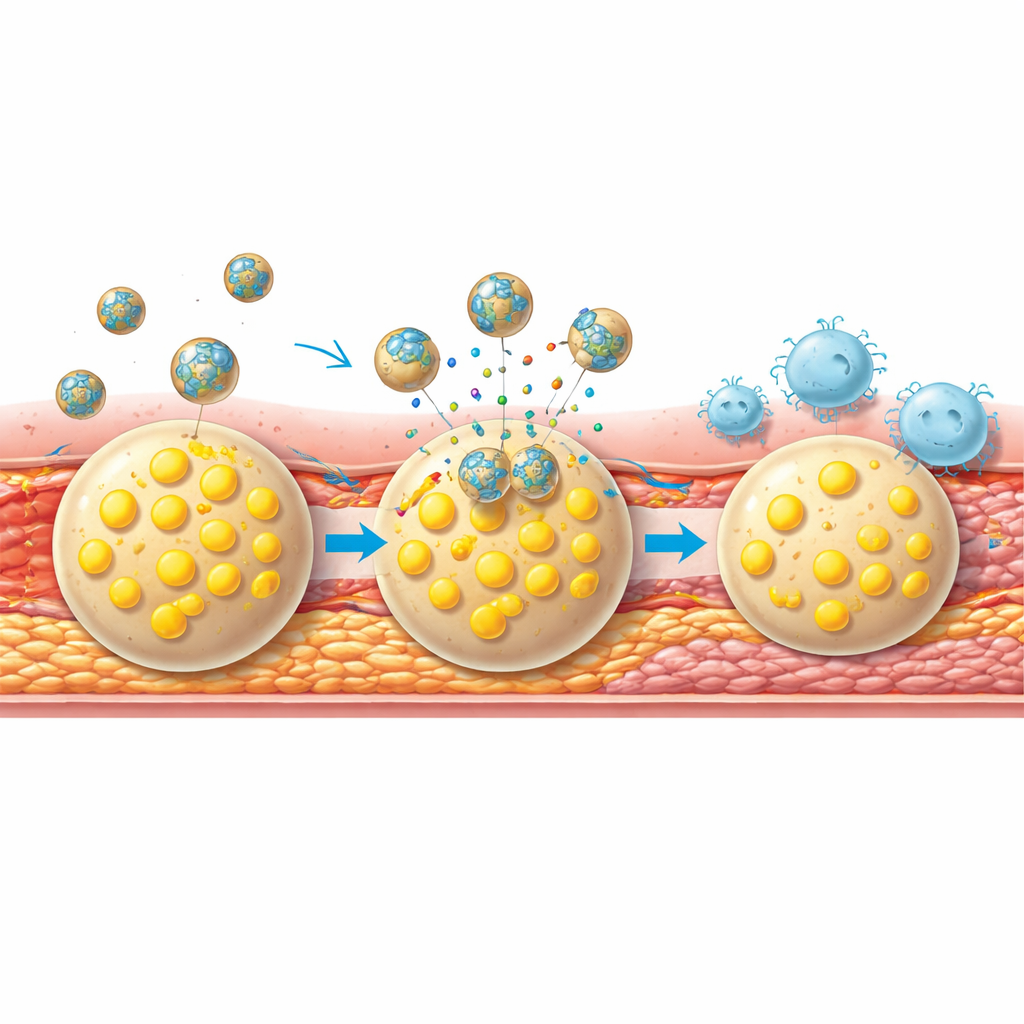
In colture cellulari, il nanoagente si è dimostrato gentile con le cellule sane, mostrando scarsa tossicità o danni alla membrana. Esponendo le cellule schiumose, però, le particelle sono state assorbite molto più efficacemente rispetto a versioni più semplici prive del mantello di membrana o del peptide bersaglio. Una volta all’interno di queste cellule malate, l’ambiente ossidativo ha innescato la degradazione del rivestimento polimerico e il rilascio dell’atorvastatina. Ciò ha ridotto i livelli dannosi di specie reattive dell’ossigeno, limitato l’assorbimento di particelle lipidiche e aumentato l’esportazione del colesterolo attivando i trasportatori naturali. Allo stesso tempo, il trattamento ha abbassato i livelli di CD47, una molecola di superficie che normalmente segnala ai fagociti “non mangiarmi”, rendendo le cellule schiumose più facili da rimuovere per i macrofagi.
Rivelare e riparare le placche negli animali viventi
In topi geneticamente predisposti all’aterosclerosi e alimentati con una dieta ricca di grassi, il nanoagente è rimasto in circolo nel flusso sanguigno per ore e si è accumulato in modo consistente nelle placche arteriose. Il team ha dimostrato che i segnali infrarossi, fotoacustici e di MRI aumentavano insieme nelle regioni ricche di placca e corrispondevano strettamente alle misure tissutali di dimensione della placca, infiammazione e fragilità. Le placche più avanzate e instabili producevano segnali più intensi rispetto a quelle più lievi, suggerendo che la piattaforma può classificare la gravità della malattia. Usato ripetutamente come terapia, il nanoagente mirato ha ridotto il carico di placca complessivo molto più della sola atorvastatina libera o di versioni nanoparticellari meno sofisticate. Ha diminuito lo stress ossidativo, abbassato i livelli di mediatori infiammatori e spostato le popolazioni di cellule immunitarie verso un equilibrio più calmo e protettivo.
Rendere le placche più resistenti e monitorare i progressi
Oltre a ridurre le dimensioni delle placche, la terapia le ha rese meno soggette a rottura. I topi trattati mostravano minori quantità di un enzima che erode il cappuccio fibroso delle placche, più collagene e più cellule muscolari lisce che rinforzano questo cappuccio, e meno neovasi fragili che possono perdere e destabilizzare la lesione. È importante che le stesse nanoparticelle usate per il trattamento siano servite anche da sensori in tempo reale del successo: dopo settimane di terapia, sessioni di imaging ripetute hanno mostrato segnali multimodali molto più deboli nelle arterie carotidi, rispecchiando la struttura della placca più sana osservata al microscopio.
Cosa potrebbe significare per i pazienti
Per un non esperto, questo lavoro indica la strada verso futuri “agenti di contrasto intelligenti” che fanno molto più che aiutare i radiologi a vedere le ostruzioni. Questo nanoagente stratificato individua le placche più pericolose e infiammate, rilascia il farmaco precisamente dove è necessario, aiuta l’organismo a rimuovere le cellule schiumose dannose e poi riferisce l’efficacia del trattamento — tutto senza intervento chirurgico. Pur essendo risultati ottenuti nei topi e richiedendo valutazioni rigorose per la traduzione clinica nell’uomo, lo studio delinea una strategia potente per trasformare placche arteriose silenti e instabili in strutture più controllate e robuste prima che causino infarti o ictus.
Citazione: Song, J., Kang, X., Yang, S. et al. A hierarchical theranostic nanoagent for multimodal imaging and targeted foam cell intervention in atherosclerosis. Nat Commun 17, 3794 (2026). https://doi.org/10.1038/s41467-026-70463-7
Parole chiave: aterosclerosi, nanoparticelle, imaging multimodale, cellule schiumose, stabilizzazione della placca