Clear Sky Science · de
Ein hierarchischer theranostischer Nanoagent für multimodale Bildgebung und gezielte Intervention an Schaumzellen bei Atherosklerose
Warum verstopfte Arterien wichtig sind
Atherosklerose – das schrittweise Verstopfen und Schwächen unserer Arterien – ist der verborgene Motor hinter Herzinfarkten und Schlaganfällen. Tief in den Gefäßwänden schwellen Immunzellen durch Fett an und verwandeln sich in sogenannte Schaumzellen, die das Plaquewachstum fördern und die Läsionen brüchig machen. Klinische Bildgebung erkennt bereits große, spätstadiale Plaques, hat aber Schwierigkeiten, gefährliche Herde frühzeitig zu identifizieren und zu behandeln, wenn ein Eingreifen Katastrophen verhindern könnte. Diese Studie stellt einen intelligenten, geschichteten Nanopartikel vor, der solche Risikobereiche mit mehreren Bildgebungsverfahren sichtbar macht und zugleich direkt beruhigend und reparierend in erkrankten Arterien von Mäusen wirkt.
Probleme in Arterien aus mehreren Blickwinkeln sehen
Die Forscher entwickelten zunächst ein spezielles Farbmolekül, das wie ein Drei‑in‑Eins‑Signalgeber wirkt. Es leuchtet im tiefen nahen Infrarot, erzeugt bei Laseranregung Ultraschallsignale (photoakustische Bildgebung) und verbessert die Magnetresonanztomographie (MRT). Jedes dieser Verfahren bietet eine andere Sicht auf den Körper: das infrarote Leuchten ist sehr empfindlich und schnell, die Photoakustik liefert scharfe strukturelle Details einige Zentimeter tief, und die MRT bildet die Anatomie im ganzen Körper ohne Strahlenbelastung ab. Durch sorgfältiges Abstimmen der Struktur des Farbstoffs und das Anfügen einer für die MRT nutzbaren Gadolinium‑Einheit schufen die Autoren ein einzelnes Molekül, das in allen drei Systemen starke Signale liefert und selbst unter harschen biologischen Bedingungen stabil bleibt.
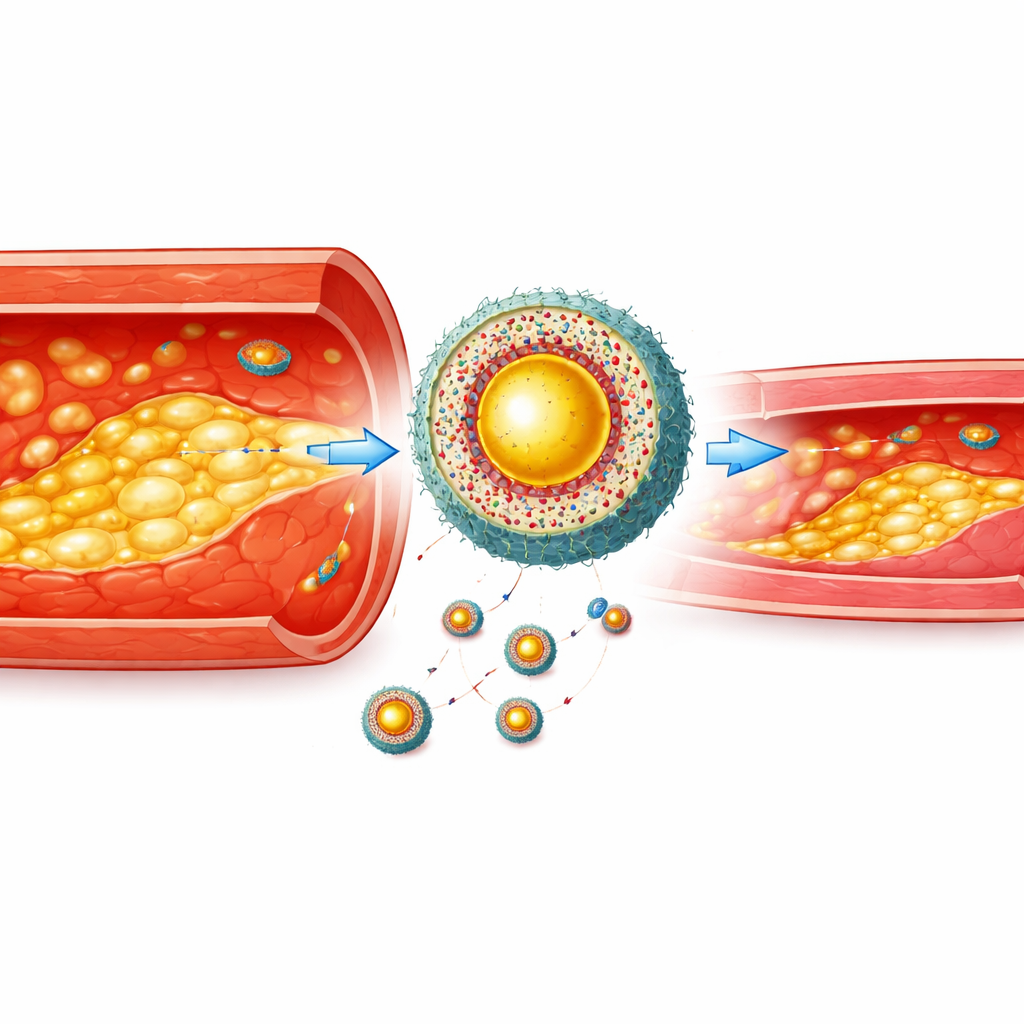
Eine Zielkapsel für erkrankte Zellen bauen
Ein helles Bildgebungssignal allein genügt nicht – es muss am richtigen Ort ankommen und dort verbleiben. Die Wissenschaftler kapselten den multimodalen Farbstoff und das cholesterinsenkende Medikament Atorvastatin in eine Polymerhülle, die sich in Gegenwart hoher Mengen reaktiver Sauerstoffspezies auflöst, einem chemischen Kennzeichen entzündeter Schaumzellen. Um den Partikeln das Durchdringen entzündeter Gefäßauskleidungen und das gezielte Ansteuern von Schaumzellen zu erleichtern, überzogen sie die Partikel mit echten Makrophagenmembranen und ergänzten einen kurzen Peptidanteil, der an ein auf Schaumzellen exponiertes "ess mich"‑Signal bindet. So entstand ein hierarchischer Nanoagent: zunächst angezogen von entzündeten Gefäßwänden, dann präziser zu in Plaques eingebetteten Schaumzellen und schließlich durch das gestresste chemische Milieu in diesen Zellen aktiviert.
Sicherheit, Präzision und Wirkung in Zellen testen
Im Zellkulturversuch erwies sich der Nanoagent als schonend gegenüber gesunden Zellen und verursachte kaum Toxizität oder Membranschäden. Bei Exposition gegenüber Schaumzellen jedoch wurden die Partikel deutlich effizienter aufgenommen als einfachere Varianten ohne Membranhülle oder Zielpeptid. Einmal in diesen kranken Zellen, löste das oxidative Milieu die Polymerhülle auf und setzte Atorvastatin frei. Dies reduzierte schädliche reaktive Sauerstofflevel, hemmte die Aufnahme fetthaltiger Partikel und förderte den Cholesterinaustransport durch Aktivierung natürlicher Transportproteine. Gleichzeitig senkte die Behandlung die Spiegel von CD47, einem Oberflächenmolekül, das normalerweise Immunzellen "friss mich nicht" signalisiert, wodurch die Schaumzellen für Makrophagen leichter zu beseitigen wurden.
Plaques in lebenden Tieren sichtbar machen und reparieren
In genetisch atheroskleroseanfälligen Mäusen, die mit fettreicher Kost gefüttert wurden, zirkulierte der Nanoagent mehrere Stunden im Blut und reicherte sich stark in arteriellen Plaques an. Das Team zeigte, dass Infrarot-, photoakustische und MRT‑Signale in plaquereichen Regionen gleichzeitig anstiegen und eng mit Gewebemaßen für Plaquegröße, Entzündung und Brüchigkeit übereinstimmten. Fortgeschrittene, instabile Plaques erzeugten stärkere Signale als mildere, was darauf hindeutet, dass die Plattform die Schwere der Erkrankung einstufen kann. Bei wiederholter Anwendung als Therapie verringerte der zielgerichtete Nanoagent die Gesamtplaquebelastung deutlich stärker als freies Atorvastatin oder weniger ausgeklügelte Nanopartikelvarianten. Er reduzierte oxidativen Stress, senkte Entzündungsbotenstoffe und verschob die Immunzellpopulationen hin zu einem ruhigeren, schützenden Gleichgewicht.
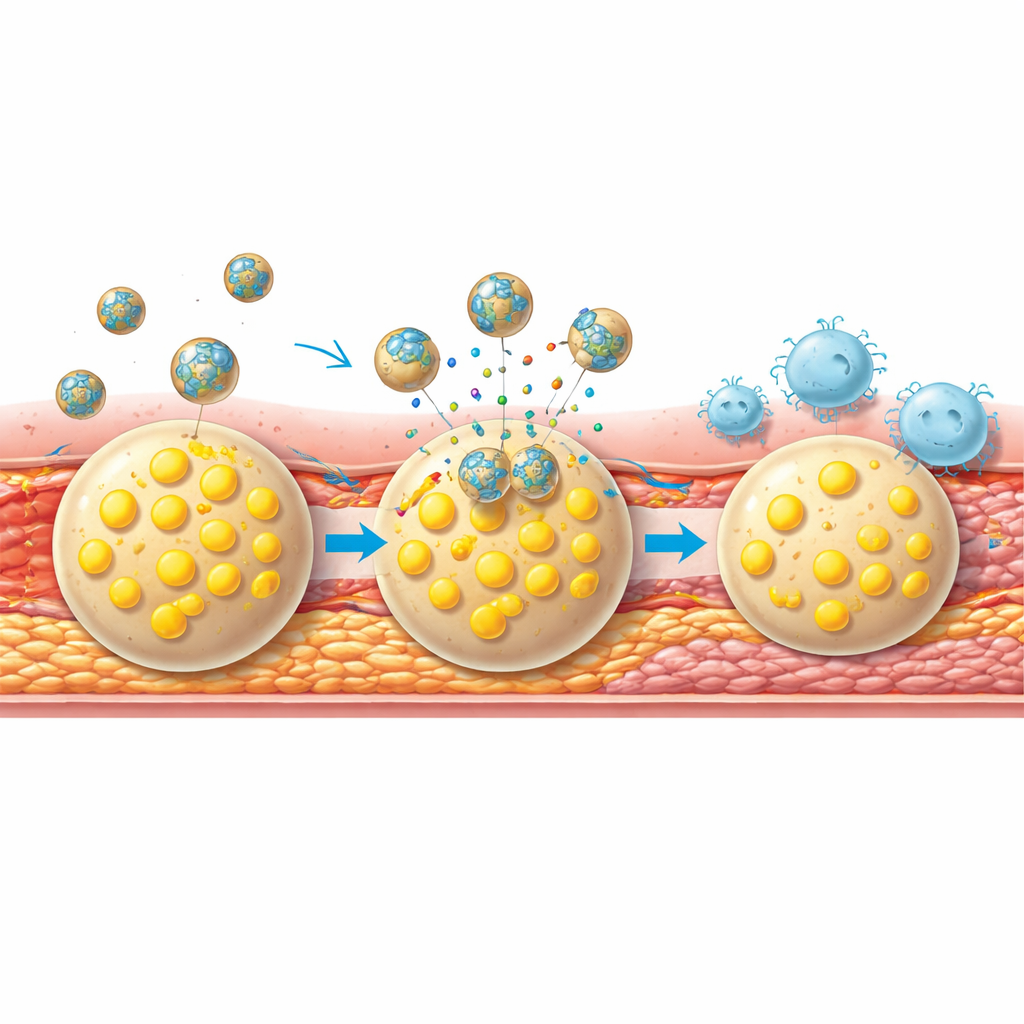
Plaques widerstandsfähiger machen und den Fortschritt verfolgen
Über das Verkleinern der Plaques hinaus machte die Therapie diese weniger rissanfällig. Behandelte Mäuse zeigten weniger eines Enzyms, das die fibröse Kappe über Plaques abbaut, mehr Kollagen und glatte Muskelzellen, die diese Kappe stärken, sowie weniger fragile Neubildungen von Blutgefäßen, die die Läsion destabilisieren können. Wichtig ist, dass dieselben für die Behandlung verwendeten Nanopartikel auch als Echtzeit‑Reporter des Therapieerfolgs dienten: Nach Wochen der Behandlung zeigten wiederholte Bildgebungssitzungen deutlich schwächere multimodale Signale in den Halsschlagadern, was der gesünderen Plaquestruktur entsprach, die unter dem Mikroskop zu sehen war.
Was das für Patienten bedeuten könnte
Für Laien deutet diese Arbeit auf künftige "intelligente Kontrastmittel" hin, die weit mehr leisten als Radiologen beim Erkennen von Gefäßverschlüssen zu unterstützen. Dieser geschichtete Nanoagent findet die gefährlichsten, entzündeten Plaques, liefert Medikamente präzise dorthin, wo sie gebraucht werden, hilft dem Körper schädliche Schaumzellen zu entfernen und berichtet anschließend über den Behandlungserfolg – und das alles ohne Operation. Obwohl diese Ergebnisse an Mäusen gewonnen wurden und die Übertragung auf den Menschen sorgfältige Tests erfordert, skizziert die Studie eine vielversprechende Strategie, stillen, instabilen Gefäßplaques das Potenzial zu nehmen, Herzinfarkte oder Schlaganfälle auszulösen, indem man sie vorher in gefügigere, stabilere Strukturen verwandelt.
Zitation: Song, J., Kang, X., Yang, S. et al. A hierarchical theranostic nanoagent for multimodal imaging and targeted foam cell intervention in atherosclerosis. Nat Commun 17, 3794 (2026). https://doi.org/10.1038/s41467-026-70463-7
Schlüsselwörter: Atherosklerose, Nanopartikel, multimodale Bildgebung, Schaumzellen, Plaquestabilisierung