Clear Sky Science · fr
Un nanoagent théranostique hiérarchique pour l’imagerie multimodale et l’intervention ciblée sur les cellules spumeuses dans l’athérosclérose
Pourquoi les artères bouchées comptent
L’athérosclérose — l’obstruction et l’affaiblissement progressifs de nos artères — est le moteur caché des infarctus et des AVC. Au cœur de la paroi artérielle, des cellules immunitaires s’enrichissent en lipides et se transforment en cellules dites spumeuses, qui favorisent la croissance des plaques et les rendent fragiles. Les scanners actuels détectent les plaques volumineuses et tardives, mais peinent à repérer et traiter les plaques dangereuses au stade précoce, quand une intervention pourrait prévenir la catastrophe. Cette étude présente une nanoparticule intelligente et stratifiée capable à la fois d’éclairer ces zones à risque par plusieurs techniques d’imagerie et de les calmer et réparer directement dans les artères malades de souris.
Voir les problèmes artériels sous plusieurs angles
Les chercheurs ont d’abord conçu une molécule de colorant spéciale qui fonctionne comme un signal trois en un. Elle fluoresce dans le proche infrarouge profond, génère des signaux ultrasonores lorsqu’on l’excite par laser (imagerie photoacoustique) et améliore l’imagerie par résonance magnétique (IRM). Chacune de ces méthodes observe le corps différemment : la fluorescence infrarouge est très sensible et rapide, la photoacoustique apporte des détails structuraux précis sur quelques centimètres de profondeur, et l’IRM cartographie l’anatomie de tout le corps sans rayonnement. En ajustant finement la structure du colorant et en greffant une unité de gadolinium utilisée en IRM, l’équipe a créé une seule molécule fournissant des signaux puissants dans les trois modalités, restée stable même en conditions biologiques exigeantes.
Construire une capsule ciblée pour les cellules malades
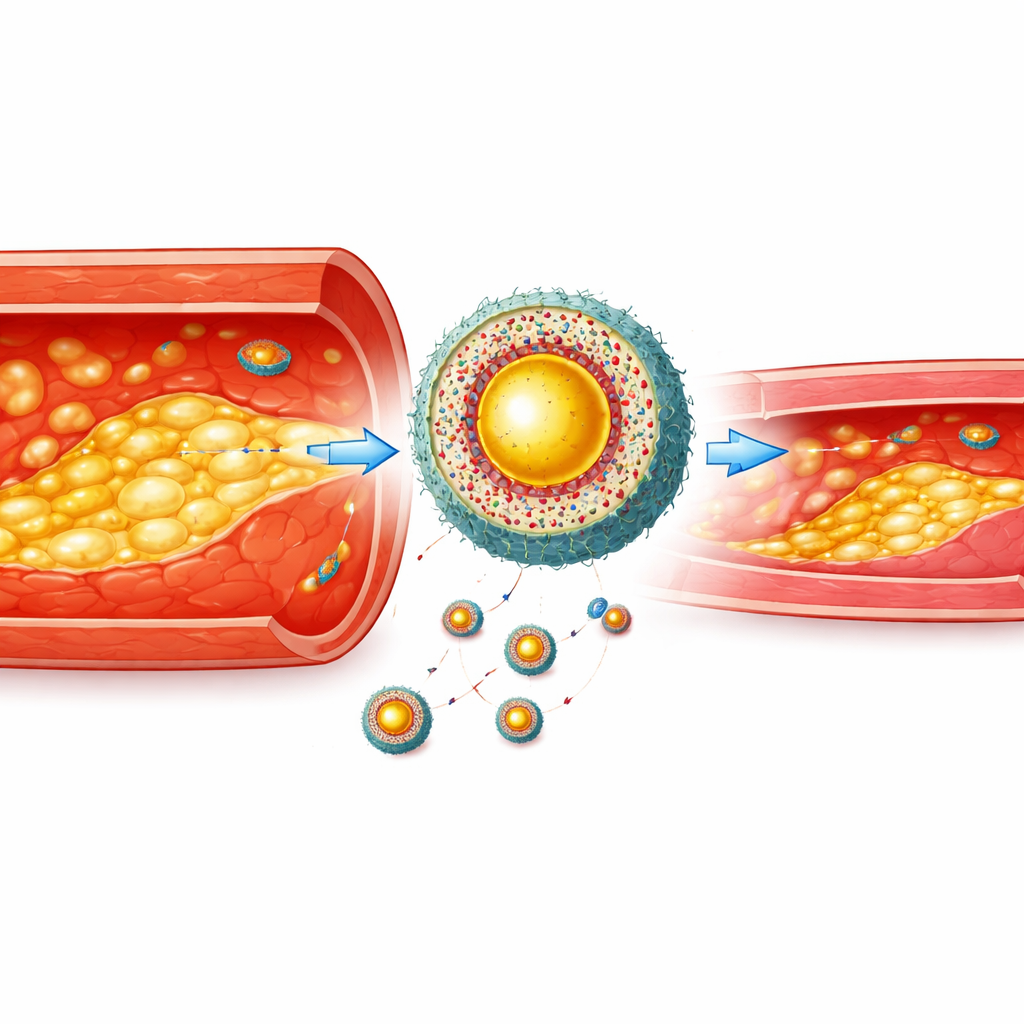
Un signal d’imagerie brillant ne suffit pas : il doit atteindre le bon endroit et y rester. Les scientifiques ont encapsulé le colorant multimodal et le médicament hypolipémiant atorvastatine dans une coque polymère qui se désagrège en présence de niveaux élevés d’espèces réactives de l’oxygène, signature chimique des cellules spumeuses enflammées. Pour aider les particules à traverser les parois vasculaires inflammées et à cibler les cellules spumeuses, ils ont enveloppé les particules dans des membranes de macrophages réels et ajouté un court peptide se liant à un signal « mange‑moi » exposé à la surface des cellules spumeuses. Cela a créé un nanoagent hiérarchique : d’abord attiré vers les parois artérielles enflammées, puis plus précisément vers les cellules spumeuses enfouies dans la plaque, et enfin activé par l’environnement chimique stressé à l’intérieur de ces cellules.
Tester la sécurité, la précision et l’effet sur des cellules
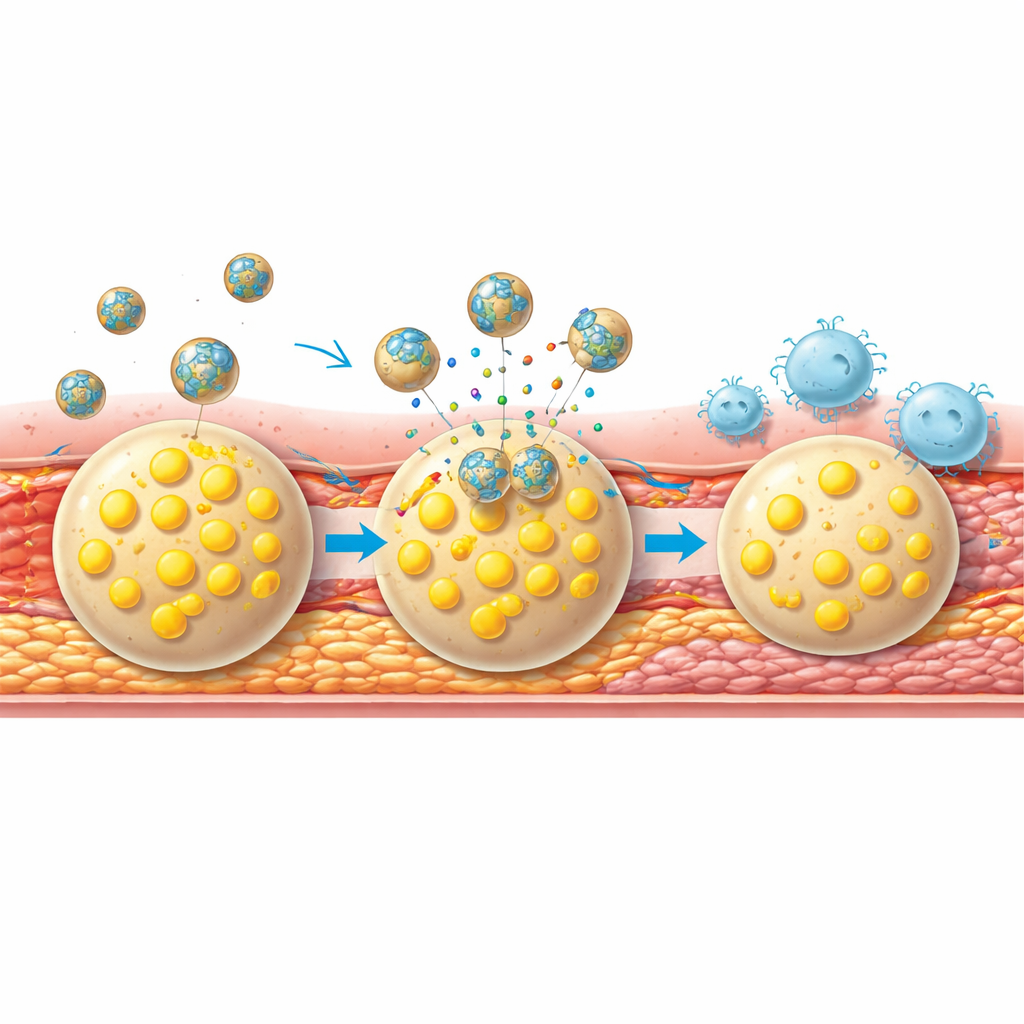
En culture cellulaire, le nanoagent s’est montré doux pour les cellules saines, avec peu de toxicité ou de dommages membranaires. Exposé aux cellules spumeuses, cependant, les particules ont été internalisées beaucoup plus efficacement que des versions plus simples dépourvues du manteau membranaire ou du peptide ciblant. Une fois à l’intérieur de ces cellules malades, l’environnement oxydatif a déclenché la dégradation de la coque polymère et la libération d’atorvastatine. Cela a réduit les niveaux nocifs d’espèces réactives, limité la captation de particules lipidiques et augmenté l’expulsion du cholestérol en activant les protéines de transport naturelles. Parallèlement, le traitement a abaissé les niveaux de CD47, une molécule de surface qui dit normalement aux cellules immunitaires « ne me mangez pas », rendant ainsi les cellules spumeuses plus facilement éliminables par les macrophages.
Détecter et réparer les plaques chez l’animal vivant
Chez des souris génétiquement prédisposées à l’athérosclérose et nourries avec un régime riche en graisses, le nanoagent a circulé dans le sang pendant des heures et s’est accumulé fortement dans les plaques artérielles. L’équipe a montré que les signaux infrarouge, photoacoustique et IRM augmentaient simultanément dans les régions riches en plaque et correspondaient étroitement aux mesures tissulaires de taille de plaque, d’inflammation et de fragilité. Les plaques plus avancées et instables généraient des signaux plus forts que les formes moins sévères, suggérant que la plateforme peut grader la sévérité de la maladie. Lorsqu’utilisé de manière répétée comme traitement, le nanoagent ciblé a réduit la charge totale en plaque bien plus que l’atorvastatine libre ou des nanoparticules moins sophistiquées. Il a diminué le stress oxydatif, abaissé les niveaux de médiateurs inflammatoires et fait évoluer les populations cellulaires immunitaires vers un équilibre plus calme et protecteur.
Rendre les plaques plus solides et suivre la progression
Au‑delà de la simple réduction des plaques, la thérapie les a rendues moins susceptibles de se rompre. Les souris traitées présentaient moins d’une enzyme qui érode le chapeau fibreux des plaques, plus de collagène et de cellules musculaires lisses renforçant ce chapeau, et moins de néovaisseaux fragiles susceptibles de fuir et de déstabiliser la lésion. Fait important, les mêmes nanoparticules utilisées pour le traitement ont aussi servi de capteurs en temps réel du succès : après des semaines de thérapie, des sessions d’imagerie répétées ont montré des signaux multimodaux nettement plus faibles dans les artères carotides, reflétant la structure de plaque plus saine observée au microscope.
Ce que cela pourrait signifier pour les patients
Pour un non‑spécialiste, ce travail ouvre la voie à de futurs « agents de contraste intelligents » qui font bien plus qu’aider les radiologues à voir des obstructions. Ce nanoagent stratifié repère les plaques les plus dangereuses et inflammées, délivre le médicament précisément là où il est nécessaire, aide l’organisme à éliminer les cellules spumeuses nocives, puis rend compte de l’efficacité du traitement — le tout sans chirurgie. Si ces résultats ont été obtenus chez la souris et que la traduction chez l’humain nécessitera des tests rigoureux, l’étude décrit une stratégie puissante pour transformer des plaques artérielles silencieuses et instables en structures mieux comportées et plus robustes avant qu’elles ne provoquent infarctus ou AVC.
Citation: Song, J., Kang, X., Yang, S. et al. A hierarchical theranostic nanoagent for multimodal imaging and targeted foam cell intervention in atherosclerosis. Nat Commun 17, 3794 (2026). https://doi.org/10.1038/s41467-026-70463-7
Mots-clés: athérosclérose, nanoparticules, imagerie multimodale, cellules spumeuses, stabilisation de la plaque