Clear Sky Science · ar
عامل نانوي ثيرانوستيكي هرمي للتصوير متعدد الوسائط والتدخل المستهدف في خلايا الرغوة في تصلب الشرايين
لماذا تهم الشرايين المسدودة
تصلب الشرايين — الانسداد والضعف التدريجي في شراييننا — هو المحرك الخفي وراء النوبات القلبية والسكتات الدماغية. في أعماق جدران الشرايين، تنتفخ الخلايا المناعية بالدهون وتتحول إلى ما يُسمى خلايا الرغوة، التي تُسهم في نمو اللويحات وجعلها هشة. يمكن للأطباء رؤية اللويحات الكبيرة والمتأخرة بالمرحلة الحالية من أجهزة المسح، لكنهم يواجهون صعوبة في اكتشاف ومعالجة اللويحات الخطرة مبكراً، عندما قد تمنع التدخلات الكارثة. تقدّم هذه الدراسة جسيمًا نانويًا ذكيًا متعدد الطبقات يمكنه أن يضيء هذه المناطق عالية الخطر بأساليب تصوير متعددة وأن يهدّئها ويُصلحها مباشرة في شرايين الفئران المصابة.
رؤية المشاكل في الشرايين من زوايا متعددة
صمم الباحثون أولاً جزيء صبغة خاص يعمل كمنارة ثلاثية الوظائف. يتوهج في نطاق الأشعة تحت الحمراء القريبة العميقة، ويولّد إشارات صوتية عند نبضه بليزر (التصوير الضوئي الصوتي)، ويُعزِّز التصوير بالرنين المغناطيسي (MRI). كل واحدة من هذه الطرق تُظهر الجسم بطريقة مختلفة: التوهج تحت الحمراء حساس وسريع جداً، والتصوير الضوئي الصوتي يوفر تفاصيل هيكلية حادة على عمق بضعة سنتيمترات، وMRI يرسم تشريح الجسم بأكمله دون إشعاع. من خلال ضبط بنية الصبغة بعناية وربط وحدة غادولينيووم المستخدمة في الMRI، أنشأ الفريق جزيئًا واحدًا يعطي إشارات قوية في الأنظمة الثلاثة، ويظل مستقرًا حتى في الظروف البيولوجية القاسية.
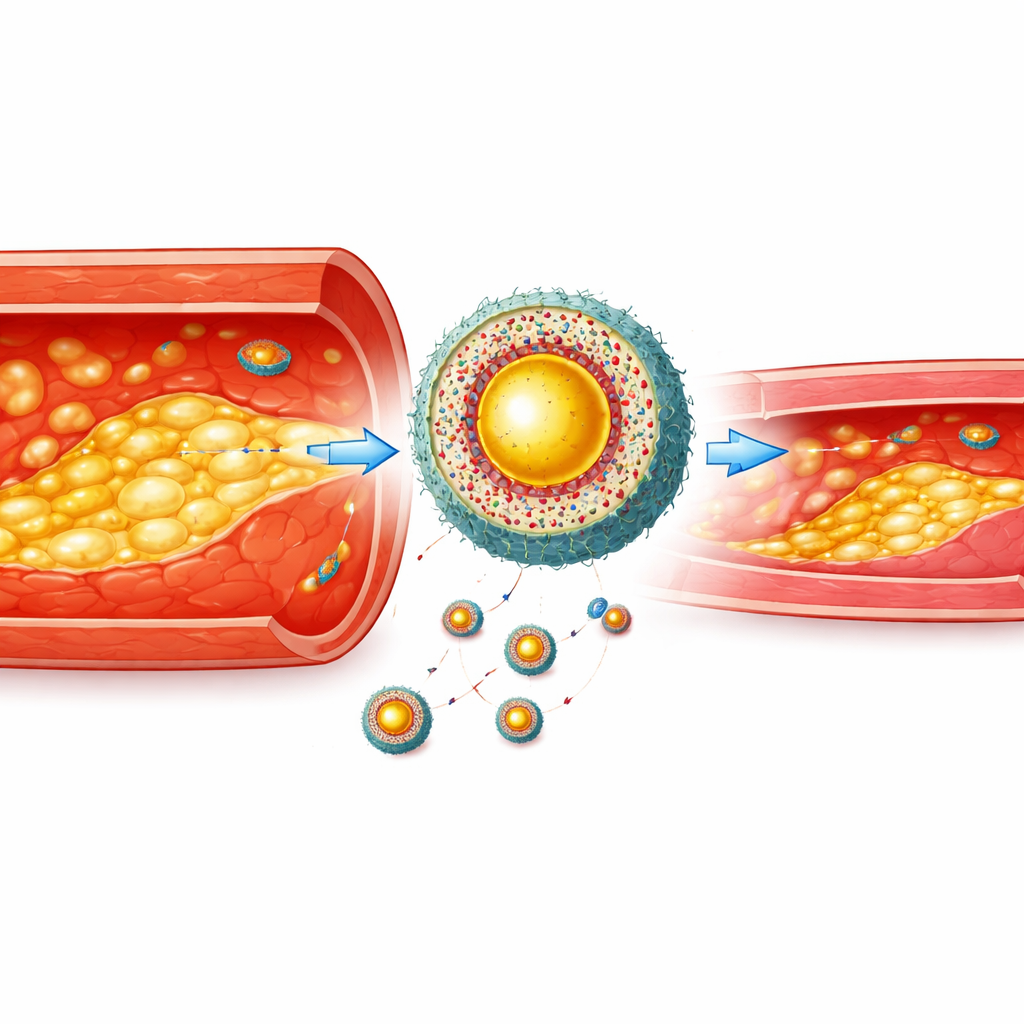
بناء كبسولة موجهة نحو الخلايا المريضة
لوحدها، فإن منارة تصوير ساطعة لا تكفي — يجب أن تصل إلى المكان الصحيح وتبقى هناك. قام العلماء بتضمين الصبغة متعددة الوسائط والدواء المخفض للكوليسترول أتورفاستاتين داخل غلاف بوليمري يتحلل بوجود مستويات عالية من أنواع الأكسجين التفاعلية، وهي سمة كيميائية مميزة لخلايا الرغوة الملتهبة. لمساعدة الجسيمات على التسلل عبر بطانات الأوعية الملتهبة والتوجه نحو خلايا الرغوة، غلفوها بأغشية من بلاعم حقيقية (خلايا مناعية) وأضافوا ببتيدًا قصيرًا يرتبط بإشارة "كُلني" التي تظهر على سطح خلايا الرغوة. هذا خلق عاملًا نانويًا هرميًا: يُجذب أولاً إلى جدران الشرايين الملتهبة، ثم بشكل أدق إلى خلايا الرغوة المدفونة في اللويحة، وأخيرًا يُفعّل بواسطة البيئة الكيميائية المجهدة داخل تلك الخلايا.
اختبار السلامة والدقة والتأثير في الخلايا
في مزروعات الخلايا، برهن العامل النانوي أنه لطيف على الخلايا السليمة، حيث أظهر سمية ضئيلة أو أذى لغشاء الخلية. عندما تعرّض لخلايا الرغوة، تم امتصاص الجسيمات بكفاءة أكبر بكثير من النسخ الأبسط التي تفتقر إلى غطاء الغشاء أو الببتيد المستهدف. وحالما دخلت هذه الخلايا المريضة، حفّزت البيئة التأكسدية تفتت الغلاف البوليمري وإطلاق الأتورفاستاتين. أدى ذلك إلى خفض مستويات أنواع الأكسجين التفاعلية الضارة، وكبح امتصاص الجسيمات الدهنية، وتعزيز تصدير الكوليسترول عبر تشغيل بروتينات النقل الطبيعية. وفي الوقت نفسه، خفّض العلاج مستويات CD47، وهو جزيء سطحي يخبر عادة الخلايا المناعية "لا تأكلني"، مما جعل خلايا الرغوة أسهل على البلاعم لإزالتها.
كشف وإصلاح اللويحات في حيوانات حية
في فئران معرضة وراثيًا لتصلب الشرايين وتغذت على نظام عالي الدهون، دار العامل النانوي في مجرى الدم لساعات وتراكم بشدة في لويحات الشرايين. أظهر الفريق أن إشارات الأشعة تحت الحمراء والضوئية الصوتية والMRI ارتفعت معًا في المناطق الغنية باللويحات وتطابقت بشكل وثيق مع مقاييس النسيج لحجم اللويحة والالتهاب والهشاشة. أنتجت اللويحات المتقدمة وغير المستقرة إشارات أقوى من اللويحات الأخف، ما يوحي بأن المنصة قادرة على تصنيف شدة المرض. عندما استُخدمت مرارًا وتكرارًا كعلاج، قلّص العامل النانوي المستهدف عبء اللويحات العام أكثر بكثير من الأتورفاستاتين الحر أو نسخ الجسيمات النانوية الأقل تطورًا. وخفّض الإجهاد التأكسدي، ودنى مستويات المرسلات الالتهابية، وحوّل توازن الخلايا المناعية نحو حالة أكثر هدوءًا وحماية.
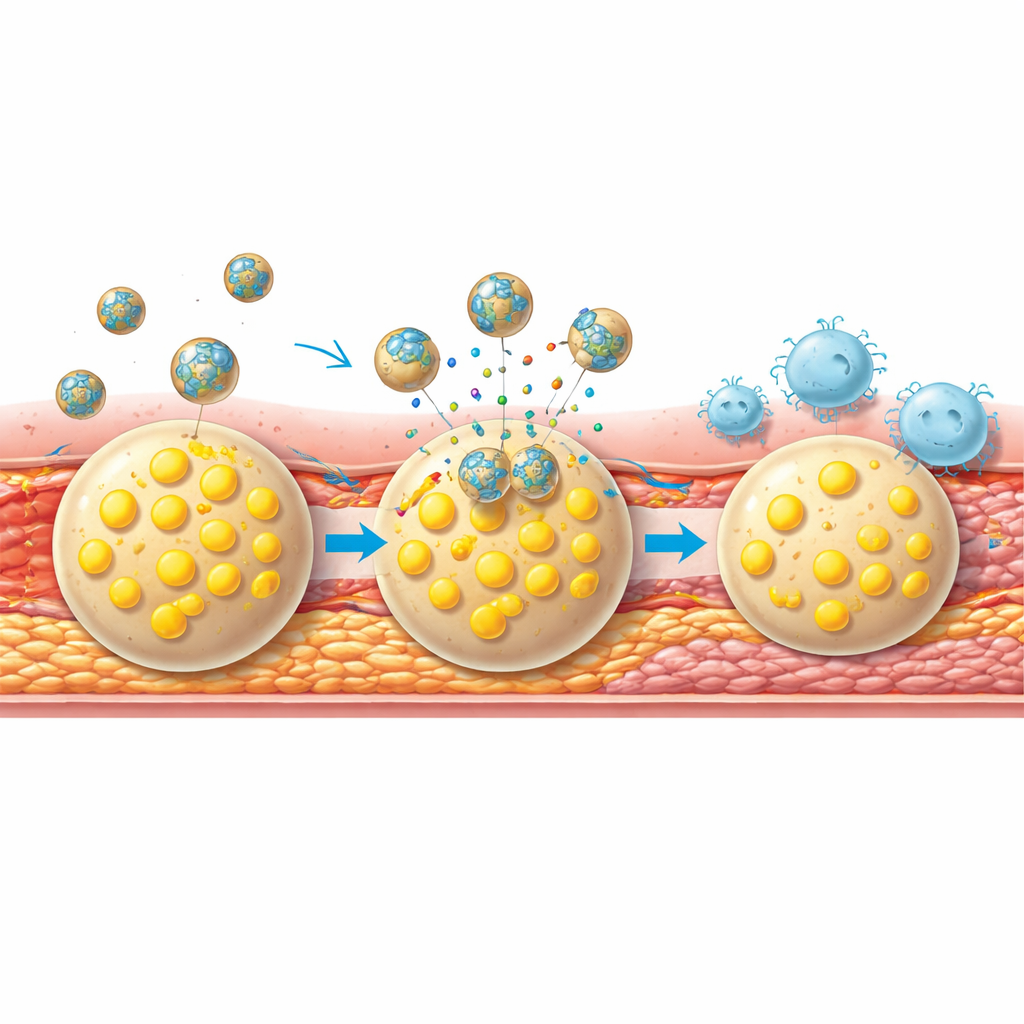
تقوية اللويحات وتتبع التقدم
بجانب تقليص اللويحات، جعل العلاج هذه اللويحات أصعب على التمزق. أظهرت الفئران المعالجة مستويات أقل من إنزيم يآكل الغطاء الليفي فوق اللويحات، ومزيدًا من الكولاجين وخلايا العضلات الملساء التي تقوّي هذا الغطاء، وعددًا أقل من الأوعية الدموية الجديدة الهشة التي قد تتسرب وتزعزع استقرار الآفة. والأهم من ذلك، أن نفس الجسيمات النانوية المستخدمة للعلاج عملت أيضًا كمراصد في الوقت الحقيقي للنجاح: بعد أسابيع من العلاج، أظهرت جلسات التصوير المتكررة إشارات متعددة الوسائط أضعف بكثير في الشرايين السباتية، بما يعكس بنية لويحة أكثر صحة تحت المجهر.
ماذا قد يعني هذا للمرضى
لغير المتخصص، يشير هذا العمل نحو "عوامل تباين ذكية" مستقبلية تفعل أكثر بكثير من مجرد مساعدة أطباء الأشعة على رؤية الانسدادات. يجد هذا العامل النانوي متعدد الطبقات اللويحات الأخطر والأكثر التهابًا، ويوصل الدواء بدقة إلى حيث يلزم، ويساعد الجسم على إزالة خلايا الرغوة الضارة، ثم يقدّم تقريرًا عن مدى نجاح العلاج — وكل ذلك دون جراحة. رغم أن هذه النتائج في فئران وأن الترجمة البشرية ستتطلب اختبارات دقيقة، فإن الدراسة تعرض استراتيجية قوية لتحويل لويحات الشرايين الصامتة وغير المستقرة إلى تراكيب أكثر التزامًا ومتانة قبل أن تتسبب في نوبات قلبية أو سكتات دماغية.
الاستشهاد: Song, J., Kang, X., Yang, S. et al. A hierarchical theranostic nanoagent for multimodal imaging and targeted foam cell intervention in atherosclerosis. Nat Commun 17, 3794 (2026). https://doi.org/10.1038/s41467-026-70463-7
الكلمات المفتاحية: تصلب الشرايين, جسيمات نانوية, التصوير متعدد الوسائط, خلايا الرغوة, استقرار اللويحة