Clear Sky Science · es
Un nanoagente terapéutico y diagnóstico jerárquico para imagen multimodal e intervención dirigida sobre células espumosas en la aterosclerosis
Por qué importan las arterias obstruidas
La aterosclerosis —la obstrucción y debilitamiento progresivo de nuestras arterias— es el motor oculto detrás de los infartos y los accidentes cerebrovasculares. En el interior de las paredes arteriales, las células inmunitarias se llenan de lípidos y se convierten en las llamadas células espumosas, que favorecen el crecimiento de placas y su fragilidad. Los médicos pueden detectar placas grandes y avanzadas con los escáneres actuales, pero les cuesta identificar y tratar las placas peligrosas en sus fases tempranas, cuando la intervención podría prevenir la catástrofe. Este estudio presenta una nanopartícula inteligente y por capas que puede, a la vez, iluminar estas áreas de riesgo con diversas técnicas de imagen y calmarlas y reparar directamente en arterias enfermas de ratones.
Ver el problema en las arterias desde varios ángulos
Los investigadores diseñaron primero una molécula colorante especial que actúa como una baliza tres en uno. Emite en una gama profunda del infrarrojo cercano, genera señales ultrasónicas cuando se ilumina con un láser (imagen fotoacústica) y mejora la resonancia magnética (RM). Cada uno de estos métodos ve el cuerpo de forma distinta: el brillo infrarrojo es muy sensible y rápido, la fotoacústica ofrece detalle estructural nítido a pocos centímetros de profundidad, y la RM cartografía la anatomía en todo el cuerpo sin radiación. Al afinar cuidadosamente la estructura del colorante y unirle una unidad de gadolinio usada en RM, el equipo creó una sola molécula que proporciona señales fuertes en los tres sistemas, manteniéndose estable incluso en condiciones biológicas adversas.
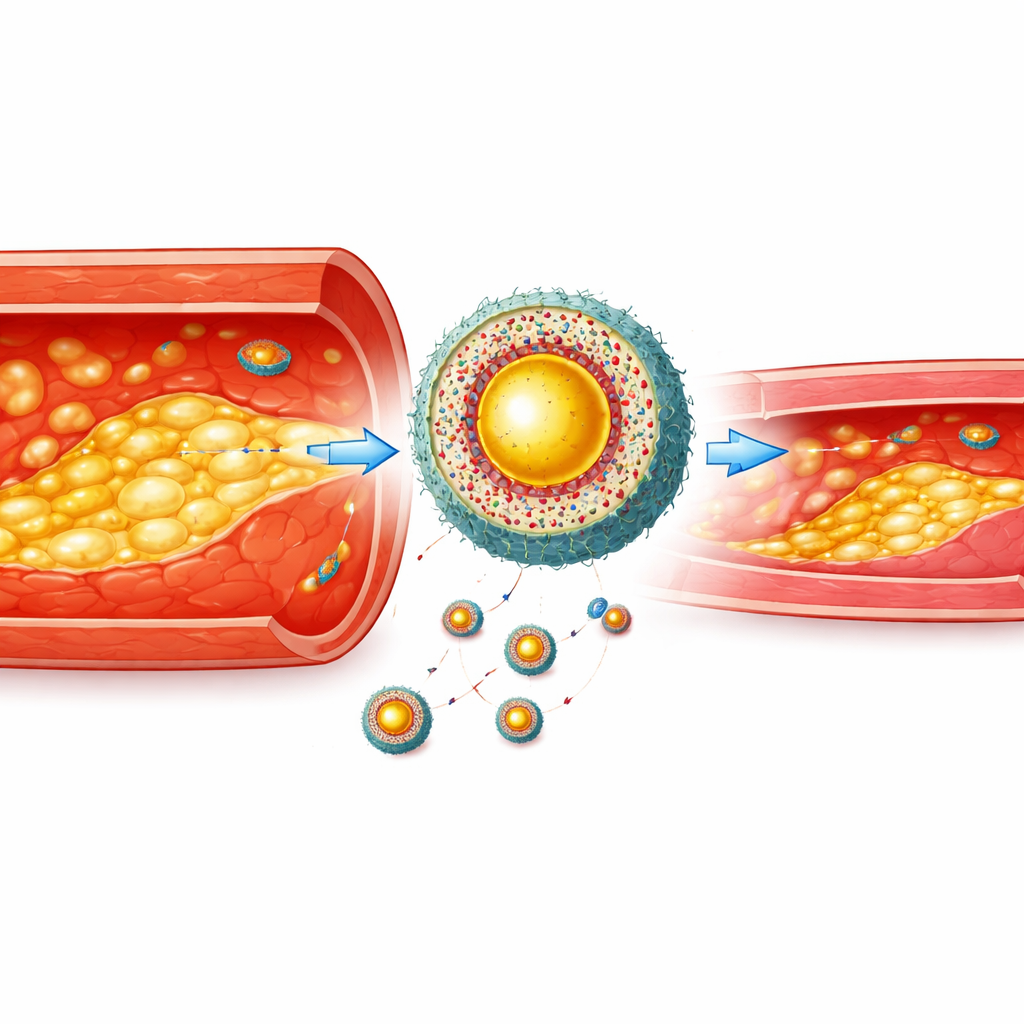
Construir una cápsula dirigida a células enfermas
Por sí sola, una baliza de imagen brillante no basta: debe llegar al lugar adecuado y permanecer allí. Los científicos encapsularon el tinte multimodal y la droga reductora de colesterol atorvastatina dentro de una carcasa polimérica que se desintegra en presencia de altos niveles de especies reactivas de oxígeno, un sello químico de las células espumosas inflamadas. Para ayudar a las partículas a atravesar los revestimientos vasculares inflamados y dirigirse a las células espumosas, recubrieron las partículas con membranas de macrófagos reales (células inmunitarias) y añadieron un péptido corto que se une a una señal de “cómeme” expuesta en la superficie de las células espumosas. Esto creó un nanoagente jerárquico: primero atraído hacia las paredes arteriales inflamadas, luego más precisamente hacia las células espumosas enterradas en la placa y, finalmente, activado por el ambiente químico estresado dentro de esas células.
Evaluar seguridad, precisión e impacto en células
En cultivo celular, el nanoagente resultó ser suave con las células sanas, mostrando poca toxicidad o daño a membranas. Sin embargo, al exponerse a células espumosas, las partículas fueron internalizadas con mucha mayor eficiencia que versiones más simples sin el manto de membrana ni el péptido dirigidor. Una vez dentro de estas células enfermas, el ambiente oxidativo provocó la degradación de la carcasa polimérica y la liberación de atorvastatina. Esto redujo los niveles dañinos de especies reactivas de oxígeno, frenó la captación de partículas grasas y aumentó la exportación de colesterol activando proteínas transportadoras naturales. Al mismo tiempo, el tratamiento disminuyó los niveles de CD47, una molécula de superficie que normalmente dice a las células inmunitarias “no me comas”, facilitando que los macrófagos eliminen las células espumosas.
Revelar y reparar placas en animales vivos
En ratones genéticamente predispuestos a la aterosclerosis y alimentados con una dieta alta en grasas, el nanoagente circuló en la sangre durante horas y se acumuló de forma pronunciada en las placas arteriales. El equipo mostró que las señales infrarrojas, fotoacústicas y de RM aumentaron de forma concomitante en las regiones ricas en placa y coincidieron estrechamente con medidas tisulares del tamaño de la placa, la inflamación y la fragilidad. Las placas más avanzadas e inestables produjeron señales más intensas que las más leves, lo que sugiere que la plataforma puede clasificar la severidad de la enfermedad. Cuando se utilizó repetidamente como tratamiento, el nanoagente dirigido redujo la carga total de placa mucho más que la atorvastatina libre o versiones nanoparticuladas menos sofisticadas. Disminuyó el estrés oxidativo, redujo los niveles de mediadores inflamatorios y desplazó las poblaciones celulares inmunitarias hacia un equilibrio más calmado y protector.
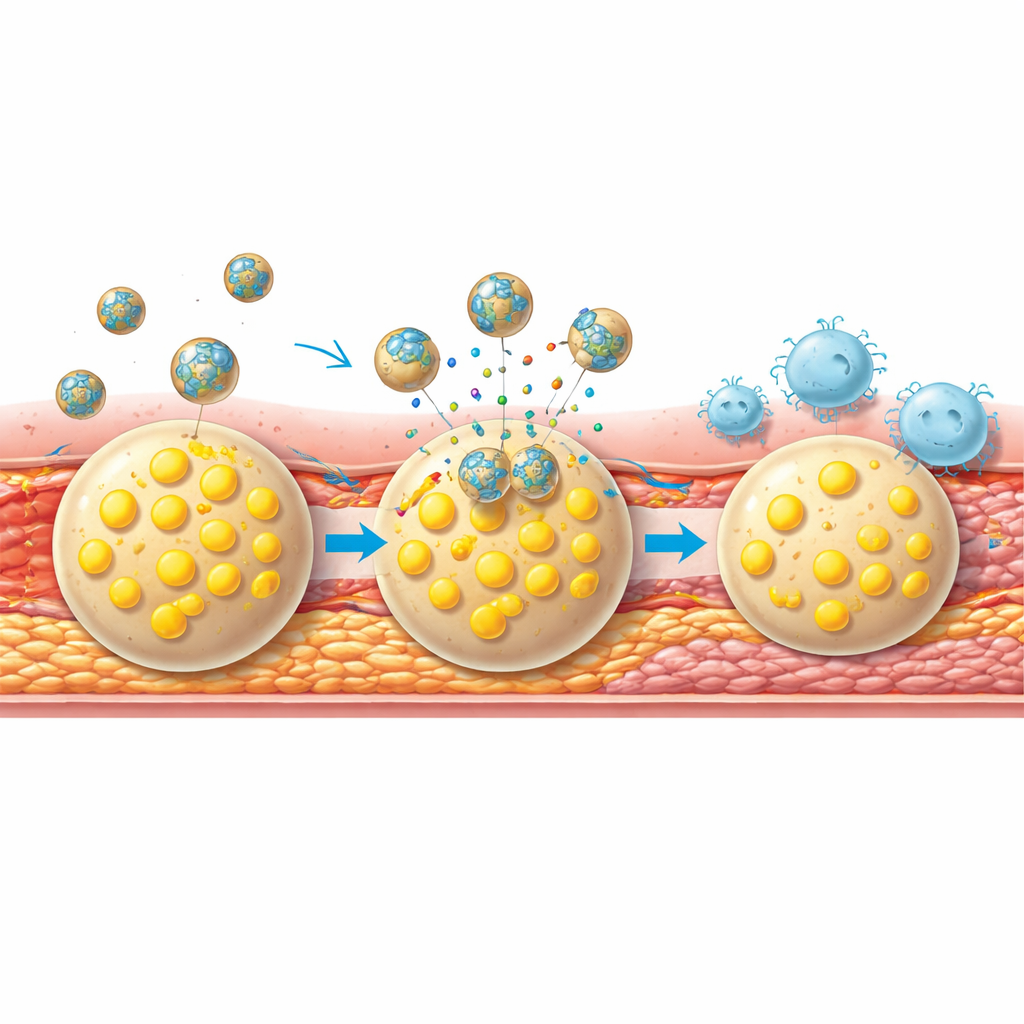
Endurecer las placas y seguir el progreso
Además de reducir el tamaño de las placas, la terapia las hizo menos propensas a romperse. Los ratones tratados mostraron menos de una enzima que erosiona la capa fibrosa sobre las placas, más colágeno y más células del músculo liso que refuerzan esa cubierta, y menos vasos sanguíneos frágiles recién formados que pueden filtrar y desestabilizar la lesión. Lo importante es que las mismas nanopartículas utilizadas para el tratamiento también sirvieron como reporteras en tiempo real del éxito: tras semanas de terapia, las sesiones de imagen repetidas mostraron señales multimodales mucho más débiles en las arterias carótidas, reflejando la estructura de placa más sana observada al microscopio.
Qué podría significar esto para los pacientes
Para una persona no experta, este trabajo apunta hacia futuros “agentes de contraste inteligentes” que hacen mucho más que ayudar a los radiólogos a ver obstrucciones. Este nanoagente por capas encuentra las placas más peligrosas e inflamadas, entrega el fármaco exactamente donde se necesita, ayuda al organismo a eliminar las células espumosas nocivas y luego informa sobre la eficacia del tratamiento, todo ello sin cirugía. Aunque estos resultados se han obtenido en ratones y la traducción a humanos requerirá pruebas cuidadosas, el estudio plantea una estrategia potente para convertir placas arteriales silenciosas e inestables en estructuras más dóciles y resistentes antes de que provoquen infartos o accidentes cerebrovasculares.
Cita: Song, J., Kang, X., Yang, S. et al. A hierarchical theranostic nanoagent for multimodal imaging and targeted foam cell intervention in atherosclerosis. Nat Commun 17, 3794 (2026). https://doi.org/10.1038/s41467-026-70463-7
Palabras clave: aterosclerosis, nanopartículas, imagen multimodal, células espumosas, estabilización de placa