Clear Sky Science · sv
PLAAT2 hämmar utvecklingen av magsäckscancer genom att underlätta ubiquitinering av cMyc och hämma MEK/ERK‑signalering
Varför denna studie är viktig för magsäckscancer
Magsäckscancer förblir en av världens dödligaste cancerformer, delvis eftersom den ofta upptäcks sent och kan sprida sig snabbt. Denna studie undersöker en hittills lågprofilerad, inneboende försvarare i våra celler—ett protein kallat PLAAT2—och visar hur det hjälper till att hålla magsäckscancer i schack. Genom att avslöja hur denna molekyl fungerar och varför den ofta förloras i tumörer pekar forskningen ut en ny svag punkt i magsäckscancer som framtida läkemedel kan rikta in sig mot.
En saknad beskyddare i tumörvävnad
För att se om PLAAT2 spelar en roll vid magsäckscancer började forskarna med att jämföra tumörprover med intilliggande icke‑cancerös vävnad från mer än hundra patienter, samt data från stora offentliga cancerregister. De fann ett tydligt mönster: PLAAT2‑nivåerna var mycket lägre i cancerös vävnad än i frisk magslemhinna. Patienter vars tumörer hade särskilt låga mängder PLAAT2 tenderade att ha mer avancerad sjukdom, mer spridning till lymfkörtlar och sämre överlevnad. Liknande minskningar sågs även i magsäckscellinjer i laboratoriet, vilket tyder på att förlust av detta protein är ett vanligt kännetecken för sjukdomen.
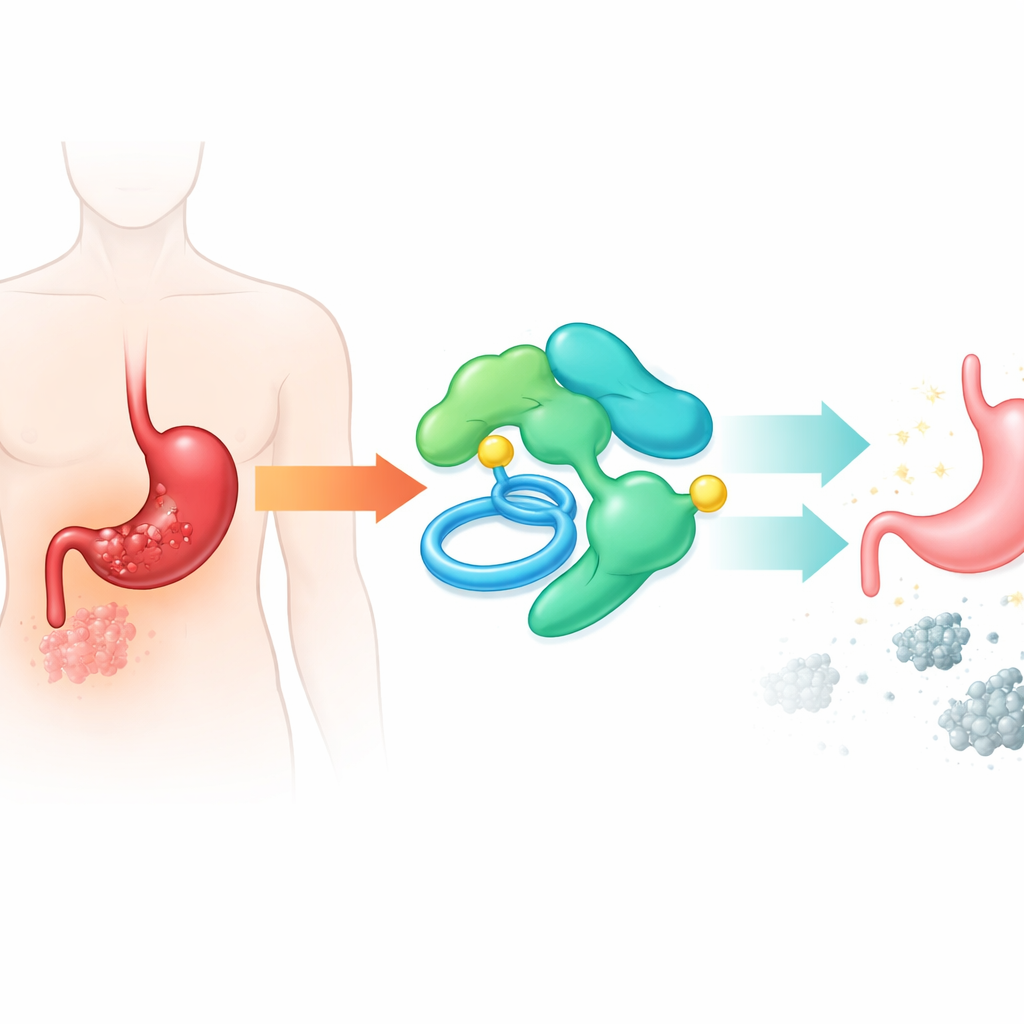
Hur avstängning och återställande av PLAAT2 förändrar cancerns beteende
Forskargruppen testade sedan vad som händer när PLAAT2‑nivåerna konstgjort sänks eller höjs i cancerceller. När PLAAT2 stängdes av växte tumörcellerna snabbare, bildade fler kolonier, rörde sig enklare genom laboratoriemembran och var mindre benägna att genomgå programmerad celldöd. När PLAAT2 återställdes till högre nivåer skedde motsatsen: celltillväxten saktade ner, rörelse och invasion minskade och fler celler dog. Dessa förändringar observerades också hos möss: tumörer utan PLAAT2 växte större, medan tumörer med extra PLAAT2 förblev mindre, vilket bekräftar att denna molekyl fungerar som en verklig broms för cancerutveckling.
Kortslutning av en tillväxtomkopplare inuti cellen
Genom att gå djupare upptäckte forskarna att PLAAT2 reglerar ett kraftfullt tillväxtdrivande protein kallat cMyc, som är abnormt aktivt i många cancerformer. I stället för att förändra hur mycket cMyc som produceras påverkade PLAAT2 hur snabbt cMyc bryts ner. Med mer PLAAT2 märktes cMyc‑proteiner ut för nedbrytning och rensades bort snabbare; med mindre PLAAT2 kvarstod cMyc och ackumulerades. Denna nedbrytningsprocess bygger på ett cellärt "återvinnings"‑system där små molekylära märken signalerar vilka proteiner som ska förstöras. PLAAT2 visade sig hjälpa till att föra cMyc i kontakt med TRIM32, ett enzym som fäster dessa märken. TRIM32 sätter sedan specifika markörer på cMyc vid två nyckelpositioner, vilket markerar det för nedbrytning och håller dess tillväxtfrämjande aktivitet i schack.
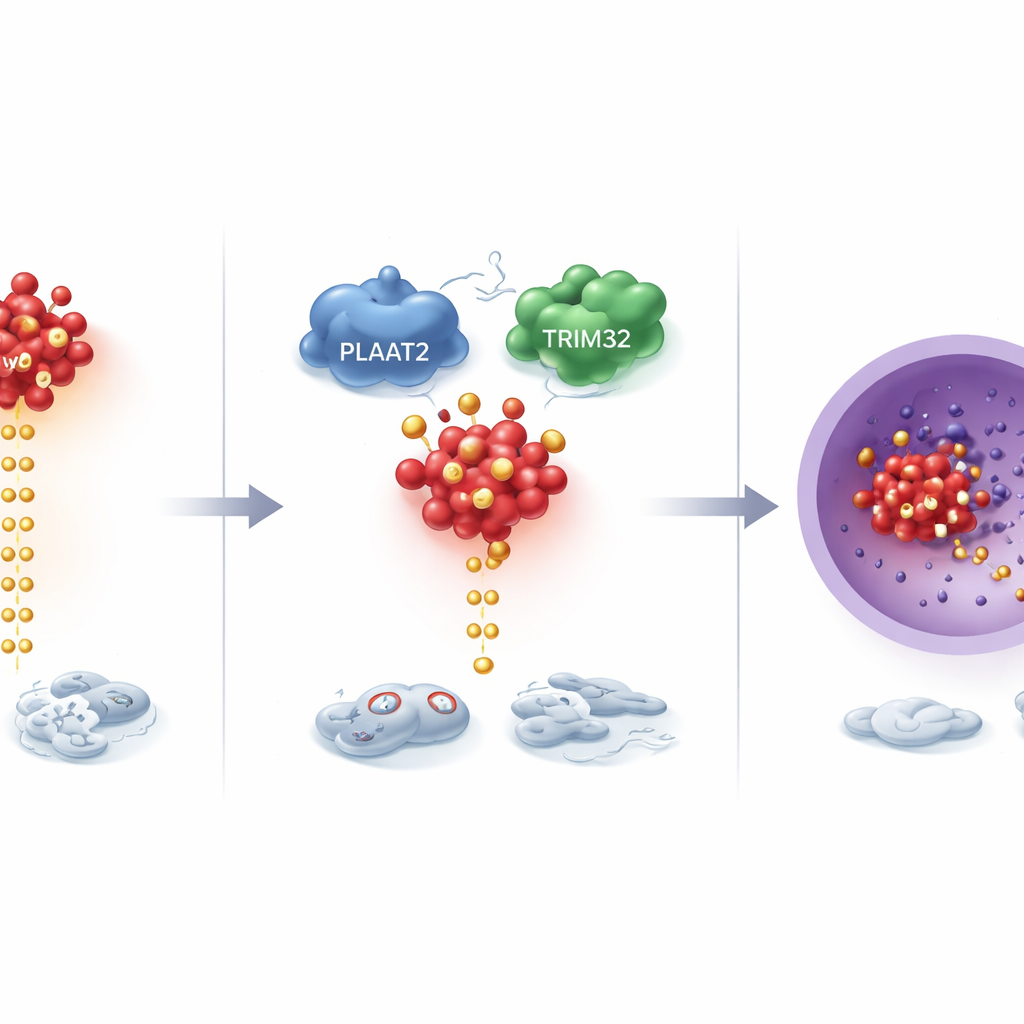
Nedreglering av en central cancer‑signalväg
Eftersom cMyc kan aktivera en kedja av signaler som uppmuntrar celler att dela sig, migrera och förändra identitet, studerade forskarna en huvudväg som det kontrollerar, känd som MEK/ERK‑vägen. När PLAAT2‑nivåerna var låga blev denna väg mer aktiv, och cancerceller visade tecken på en process kallad epitelial–mesenkymal omvandling, där normalt välordnade celler lossnar från varandra och blir mer rörliga och invasiva. Återställande av PLAAT2 vände dessa förändringar: MEK/ERK‑vägen tystnade, markörer för invasivt beteende minskade och cellerna uppträdde mindre aggressivt. Att blockera eller förstärka cMyc direkt kunde utplåna effekterna av PLAAT2, vilket understryker att detta skyddande protein till stor del verkar genom att tygla cMyc och de signaler det sänder.
Vad detta betyder för framtida behandlingar
Sammantaget tyder fynden på att PLAAT2 är en viktig inneboende skyddsmekanism mot magsäckscancer: det hjälper till att rekrytera TRIM32 för att avlägsna överskott av cMyc och därigenom dämpa en central väg för tillväxt och spridning. När PLAAT2 förloras eller tystas blir cMyc och MEK/ERK‑signalering okontrollerade, vilket tillåter tumörer att växa och invadera lättare. Genom att belysa kedjan PLAAT2–TRIM32–cMyc som en kritisk kontrollpunkt öppnar studien nya möjligheter: framtida behandlingar kan syfta till att återställa PLAAT2, stärka TRIM32:s verkan på cMyc eller direkt imitera denna nedbrytningsprocess för att bromsa eller stoppa utvecklingen av magsäckscancer.
Citering: Chu, M., Shi, X., Shi, Z. et al. PLAAT2 suppresses gastric cancer progression by facilitating cMyc ubiquitination and inhibiting MEK/ERK signaling. Cell Death Dis 17, 314 (2026). https://doi.org/10.1038/s41419-026-08546-y
Nyckelord: magsäckscancer, PLAAT2, cMyc, ubiquitinering, MEK ERK‑signalering