Clear Sky Science · pl
PLAAT2 hamuje postęp raka żołądka przez ułatwienie ubikwitynacji cMyc i zahamowanie sygnalizacji MEK/ERK
Dlaczego to badanie ma znaczenie dla raka żołądka
Rak żołądka pozostaje jednym z najgroźniejszych nowotworów na świecie, między innymi dlatego, że często wykrywa się go późno i potrafi szybko się rozprzestrzeniać. W tym badaniu zbadano mało poznanego wewnętrznego obrońcę komórkowego — białko o nazwie PLAAT2 — i wykazano, jak pomaga ono kontrolować rozwój raka żołądka. Odkrycie mechanizmu działania tej cząsteczki oraz przyczyn jej utraty w wielu guzach wskazuje na nowy punkt wrażliwości raka żołądka, który w przyszłości mogą wykorzystać leki.
Brakujący ochroniarz w tkance guza
Aby ustalić, czy PLAAT2 odgrywa rolę w raku żołądka, badacze porównali próbki nowotworowe z pobliską tkanką niespokrewnioną nowotworowo pochodzącą od ponad stu pacjentów oraz dane z dużych publicznych baz nowotworowych. Stwierdzili wyraźny wzorzec: poziomy PLAAT2 były znacznie niższe w tkance nowotworowej niż w zdrowej błonie śluzowej żołądka. Pacjenci, których guzy zawierały szczególnie mało PLAAT2, mieli zazwyczaj chorobę w bardziej zaawansowanym stadium, większe zajęcie węzłów chłonnych i gorsze przeżycia ogólne. Podobne obniżenia zaobserwowano w liniach komórkowych raka żołądka w laboratorium, co sugeruje, że utrata tego białka jest częstą cechą choroby.
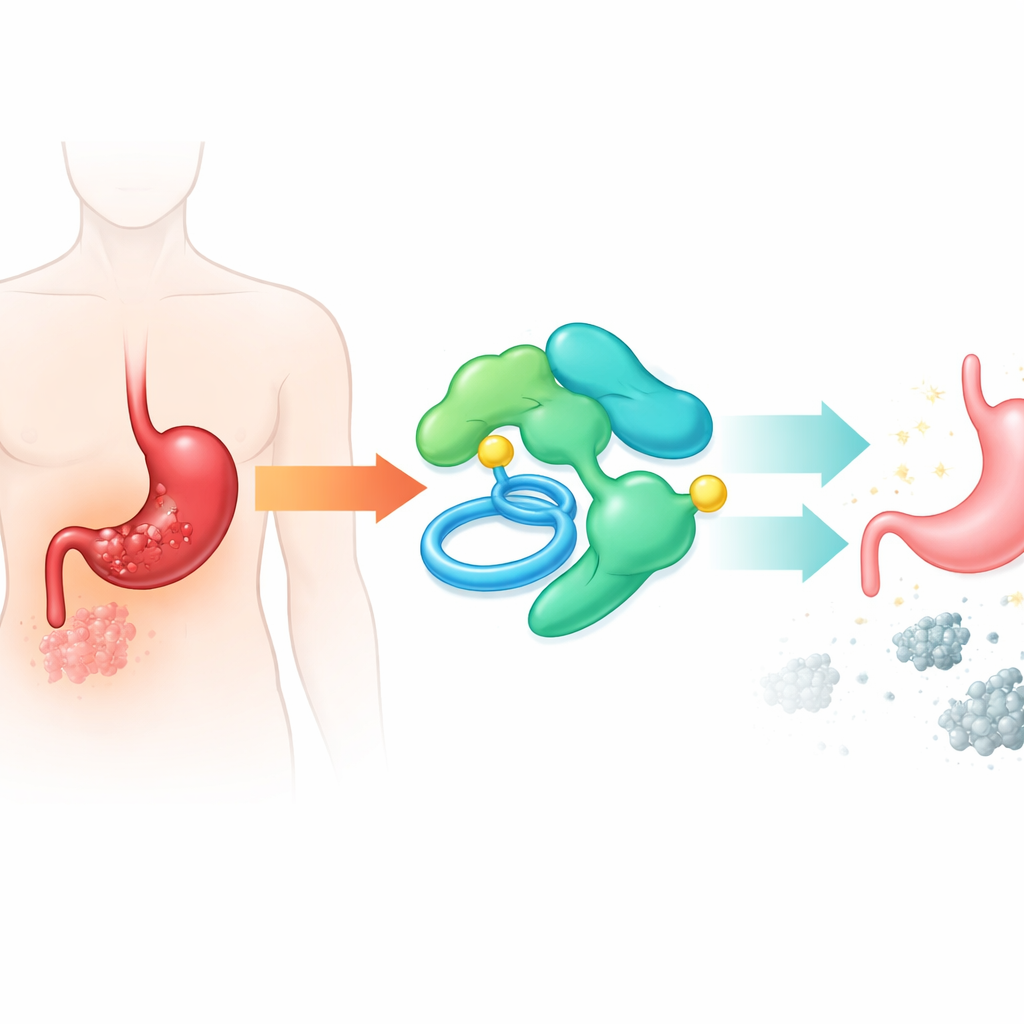
Jak wyciszenie i przywrócenie PLAAT2 zmienia zachowanie nowotworu
Zespół następnie sprawdził, co się dzieje, gdy poziomy PLAAT2 są sztucznie obniżane lub podnoszone w komórkach nowotworowych. Gdy PLAAT2 zostało wyłączone, komórki nowotworowe rosły szybciej, tworzyły więcej kolonii, łatwiej przechodziły przez laboratoryjne membrany i miały mniejsze skłonności do zaprogramowanej śmierci. Gdy PLAAT2 przywrócono do wyższych poziomów, obserwowano odwrotny efekt: wzrost komórek spowalniał, ruch i inwazja zmniejszały się, a więcej komórek umierało. Zmiany te zaobserwowano także u myszy — guzy pozbawione PLAAT2 rosły większe, podczas gdy te z nadmiarem PLAAT2 pozostawały mniejsze — co potwierdza, że cząsteczka ta działa jako rzeczywisty hamulec postępu nowotworu.
Przerywanie wewnątrzkomórkowego przełącznika wzrostu
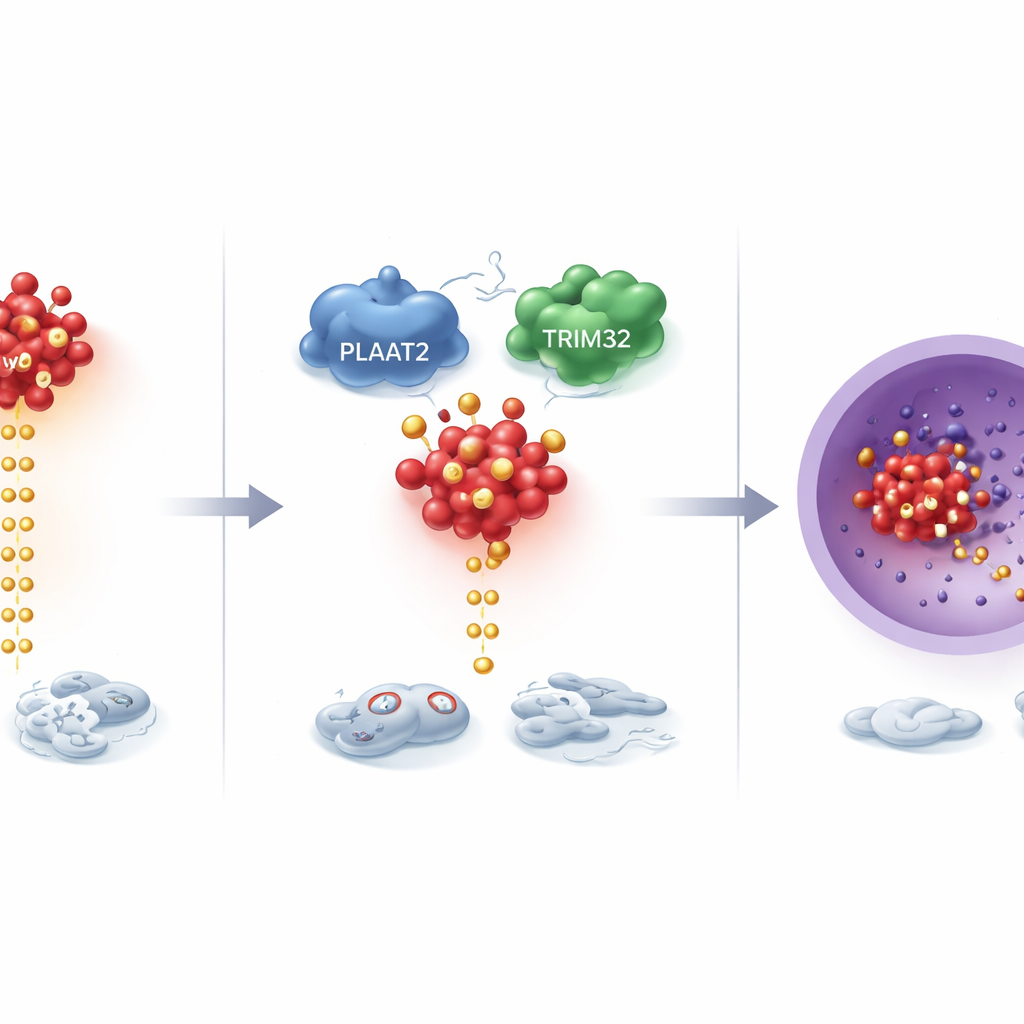
Badając mechanizm głębiej, naukowcy odkryli, że PLAAT2 kontroluje silny promotor wzrostu — białko cMyc — które jest nadmiernie aktywne w wielu nowotworach. Zamiast zmieniać tempo produkcji cMyc, PLAAT2 wpływało na szybkość jego rozkładu. Przy wyższych poziomach PLAAT2 białka cMyc były oznaczane do usunięcia i szybciej eliminowane; przy niższych poziomach cMyc utrzymywał się i kumulował. Proces ten opiera się na komórkowym systemie „recyklingu”, w którym małe znaczniki molekularne sygnalizują, które białka powinny zostać zniszczone. Stwierdzono, że PLAAT2 pomaga sprowadzić cMyc do TRIM32 — enzymu przyłączającego te znaczniki. TRIM32 następnie umieszcza specyficzne znaczniki na cMyc w dwóch kluczowych pozycjach, oznaczając je do degradacji i ograniczając jego aktywność promującą wzrost.
Przyciszanie głównej ścieżki sygnalizacyjnej raka
Ponieważ cMyc może aktywować kaskadę sygnałów sprzyjających dzieleniu, migracji i zmianie tożsamości komórek, badacze zajrzeli na jedną z głównych dróg, które kontroluje — znaną jako ścieżka MEK/ERK. Gdy poziomy PLAAT2 były niskie, ta ścieżka stawała się bardziej aktywna, a komórki nowotworowe wykazywały cechy przejścia nabłonkowo-mezenchymalnego (EMT), w którym normalnie uporządkowane komórki luzują połączenia i stają się bardziej ruchome i inwazyjne. Przywrócenie PLAAT2 odwracało te zmiany: ścieżka MEK/ERK uspokajała się, markery zachowań inwazyjnych spadały, a komórki zachowywały się mniej agresywnie. Blokowanie lub bezpośrednie zwiększanie aktywności cMyc mogło cofnąć efekty PLAAT2, podkreślając, że to ochronne białko działa w dużej mierze przez ograniczanie cMyc i sygnałów, które on wysyła.
Co to znaczy dla przyszłych terapii
Podsumowując, wyniki sugerują, że PLAAT2 jest ważnym naturalnym zabezpieczeniem przeciwko rakowi żołądka — pomaga rekrutować TRIM32 do pozbywania się nadmiaru cMyc i w ten sposób tłumi większą ścieżkę wzrostu i rozprzestrzeniania. Gdy PLAAT2 jest utracone lub wyciszone, cMyc i sygnalizacja MEK/ERK działają bez kontroli, co pozwala guzom łatwiej rosnąć i naciekać okoliczne tkanki. Wskazanie łańcucha PLAAT2–TRIM32–cMyc jako kluczowego punktu kontroli otwiera nowe możliwości: przyszłe terapie mogłyby dążyć do przywrócenia PLAAT2, wzmocnienia działania TRIM32 na cMyc lub bezpośredniego naśladowania tego procesu degradacji, aby spowolnić lub zatrzymać postęp raka żołądka.
Cytowanie: Chu, M., Shi, X., Shi, Z. et al. PLAAT2 suppresses gastric cancer progression by facilitating cMyc ubiquitination and inhibiting MEK/ERK signaling. Cell Death Dis 17, 314 (2026). https://doi.org/10.1038/s41419-026-08546-y
Słowa kluczowe: rak żołądka, PLAAT2, cMyc, ubikwitynacja, sygnalizacja MEK ERK