Clear Sky Science · ru
PLAAT2 подавляет прогрессию рака желудка, способствуя убиквитинированию cMyc и подавляя сигнальную каскаду MEK/ERK
Почему это исследование важно для рака желудка
Рак желудка по-прежнему остается одним из самых смертоносных видов рака в мире, отчасти потому, что его часто выявляют поздно, и он может быстро распространяться. В этом исследовании изучается малоизвестный внутриклеточный защитник — белок PLAAT2 — и показано, как он помогает сдерживать развитие рака желудка. Раскрывая механизм действия этой молекулы и причины её утраты во многих опухолях, работа указывает на новую уязвимость при гастральном раке, которую в будущем можно было бы использовать в терапии.
Отсутствующий защитник в опухолевой ткани
Чтобы понять, играет ли PLAAT2 роль при раке желудка, исследователи сравнили опухолевые образцы с прилежащей незлокачественной тканью более чем у сотни пациентов, а также проанализировали данные крупных публичных онкологических баз. Они обнаружили четкую закономерность: уровень PLAAT2 был значительно ниже в опухолевой ткани по сравнению со здоровой слизистой желудка. У пациентов с особенно низким содержанием PLAAT2 опухоль чаще была на более поздних стадиях, чаще отмечалось поражение лимфоузлов и наблюдалась худшая выживаемость в целом. Аналогичное снижение выявлялось и в линиях клеток рака желудка в лаборатории, что указывает на то, что утрата этого белка является общей чертой заболевания.
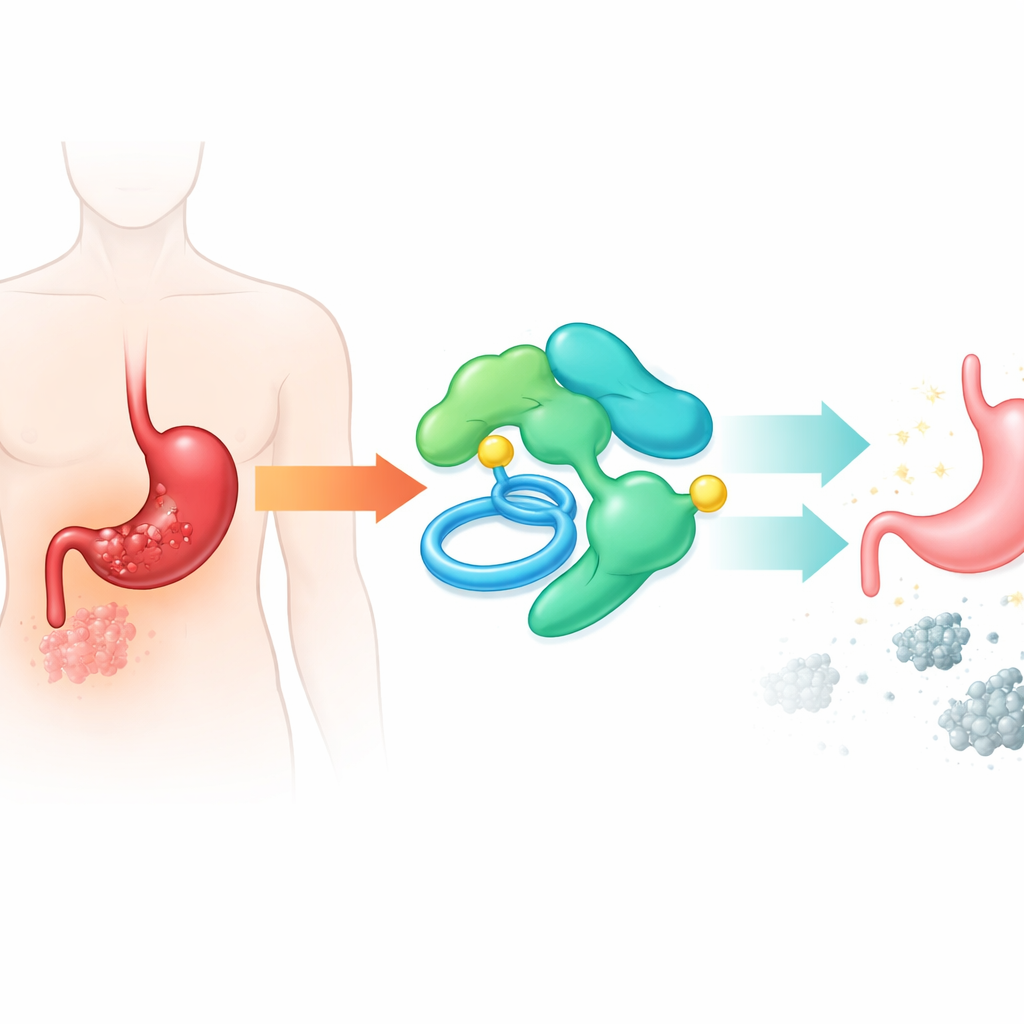
Как подавление и восстановление PLAAT2 меняют поведение раковых клеток
Далее команда проверила, что происходит при искусственном снижении или повышении уровня PLAAT2 в раковых клетках. При выключении PLAAT2 клетки опухоли росли быстрее, образовывали больше колоний, легче проходили через лабораторные мембраны и реже подвергались программируемой гибели. При восстановлении PLAAT2 до более высокого уровня наблюдалось обратное: рост клеток замедлялся, миграция и инвазия уменьшались, и доля погибающих клеток увеличивалась. Эти изменения подтвердились и на моделях с мышами: опухоли без PLAAT2 росли больше, тогда как опухоли с избытком PLAAT2 оставались меньшими, что подтверждает, что этот белок действительно действует как тормоз прогрессии рака.
Короткое замыкание ключевого сигнального переключателя в клетке
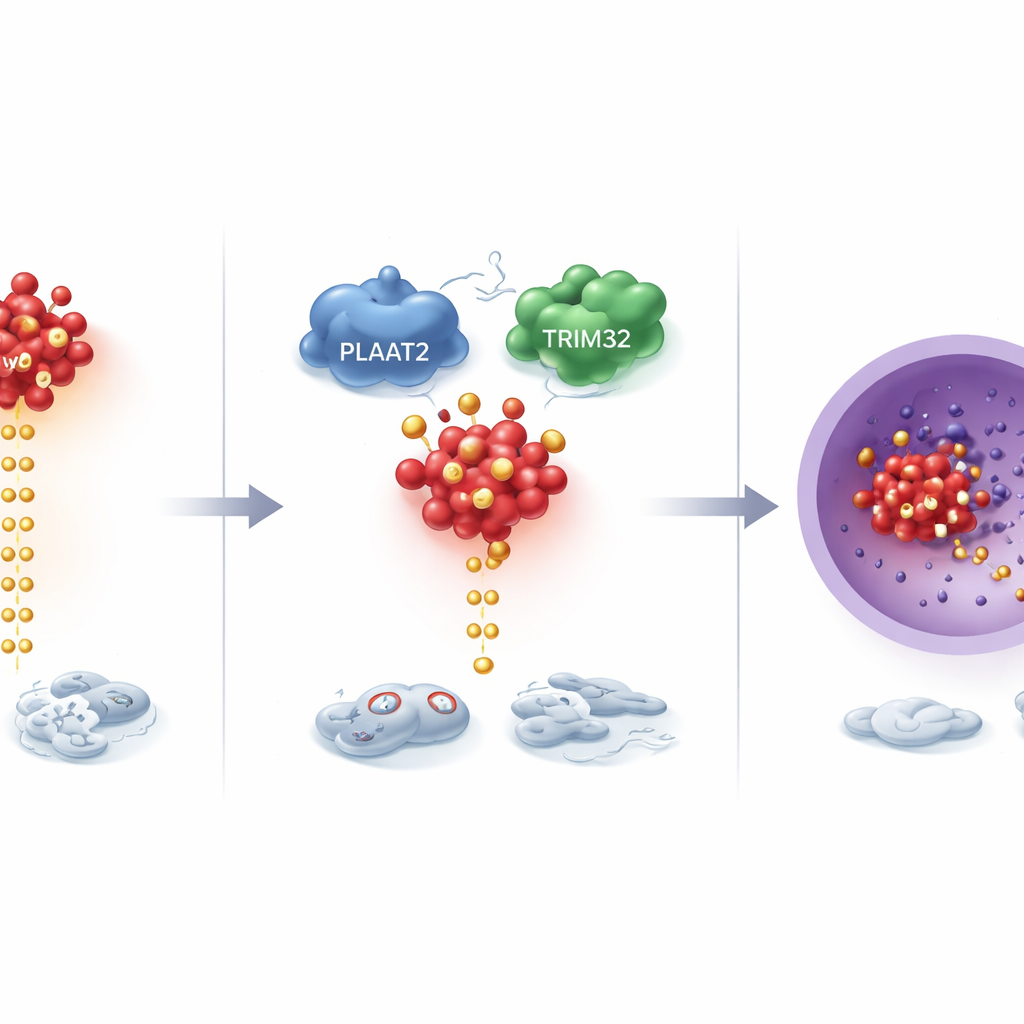
При более глубоком изучении ученые выяснили, что PLAAT2 контролирует мощный белок, стимулирующий рост, известный как cMyc, который чрезмерно активен во многих раках. PLAAT2 влиял не на синтез cMyc, а на скорость его разрушения. При повышенном уровне PLAAT2 молекулы cMyc помечались для удаления и быстрее удалялись; при снижении PLAAT2 cMyc дольше сохранялся и накапливался. Этот процесс разрушения опирается на клеточную «переработку», в которой маленькие молекулярные метки указывают, какие белки следует уничтожить. PLAAT2 помогает сближать cMyc с TRIM32 — ферментом, присоединяющим эти метки. TRIM32 ставит специфические метки на cMyc в двух ключевых позициях, помечая его для разрушения и сдерживая его промоторную по отношению к росту активность.
Торможение важного онкологического сигнального пути
Поскольку cMyc способен активировать каскад сигналов, стимулирующих деление, миграцию и смену фенотипа клеток, исследователи изучили один из основных маршрутов, которым он управляет — путь MEK/ERK. При низком уровне PLAAT2 этот путь становился более активным, и клетки проявляли признаки эпителиально-мезенхимального перехода — процесса, при котором обычно хорошо организованные клетки ослабляют контакты и становятся более подвижными и инвазивными. Восстановление PLAAT2 обращало эти изменения: активность MEK/ERK снижалась, маркеры инвазивного поведения уменьшались, и клетки вели себя менее агрессивно. Блокирование или прямое усиление cMyc могло нивелировать эффекты PLAAT2, что подчеркивает, что защитное действие этого белка в основном реализуется через подавление cMyc и связанных с ним сигналов.
Что это значит для будущих методов лечения
В целом результаты указывают, что PLAAT2 является важным природным защитным фактором против рака желудка: он помогает привлекать TRIM32 для удаления избыточного cMyc и, в свою очередь, ослабляет ключевой путь роста и распространения. При утрате или выключении PLAAT2 cMyc и сигнализация MEK/ERK выходят из-под контроля, что способствует росту и инвазии опухолей. Выделив цепочку PLAAT2–TRIM32–cMyc как критический контрольный узел, исследование открывает новые возможности: будущие терапии могут быть направлены на восстановление PLAAT2, усиление действия TRIM32 на cMyc или прямое имитирование этого процесса деградации, чтобы замедлить или остановить прогрессию рака желудка.
Цитирование: Chu, M., Shi, X., Shi, Z. et al. PLAAT2 suppresses gastric cancer progression by facilitating cMyc ubiquitination and inhibiting MEK/ERK signaling. Cell Death Dis 17, 314 (2026). https://doi.org/10.1038/s41419-026-08546-y
Ключевые слова: рак желудка, PLAAT2, cMyc, убиквитинирование, сигнализация MEK ERK