Clear Sky Science · fr
PLAAT2 supprime la progression du cancer gastrique en facilitant l’ubiquitination de cMyc et en inhibant la signalisation MEK/ERK
Pourquoi cette étude est importante pour le cancer de l’estomac
Le cancer de l’estomac (gastrique) reste l’un des cancers les plus mortels au monde, en partie parce qu’il est souvent diagnostiqué tardivement et peut se propager rapidement. Cette étude explore un défenseur peu connu présent dans nos cellules, une protéine appelée PLAAT2, et montre comment elle contribue à contenir le cancer gastrique. En dévoilant le mode d’action de cette molécule et les raisons de sa perte dans de nombreuses tumeurs, les chercheurs mettent en évidence une nouvelle vulnérabilité du cancer gastrique que de futurs traitements pourraient cibler.
Un protecteur absent dans les tissus tumoraux
Pour déterminer si PLAAT2 joue un rôle dans le cancer gastrique, les chercheurs ont commencé par comparer des échantillons tumoraux avec des tissus non cancéreux adjacents provenant de plus d’une centaine de patients, ainsi que des données de larges bases publiques sur le cancer. Ils ont observé un schéma clair : les niveaux de PLAAT2 étaient nettement plus faibles dans les tissus cancéreux que dans la muqueuse gastrique saine. Les patients dont les tumeurs présentaient des quantités particulièrement faibles de PLAAT2 avaient tendance à présenter une maladie plus avancée, plus de métastases ganglionnaires et une survie globale plus mauvaise. Des réductions similaires ont été constatées lors de l’examen de lignées cellulaires de cancer gastrique en laboratoire, ce qui suggère que la perte de cette protéine est une caractéristique fréquente de la maladie.
Comment le silence et la restauration de PLAAT2 modifient le comportement du cancer
L’équipe a ensuite évalué ce qui se produit lorsque les niveaux de PLAAT2 sont artificiellement réduits ou augmentés dans des cellules tumorales. Lorsque PLAAT2 était éteint, les cellules tumorales proliféraient plus rapidement, formaient davantage de colonies, traversaient plus facilement des membranes expérimentales et avaient moins tendance à entrer en apoptose. Quand PLAAT2 était rétabli à des niveaux plus élevés, l’effet inverse était observé : la croissance cellulaire ralentissait, la mobilité et l’invasion diminuaient et davantage de cellules mouraient. Ces changements ont également été observés chez la souris, où les tumeurs dépourvues de PLAAT2 croissaient davantage, tandis que celles exprimant un surplus de PLAAT2 restaient plus petites, confirmant que cette molécule agit comme un véritable frein à la progression tumorale.
Court-circuiter un interrupteur de croissance intracellulaire
En creusant plus avant, les scientifiques ont découvert que PLAAT2 contrôle une protéine promotrice de croissance puissante appelée cMyc, qui est anormalement active dans de nombreux cancers. Plutôt que d’altérer la production de cMyc, PLAAT2 influait sur la vitesse à laquelle cMyc est dégradé. En présence de davantage de PLAAT2, les protéines cMyc étaient marquées pour élimination et éliminées plus rapidement ; en cas de déficit en PLAAT2, cMyc persistait et s’accumulait. Ce processus de dégradation dépend d’un système cellulaire de « recyclage » dans lequel de petites étiquettes moléculaires indiquent quelles protéines doivent être détruites. Il a été montré que PLAAT2 aide à rapprocher cMyc de TRIM32, une enzyme qui attache ces étiquettes. TRIM32 ajoute alors des marques spécifiques sur cMyc à deux positions clés, le signalant pour destruction et limitant ainsi son activité promotrice de croissance.
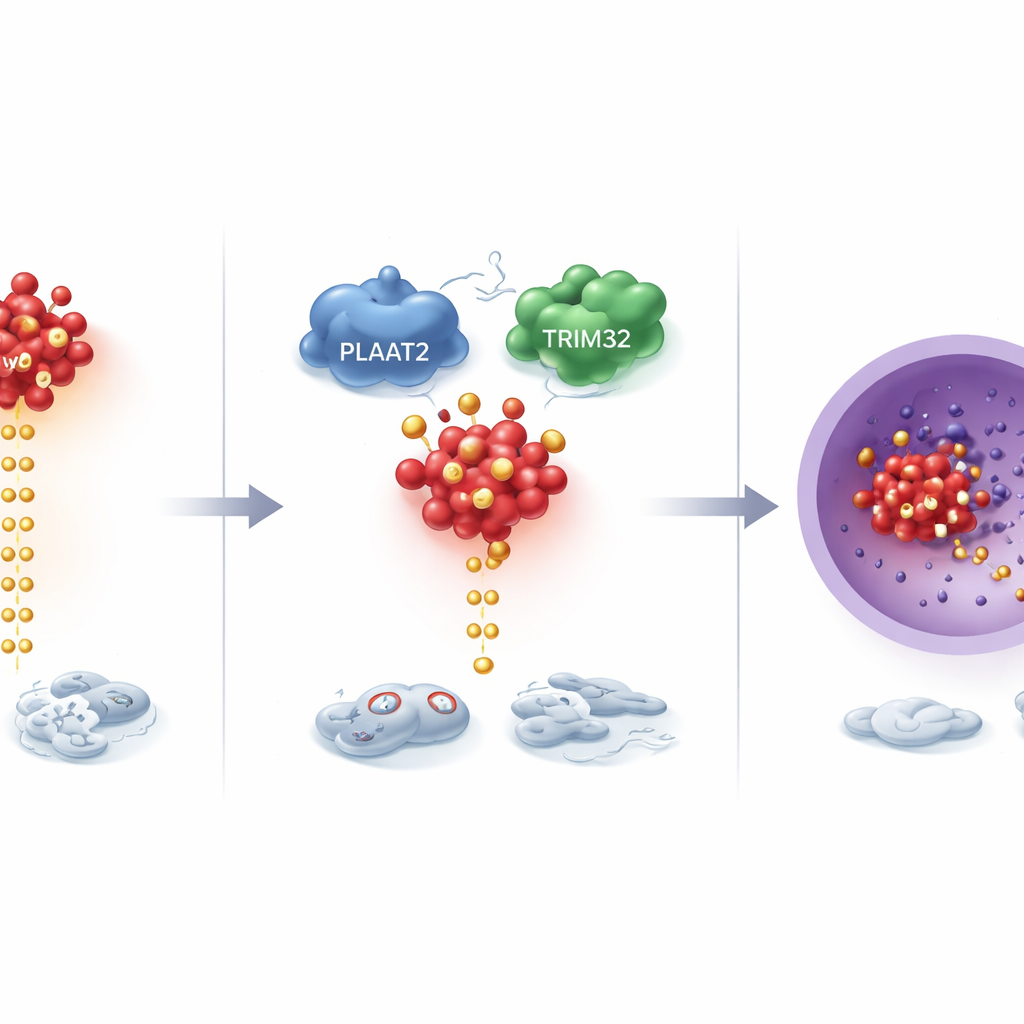
Réduire une voie majeure de signalisation du cancer
Parce que cMyc peut activer une cascade de signaux qui favorisent la division, la migration et la modification d’identité cellulaire, les chercheurs se sont intéressés à une voie majeure qu’il contrôle, connue sous le nom de voie MEK/ERK. Lorsque les niveaux de PLAAT2 étaient bas, cette voie devenait plus active et les cellules tumorales présentaient des caractéristiques d’un processus appelé transition épithélio–mésenchymateuse, au cours duquel des cellules normalement bien ordonnées relâchent leurs connexions et deviennent plus mobiles et invasives. La restauration de PLAAT2 inversait ces changements : la voie MEK/ERK se calmait, les marqueurs du comportement invasif diminuaient et les cellules adoptaient un comportement moins agressif. Bloquer ou renforcer directement cMyc pouvait annuler les effets de PLAAT2, soulignant que cette protéine protectrice agit principalement en maîtrisant cMyc et les signaux qu’il engendre.
Ce que cela signifie pour les traitements futurs
Pris ensemble, ces résultats suggèrent que PLAAT2 est un garde-fou naturel important contre le cancer gastrique, aidant à recruter TRIM32 pour éliminer l’excès de cMyc et, par conséquent, à atténuer une voie majeure de croissance et de dissémination. Lorsque PLAAT2 est perdu ou silencé, cMyc et la signalisation MEK/ERK fonctionnent sans contrôle, permettant aux tumeurs de croître et d’envahir plus facilement. En mettant en lumière cette chaîne PLAAT2–TRIM32–cMyc comme point de contrôle critique, l’étude ouvre de nouvelles possibilités : les thérapies futures pourraient viser à restaurer PLAAT2, augmenter l’action de TRIM32 sur cMyc, ou imiter directement ce processus de dégradation pour ralentir ou arrêter la progression du cancer gastrique.
Citation: Chu, M., Shi, X., Shi, Z. et al. PLAAT2 suppresses gastric cancer progression by facilitating cMyc ubiquitination and inhibiting MEK/ERK signaling. Cell Death Dis 17, 314 (2026). https://doi.org/10.1038/s41419-026-08546-y
Mots-clés: cancer gastrique, PLAAT2, cMyc, ubiquitination, signalisation MEK ERK