Clear Sky Science · ar
PLAAT2 يثبط تقدم سرطان المعدة عن طريق تيسير يوبيكويتينية cMyc وكبح إشارات MEK/ERK
لماذا تهم هذه الدراسة سرطان المعدة
لا يزال سرطان المعدة واحداً من أخطر أنواع السرطان في العالم، جزئياً لأنه غالباً ما يُكتشف متأخراً ويمكن أن ينتشر بسرعة. تستكشف هذه الدراسة حاجزاً طبيعياً قليلاً المعروفة داخل خلايانا، وهو بروتين يُسمى PLAAT2، وتُظهر كيف يساعد في كبح سرطان المعدة. من خلال توضيح طريقة عمل هذا الجزيء ولماذا يفتقد في العديد من الأورام، تشير الأبحاث إلى نقطة ضعف جديدة في سرطان المعدة قد يكون بالإمكان استهدافها بعقاقير مستقبلية.
حامٍ مفقود في نسيج الورم
لفحص ما إذا كان PLAAT2 يلعب دوراً في سرطان المعدة، بدأ الباحثون بمقارنة عينات الأورام بالأنسجة غير السرطانية المجاورة من أكثر من مئة مريض، بالإضافة إلى بيانات من قواعد بيانات سرطان عامة كبيرة. وجدوا نمطاً واضحاً: كانت مستويات PLAAT2 أقل بكثير في الأنسجة السرطانية مقارنةً ببطانة المعدة السليمة. المرضى الذين كانت أورامهم تحتوي على كميات منخفضة جداً من PLAAT2 كانوا يميلون إلى وجود مرض أكثر تقدماً، ومدَى أكبر من انتشار للعقد اللمفاوية، وبقاء إجمالي أسوأ. شوهدت تخفيضات مماثلة عند فحص خطوط خلايا سرطان المعدة في المختبر، مما يوحي أن فقدان هذا البروتين سمة شائعة للمرض.
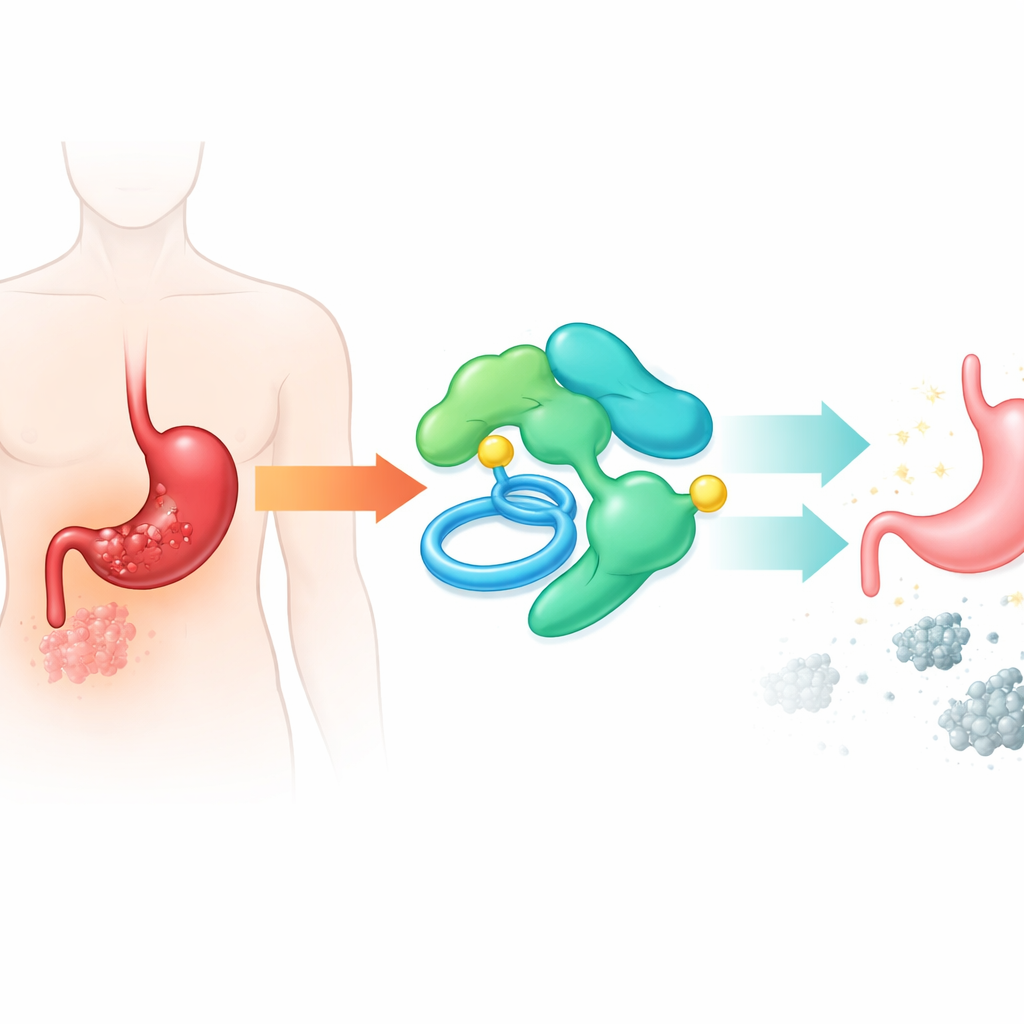
كيف يغير إسكات واستعادة PLAAT2 سلوك السرطان
اختبر الفريق بعد ذلك ما يحدث عندما تُخفض مستويات PLAAT2 أو تُعزز صناعياً في خلايا السرطان. عندما تم إيقاف PLAAT2، نمت خلايا الورم بسرعة أكبر، وتشكّلت مستعمرات أكثر، وتحركت بسهولة أكبر عبر أغشية المختبر، وكانت أقل ميلاً للخضوع للموت الخلوي المبرمج. عندما أعيد PLAAT2 لمستويات أعلى، حدث العكس: تباطأ نمو الخلايا، وانخفضت الحركة والغزو، وماتت مزيد من الخلايا. لوحظت هذه التغيرات أيضاً في الفئران، حيث نمت الأورام التي تفتقر إلى PLAAT2 أكبر، بينما بقيت الأورام التي تحتوي على PLAAT2 زائد أصغر، مؤكدةً أن هذا الجزيء يعمل كفرامل حقيقية لتقدم السرطان.
قصر دارة مفتاح نمو داخل الخلية
بتعمق أكثر، اكتشف العلماء أن PLAAT2 يتحكم في بروتين محرك قوي للنمو يُدعى cMyc، والذي يكون نشطاً بشكل غير طبيعي في العديد من السرطانات. بدل أن يغير كمية إنتاج cMyc، أثر PLAAT2 على مدى سرعة تكسير cMyc. بوجود المزيد من PLAAT2، تم وسم بروتينات cMyc للتخلص منها وإزالتها بشكل أسرع؛ ومع قلة PLAAT2، بقي cMyc أطول وتراكم. تعتمد عملية التكسير هذه على نظام «إعادة تدوير» خلوي حيث تشير وسوم جزيئية صغيرة إلى البروتينات التي يجب تدميرها. وُجد أن PLAAT2 يساعد على تقريب cMyc من TRIM32، إنزيم يعلّق هذه الوسوم. ثم يضع TRIM32 وسوماً محددة على cMyc في موقعين رئيسيين، معنوين إياه للتدمير وكبح نشاطه المحفز للنمو.
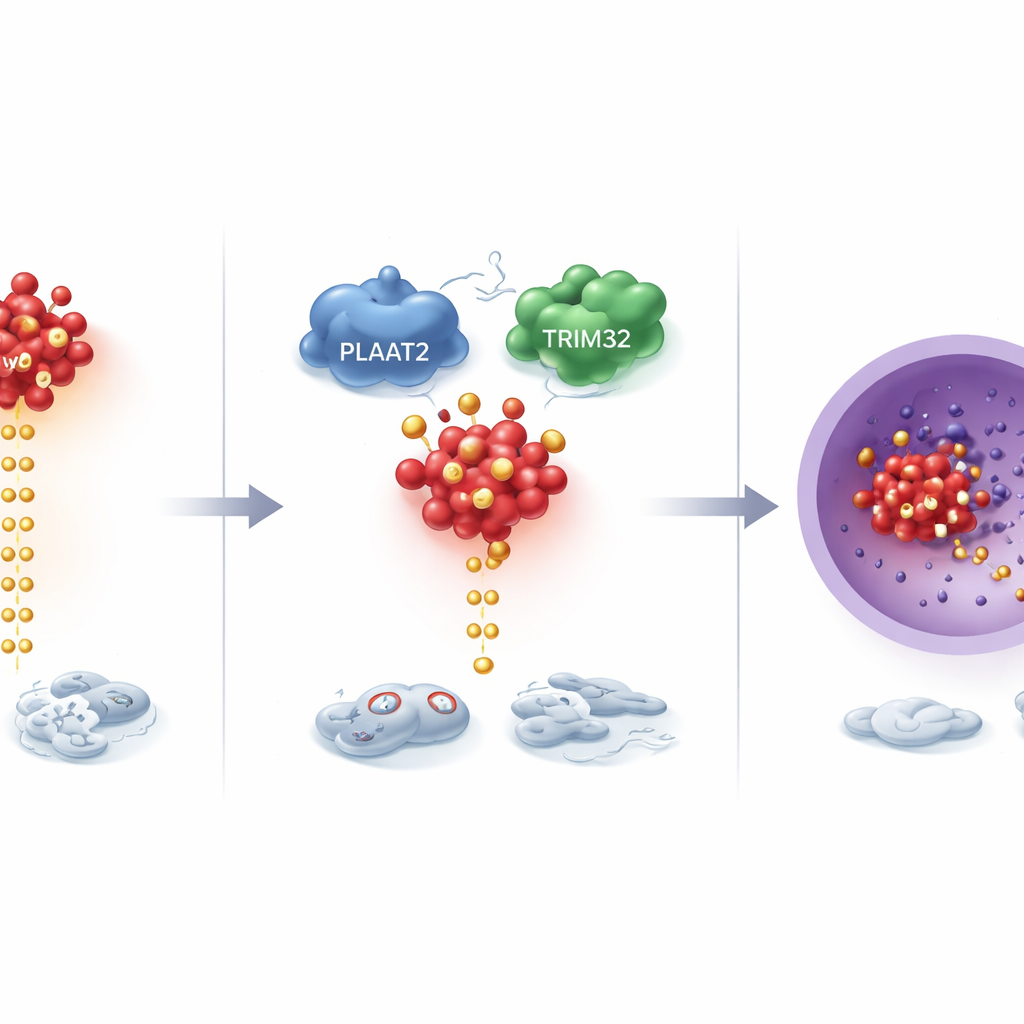
إخماد مسار إشاري كبير للسرطان
لأن cMyc يمكنه تنشيط سلسلة إشارات تشجع الخلايا على الانقسام والهجرة وتغيير الهوية، نظر الباحثون في أحد المسارات الرئيسية التي يتحكم بها، والمعروف بمسار MEK/ERK. عندما كانت مستويات PLAAT2 منخفضة، أصبح هذا المسار أكثر نشاطاً، وأظهرت الخلايا السرطانية خصائص عملية تسمى الانتقال الظهاري البطاني–اللحمي (EMT)، حيث تفقد الخلايا عادة المرتبطة فيما بينها وتصبح أكثر حركة وغزوًا. أعادت استعادة PLAAT2 هذه التغيرات إلى الوراء: هدأ مسار MEK/ERK، انخفضت علامات السلوك الغازي، وتصرفت الخلايا بأقل عدوانية. كان بإمكان حجب أو تعزيز cMyc مباشرةً أن يلغي آثار PLAAT2، مما يبرز أن هذا البروتين الواقي يعمل إلى حد كبير عن طريق ضبط cMyc والإشارات التي يرسلها.
ماذا يعني هذا للعلاجات المستقبلية
مجتمعين النتائج معاً، تشير الأدلة إلى أن PLAAT2 هو حاجز طبيعي مهم ضد سرطان المعدة، يساعد في استقطاب TRIM32 لنزع فائض cMyc ومن ثم إخماد مسار رئيسي للنمو والانتشار. عندما يُفقد PLAAT2 أو يُسكَت، تعمل إشارات cMyc وMEK/ERK بلا كبح، مما يسمح للأورام بالنمو والغزو بسهولة أكبر. من خلال تسليط الضوء على سلسلة PLAAT2–TRIM32–cMyc كنقطة تحكم حاسمة، تفتح الدراسة إمكانيات جديدة: قد تهدف العلاجات المستقبلية إلى استعادة PLAAT2، أو تعزيز عمل TRIM32 على cMyc، أو تقليد هذه عملية التحلل مباشرة لإبطاء أو إيقاف تقدم سرطان المعدة.
الاستشهاد: Chu, M., Shi, X., Shi, Z. et al. PLAAT2 suppresses gastric cancer progression by facilitating cMyc ubiquitination and inhibiting MEK/ERK signaling. Cell Death Dis 17, 314 (2026). https://doi.org/10.1038/s41419-026-08546-y
الكلمات المفتاحية: سرطان المعدة, PLAAT2, cMyc, يوبيكويتينية, إشارة MEK ERK