Clear Sky Science · de
PLAAT2 unterdrückt das Fortschreiten von Magenkrebs, indem es die Ubiquitinierung von cMyc fördert und die MEK/ERK-Signalgebung hemmt
Warum diese Studie für Magenkrebs wichtig ist
Magenkrebs bleibt eine der tödlichsten Krebserkrankungen weltweit, teilweise weil er häufig spät entdeckt wird und sich schnell ausbreiten kann. Diese Studie untersucht einen wenig bekannten körpereigenen Schutzfaktor, ein Protein namens PLAAT2, und zeigt, wie es dazu beiträgt, Magenkrebs in Schach zu halten. Indem sie aufdeckt, wie dieses Molekül wirkt und warum es in vielen Tumoren verloren geht, weist die Forschung auf eine neue Schwachstelle bei gastroösophagealen Tumoren hin, die künftige Medikamente angreifen könnten.
Ein fehlender Beschützer im Tumorgewebe
Um zu prüfen, ob PLAAT2 eine Rolle bei Magenkrebs spielt, verglichen die Forschenden Tumorproben mit benachbartem nicht-krebshaltem Gewebe von mehr als hundert Patienten sowie Daten aus großen öffentlichen Krebsdatenbanken. Sie fanden ein klares Muster: Die PLAAT2-Spiegel waren im Krebsgewebe deutlich niedriger als in gesunder Magenschleimhaut. Patienten, deren Tumoren besonders geringe Mengen an PLAAT2 aufwiesen, hatten tendenziell weiter fortgeschrittene Erkrankungen, mehr Lymphknotenbefall und eine schlechtere Gesamtüberlebensrate. Ähnliche Reduktionen zeigten sich bei Untersuchungen von Magenkrebszelllinien im Labor, was darauf hindeutet, dass der Verlust dieses Proteins ein häufiges Merkmal der Erkrankung ist.
Wie das Stilllegen und Wiederherstellen von PLAAT2 das Krebsverhalten verändert
Das Team testete anschließend, was passiert, wenn PLAAT2 in Krebszellen künstlich herunterreguliert oder erhöht wird. Wenn PLAAT2 ausgeschaltet wurde, wuchsen die Tumorzellen schneller, bildeten mehr Kolonien, bewegten sich leichter durch Labormembranen und unterlagen seltener dem programmierten Zelltod. Wurde PLAAT2 auf höhere Werte zurückgebracht, geschah das Gegenteil: Das Zellwachstum verlangsamte sich, Bewegung und Invasion nahmen ab, und mehr Zellen starben. Diese Veränderungen zeigten sich auch in Mäusen: Tumoren ohne PLAAT2 wuchsen größer, während Tumoren mit zusätzlichem PLAAT2 kleiner blieben, was bestätigt, dass dieses Molekül als echte Bremse des Krebsfortschritts wirkt.
Eine Wachstumsschaltung innerhalb der Zelle kurzschließen
Bei tiefer gehenden Untersuchungen entdeckten die Forschenden, dass PLAAT2 ein mächtiges Wachstumssteuerungsprotein namens cMyc kontrolliert, das in vielen Krebsarten ungewöhnlich aktiv ist. PLAAT2 veränderte nicht, wie viel cMyc produziert wird, sondern wie schnell cMyc abgebaut wird. Bei höherem PLAAT2 wurde cMyc schneller markiert und entfernt; bei geringerem PLAAT2 blieb cMyc länger erhalten und baute sich an. Dieser Abbauprozess beruht auf einem zellulären „Recycling“-System, bei dem kleine Molekülanhängsel signalisieren, welche Proteine zerstört werden sollen. Man fand, dass PLAAT2 hilft, cMyc mit TRIM32 zusammenzubringen, einem Enzym, das diese Anhängsel anbringt. TRIM32 setzt dann an zwei Schlüsselstellen spezifische Markierungen auf cMyc, wodurch es für den Abbau vorgesehen wird und seine wachstumsfördernde Aktivität gedämpft bleibt.
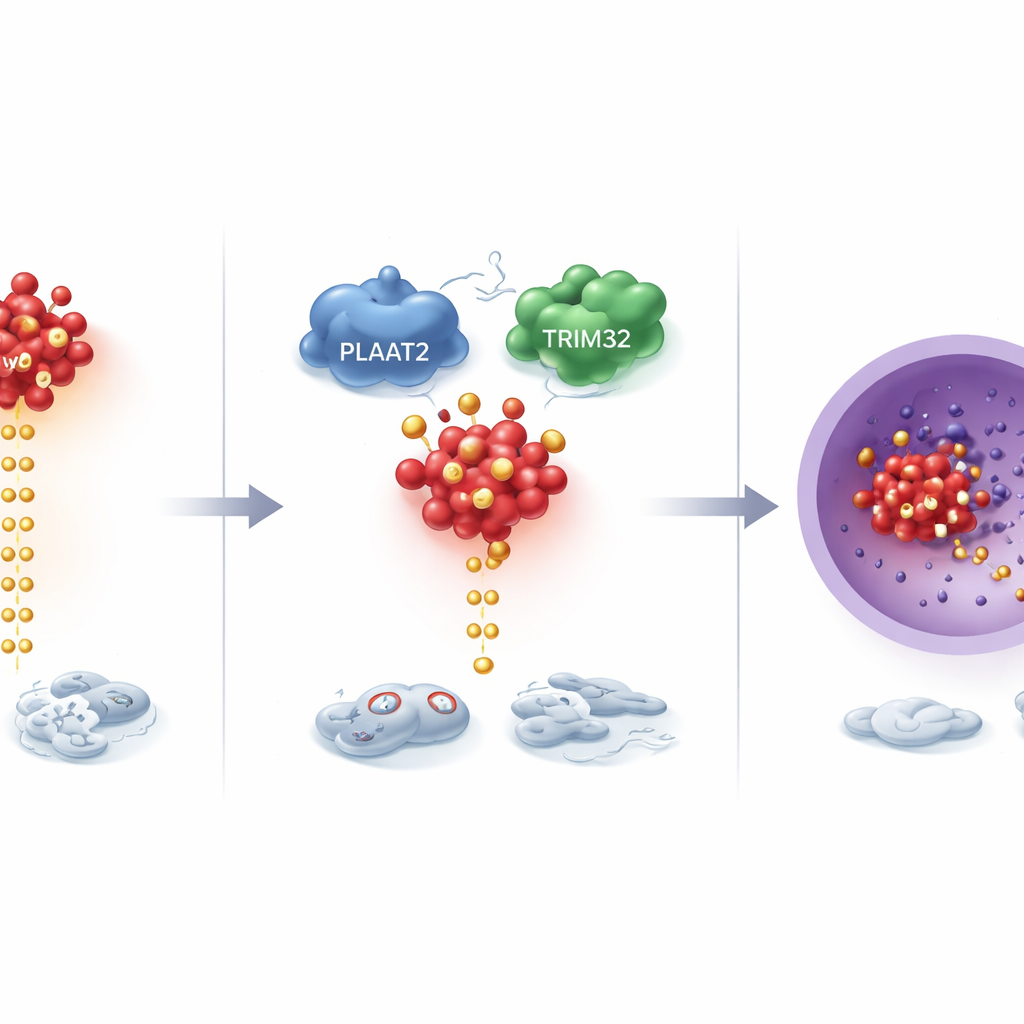
Abschwächung eines wichtigen krebsfördernden Signalwegs
Da cMyc eine Signalkette aktivieren kann, die Zellteilung, Migration und Identitätsveränderungen fördert, untersuchten die Forschenden einen wichtigen Weg, den es kontrolliert: den MEK/ERK-Pfad. Bei niedrigen PLAAT2-Spiegeln wurde dieser Pfad aktiver, und die Krebszellen zeigten Merkmale eines Prozesses namens epithelial–mesenchymale Transition, bei dem sich sonst gut vernetzte Zellen lockern und mobil und invasiv werden. Die Wiederherstellung von PLAAT2 kehrte diese Veränderungen um: Der MEK/ERK-Weg beruhigte sich, Marker invasiven Verhaltens sanken und die Zellen verhielten sich weniger aggressiv. Das gezielte Hemmen oder Verstärken von cMyc konnte die Effekte von PLAAT2 rückgängig machen, was unterstreicht, dass dieses schützende Protein hauptsächlich durch die Eindämmung von cMyc und dessen Signalwirkung wirkt.
Was das für zukünftige Therapien bedeutet
Zusammengefasst deuten die Ergebnisse darauf hin, dass PLAAT2 eine wichtige natürliche Schutzfunktion gegen Magenkrebs erfüllt, indem es TRIM32 anwirbt, um überschüssiges cMyc zu entfernen und dadurch einen zentralen Wachstums- und Ausbreitungsweg abzuschwächen. Geht PLAAT2 verloren oder wird es stillgelegt, laufen cMyc und die MEK/ERK-Signalgebung ungehindert, wodurch Tumoren leichter wachsen und in umliegendes Gewebe eindringen können. Indem die Studie die PLAAT2–TRIM32–cMyc-Kette als kritischen Kontrollpunkt hervorhebt, eröffnet sie neue Möglichkeiten: Zukünftige Therapien könnten darauf abzielen, PLAAT2 wiederherzustellen, die Wirkung von TRIM32 auf cMyc zu verstärken oder diesen Abbauprozess direkt nachzuahmen, um das Fortschreiten von Magenkrebs zu verlangsamen oder zu stoppen.
Zitation: Chu, M., Shi, X., Shi, Z. et al. PLAAT2 suppresses gastric cancer progression by facilitating cMyc ubiquitination and inhibiting MEK/ERK signaling. Cell Death Dis 17, 314 (2026). https://doi.org/10.1038/s41419-026-08546-y
Schlüsselwörter: Magenkrebs, PLAAT2, cMyc, Ubiquitinierung, MEK ERK Signalgebung