Clear Sky Science · sv
CCK2R reglerar METH‑inducerad inlärning av platspreferens inom VTA‑BLA‑BNST‑kretsen hos hanmöss
Varför detta har betydelse för människor och samhälle
Metamfetaminberoende förstör liv, och dagens behandlingar lyckas ofta inte släcka kraftiga sug eller förhindra återfall. Denna studie går djupt in i hjärnan för att hitta en specifik ”strömbrytare” som hjälper met att koppla drogens belönande effekter till platser och ledtrådar i omgivningen. Genom att peka ut denna strömbrytare i en precis kedja av hjärnregioner hos möss antyder arbetet nya, starkt riktade sätt att försvaga drogminnen och minska met‑dragningskraften, samtidigt som normal stämning och tänkande i stor utsträckning lämnas intakta. 
En hjärnväg som omvandlar kontext till åtrå
Forskarna fokuserade på en tredelad bana som kopplar viktiga belönings‑ och känslocentra: ventrala tegmentområdet (VTA), basolaterala amygdala (BLA) och bed nucleus of the stria terminalis (BNST). VTA innehåller dopaminfrisättande celler som signalerar belöning; BLA hjälper till att fästa känslomässig betydelse vid upplevelser; och BNST integrerar stress och motivation. När möss fick meth i ena kammaren i en tvådelad box föredrog de senare den sidan, ett klassiskt tecken på att drogens behag blivit knutet till platsen. Denna modell för betingad platspreferens gjorde det möjligt för teamet att följa hur aktiviteten i VTA–BLA–BNST‑kedjan förändrades när drogminnen bildades.
Ett matsmältningshormon som jobbar extra i hjärnan
Överraskande nog visade sig en molekyl mest känd från tarmen—kolecystokinin (CCK)—vara central. I hjärnan frisätter vissa dopaminceller i VTA även CCK. Forskarna använde genetiskt modifierade möss för att ta bort CCK enbart från dessa celler. Utan CCK utvecklade mössen inte längre en stark preferens för meth‑parade kammaren, och den vanliga meth‑drivna ökningen i VTA‑cellernas fyrningsaktivitet dämpades. Ändå uppträdde dessa möss normalt i tester av rörelse, minne, ångest och depressionsliknande beteenden. Det tyder på att VTA‑CCK inte krävs för vardaglig hjärnfunktion, men är avgörande när meth försöker etablera ett starkt belöningsminne.
En enda receptor som en kritisk grind i amygdala
CCK verkar genom att binda till receptorer på andra neuroner, och författarna fann att en av dem, kallad CCK2R, blir särskilt rikligt uttryckt i BLA efter meth‑exponering. När de tog bort CCK2R specifikt från BLA:s exciterande celler kunde meth inte längre skapa stark platspreferens, och den onormala burst‑aktiviteten i dessa celler normaliserades till stor del. Finkorniga inspelningar visade att meth vanligtvis förstärker exciterande synaptiska kontakter och små utskott kallade dendritiska spines i BLA—förändringar kopplade till starkare, mer långvariga minnen. Att ta bort CCK2R förhindrade dessa strukturella och elektriska förändringar, samtidigt som allmän inlärning och sinnestillstånd åter förblev opåverkade.
Att föra vidare signalen till ett stresscentrum
Berättelsen slutade inte i amygdala. Med sofistikerad viral spårning visade forskarna att VTA‑dopaminceller matar in till BLA:s exciterande celler, som i sin tur projicerar till BNST, en region kopplad till ångest och beroende. Att tysta denna VTA–BLA–BNST‑kedja under meth‑träningen minskade kraftigt platspreferensen och lugnade de överaktiva BNST‑neuronerna. Avgörande var att utslagning av CCK2R endast i den delmängd av BLA‑celler som både tar emot VTA‑input och skickar signaler till BNST blockerade meths effekter på BNST‑aktivitet, synaptisk förstärkning och tillväxt av dendritiska spines. Kretsar som inte projicerade till BNST påverkades mycket mindre, vilket understryker hur precist CCK2R‑"strömbrytaren" är kopplad. 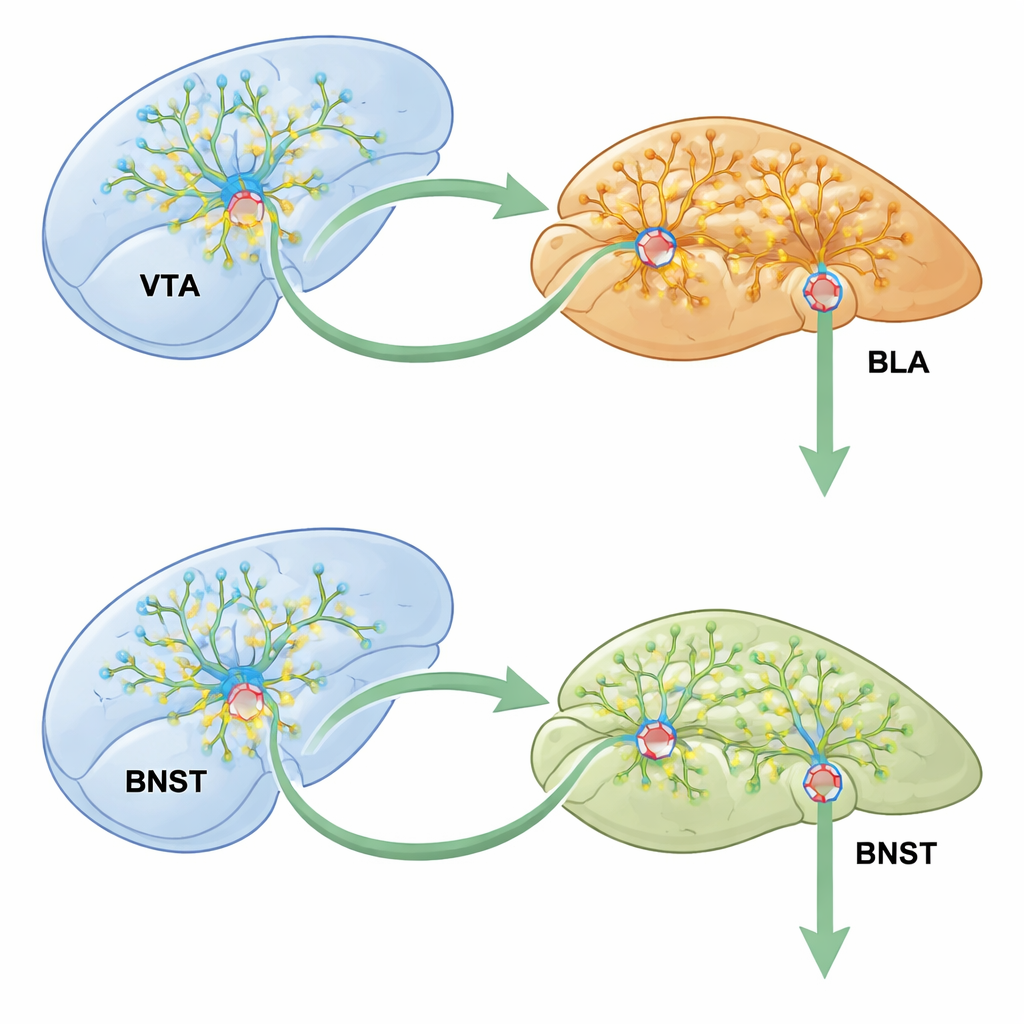
Vad detta kan innebära för framtida behandling
Sammantaget visar studien att meth kapar ett specifikt tarm‑till‑hjärna‑signalsystem—CCK som verkar på CCK2R—inom en definierad VTA–BLA–BNST‑bana för att hårdna drogrelaterade minnen och driva preferens för drogassocierade platser. Att stänga av CCK2R i denna krets suddade ut många kännetecken för beroende hos mössen, från förhöjd neuronfyrning till extra synapser och förändrade hjärnrytmiska mönster, utan att i stort rubba känsloliv eller kognition. För en lekman betyder det att forskarna identifierat en mycket selektiv "kretsspärr" för metamfetaminbelöning. Läkemedel som säkert blockerar CCK2R i rätt hjärnvägar skulle en dag kunna hjälpa till att försvaga met‑sug och minska återfallsrisken, och därigenom erbjuda en mer målinriktad terapi än dagens metoder.
Citering: Wang, J., Zhang, M., Qiao, L. et al. CCK2R regulates METH-induced CPP acquisition within VTA-BLA-BNST circuit in male mice. Transl Psychiatry 16, 210 (2026). https://doi.org/10.1038/s41398-026-03982-y
Nyckelord: amfetaminberoende, hjärnans belöningskretsar, kolecystokinin, amygdala och BNST, drogsminne