Clear Sky Science · de
CCK2R reguliert die mit Meth induzierte CPP-Akquisition innerhalb des VTA–BLA–BNST-Kreises bei männlichen Mäusen
Warum das für Menschen und die Gesellschaft wichtig ist
Methamphetamin‑Abhängigkeit zerstört Leben, und aktuelle Behandlungen scheitern oft daran, starke Verlangen und Rückfälle zu verhindern. Diese Studie blickt tief ins Gehirn und identifiziert einen spezifischen „Schalter“, der Meth dabei hilft, angenehme Drogeneffekte mit Orten und Hinweisen in der Umgebung zu verknüpfen. Indem die Forschenden diesen Schalter in einer präzisen Kette von Hirnregionen bei Mäusen lokalisieren, legen die Ergebnisse nahe, dass sich neue, sehr gezielte Wege eröffnen, Drogen‑Gedächtnisse zu schwächen und die Anziehungskraft von Meth zu reduzieren, während normale Stimmung und kognitive Funktionen weitgehend unbeeinflusst bleiben. 
Ein Hirnweg, der Kontext in Verlangen verwandelt
Die Forschenden konzentrierten sich auf einen dreistufigen Weg, der zentrale Belohnungs‑ und Emotionszentren verbindet: das ventrale tegmentale Areal (VTA), die basolaterale Amygdala (BLA) und den Nucleus bed nucleus of the stria terminalis (BNST). Das VTA enthält dopaminfreisetzende Zellen, die Belohnung signalisieren; die BLA hilft, Erfahrungen emotional zu bewerten; und der BNST integriert Stress und Motivation. Bekamen Mäuse Meth in einer Kammer eines Zwei‑Raum‑Behälters, zogen sie später diese Seite vor — ein klassisches Zeichen dafür, dass die angenehmen Effekte der Droge an diesen Ort gebunden wurden. Dieses Modell der konditionierten Platzpräferenz erlaubte es dem Team, zu verfolgen, wie sich die Aktivität entlang der VTA–BLA–BNST‑Kette veränderte, während Drogen‑Gedächtnisse entstanden.
Ein Verdauungshormon mit Nebenjob im Gehirn
Überraschenderweise erwies sich ein Molekül, das vor allem aus dem Darm bekannt ist — Cholezystokinin (CCK) — als zentral. Im Gehirn setzen bestimmte VTA‑Dopaminneurone ebenfalls CCK frei. Das Team nutzte genetisch veränderte Mäuse, um CCK nur in diesen Zellen gezielt zu entfernen. Ohne CCK entwickelten die Mäuse keine ausgeprägte Präferenz mehr für die mit Meth verknüpfte Kammer, und die übliche meth‑bedingte Zunahme der VTA‑Feuerungsrate war abgeschwächt. Dennoch zeigten diese Tiere normale Verhaltensweisen in Tests zu Bewegung, Gedächtnis, Angst und depressionsähnlichem Verhalten. Das deutet darauf hin, dass VTA‑CCK für alltägliche Gehirnfunktionen nicht nötig ist, wohl aber eine Schlüsselrolle spielt, wenn Meth versucht, ein starkes Belohnungs‑Gedächtnis zu verankern.
Ein einzelner Rezeptor als kritisches Tor in der Amygdala
CCK wirkt, indem es an Rezeptoren auf anderen Neuronen bindet, und die Autoren fanden heraus, dass einer dieser Rezeptoren, CCK2R, nach Meth‑Exposition in der BLA besonders stark hochreguliert ist. Löschten sie CCK2R gezielt aus den exzitatorischen Zellen der BLA, konnte Meth keine starke Platzpräferenz mehr erzeugen, und der auffällige Aktivitätsausbruch in diesen Zellen normalisierte sich größtenteils. Feinelektrophysiologische Aufzeichnungen zeigten, dass Meth normalerweise exzitatorische Verbindungen und winzige Ausstülpungen, sogenannte dendritische Dornen, in der BLA verstärkt — Veränderungen, die mit stärkeren und länger anhaltenden Gedächtnissen verknüpft sind. Das Entfernen von CCK2R verhinderte diese strukturellen und elektrischen Umstellungen, während allgemeines Lernen und Stimmung wiederum unbeeinträchtigt blieben.
Das Signal reicht bis zu einem Stresszentrum
Die Geschichte endete nicht in der Amygdala. Mittels ausgefeilter viraler Tracing‑Methoden zeigten die Forschenden, dass VTA‑Dopaminneurone auf exzitatorische Zellen der BLA einwirken, die wiederum zum BNST projizieren — einer Region, die mit Angst und Sucht verbunden ist. Das Stummschalten dieser VTA–BLA–BNST‑Kette während des Meth‑Trainings verringerte die Platzpräferenz deutlich und beruhigte die überaktiven BNST‑Neurone. Entscheidend war: Das Entfernen von CCK2R nur in jener Untergruppe von BLA‑Zellen, die sowohl VTA‑Input erhalten als auch Signale an den BNST senden, blockierte Meths Effekte auf die BNST‑Aktivität, die synaptische Verstärkung und das Wachstum dendritischer Dornen. Schaltungen, die nicht zum BNST führten, waren deutlich weniger betroffen, was unterstreicht, wie präzise der CCK2R‑„Schalter“ verdrahtet ist. 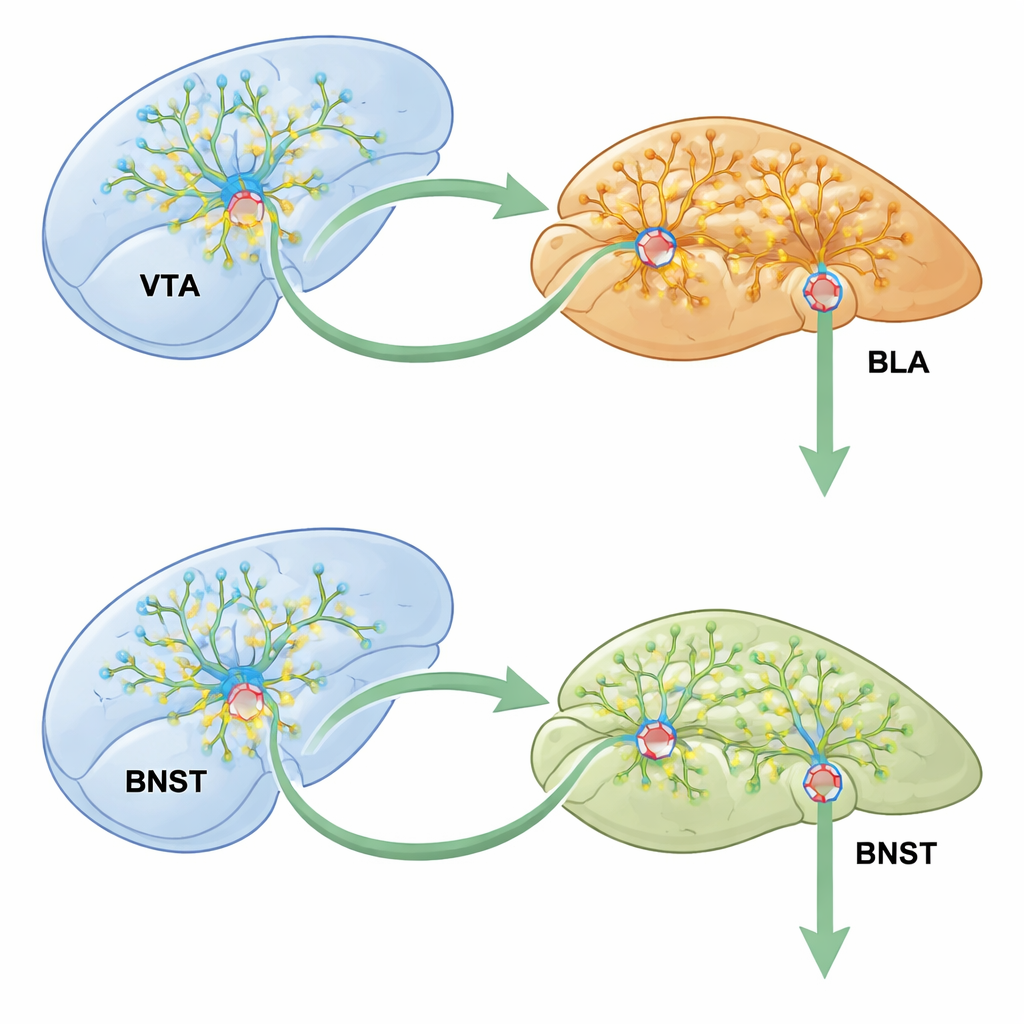
Was das für künftige Therapien bedeuten könnte
Insgesamt zeigt die Studie, dass Meth ein spezifisches Darm‑Gehirn‑Botensystem kapert — CCK, das auf CCK2R wirkt — innerhalb eines klar definierten VTA–BLA–BNST‑Pfads, um drogenbezogene Gedächtnisse zu verhärten und die Präferenz für drogenassoziierte Orte zu steigern. Das Abschalten von CCK2R in diesem Schaltkreis beseitigte viele Kennzeichen der Sucht bei den Mäusen — von verstärkter Neuronenfeuerung über zusätzliche Synapsen bis hin zu veränderten Hirnrhythmusmustern — ohne breit die Emotionen oder kognitive Funktionen zu stören. Für Laien bedeutet das: Forschende haben einen sehr selektiven „Leistungsschalter“ für Meth‑Belohnung identifiziert. Wirkstoffe, die CCK2R sicher in den richtigen Hirnwegen blockieren, könnten eines Tages helfen, Meth‑Verlangen und Rückfallrisiko zu schwächen und damit eine fokussiertere Therapie bieten als heutige Ansätze.
Zitation: Wang, J., Zhang, M., Qiao, L. et al. CCK2R regulates METH-induced CPP acquisition within VTA-BLA-BNST circuit in male mice. Transl Psychiatry 16, 210 (2026). https://doi.org/10.1038/s41398-026-03982-y
Schlüsselwörter: Methamphetamin-Abhängigkeit, Belohnungsnetzwerke im Gehirn, Cholezystokinin, Amygdala und BNST, Drogen‑Gedächtnis