Clear Sky Science · nl
CCK2R reguleert METH-geïnduceerde CPP-acquisitie binnen het VTA-BLA-BNST-circuit bij mannelijke muizen
Waarom dit ertoe doet voor mensen en de samenleving
Verslaving aan methamfetamine verwoest levens, maar de huidige behandelingen slagen er vaak niet in om krachtige cravings en terugval te stoppen. Deze studie kijkt diep in de hersenen om een specifiek “schakelaartje” te vinden dat meth helpt om plezierige drugs-effecten te koppelen aan plaatsen en signalen in de omgeving. Door dit schakelaartje te lokaliseren in een nauwkeurige keten van hersengebieden bij muizen, suggereert het werk nieuwe, zeer doelgerichte manieren om druggerelateerde herinneringen te verzwakken en de aantrekkingskracht van meth te verminderen, terwijl normale stemming en denkprocessen grotendeels onaangetast blijven. 
Een hersenpad dat context in craving omzet
De onderzoekers concentreerden zich op een drie-stappenpad dat sleutelcentra voor beloning en emotie verbindt: het ventrale tegmentale gebied (VTA), de basolaterale amygdala (BLA) en de bed nucleus of the stria terminalis (BNST). De VTA bevat dopamine-afgevende cellen die beloning signaleren; de BLA helpt emotionele waarde aan ervaringen te koppelen; en de BNST integreert stress en motivatie. Wanneer muizen meth kregen in één gedeelte van een twee-kamer doos, gaven ze later de voorkeur aan die zijde — een klassiek teken dat de plezierige effecten van de drug aan die plaats zijn gekoppeld. Dit model van conditioneerde plaatsvoorkeur stelde het team in staat te volgen hoe de activiteit in de VTA–BLA–BNST-keten veranderde terwijl drugherinneringen gevormd werden.
Een spijsverteringshormoon met een nevenfunctie in de hersenen
Verrassend genoeg bleek een molecuul dat vooral bekend is uit de darmen — cholecystokinine (CCK) — centraal te staan. In de hersenen scheiden bepaalde VTA-dopaminecellen ook CCK uit. Het team gebruikte genetisch gemodificeerde muizen om CCK alleen uit deze cellen te verwijderen. Zonder CCK ontwikkelden muizen geen sterke voorkeur meer voor de met meth geassocieerde kamer, en de gebruikelijke door meth veroorzaakte toename in VTA-vuursnelheid was afgezwakt. Toch gedroegen deze muizen zich normaal in tests voor beweging, geheugen, angst en depressieachtig gedrag. Dit suggereert dat VTA-CCK niet nodig is voor alledaagse hersenfuncties, maar wel cruciaal is wanneer meth probeert een krachtige beloningsherinnering te verankeren.
Een enkele receptor als kritieke poort in de amygdala
CCK werkt door te binden aan receptoren op andere neuronen, en de auteurs vonden dat één daarvan, CCK2R genoemd, bijzonder overvloedig wordt in de BLA na methblootstelling. Toen ze CCK2R specifiek verwijderden uit de exciterende cellen van de BLA, kon meth geen sterke plaatsvoorkeur meer creëren en normaliseerde de abnormale activiteitspiek in deze cellen grotendeels. Fijne-opnames toonden dat meth gewoonlijk exciterende verbindingen en kleine uitsteeksels die dendritische spines heten in de BLA versterkt — veranderingen die gekoppeld zijn aan sterkere, langduriger herinneringen. Het verwijderen van CCK2R verhinderde deze structurele en elektrische verschuivingen, terwijl algemeen leren en stemming opnieuw onaangetast bleven.
Het signaal uitbreiden naar een stresscentrum
Het verhaal eindigde niet in de amygdala. Met behulp van verfijnde virale tracing toonden de onderzoekers aan dat VTA-dopaminecellen verbindingen maken met exciterende BLA-cellen, die op hun beurt projecteren naar de BNST, een regio die samenhangt met angst en verslaving. Het stilleggen van deze VTA–BLA–BNST-keten tijdens meth-training verminderde de plaatsvoorkeur sterk en kalmeerde de overactieve BNST-cellen. Cruciaal was dat het uitschakelen van CCK2R alleen in de subset van BLA-cellen die zowel VTA-input ontvangen als signalen naar de BNST sturen, de effecten van meth op BNST-activiteit, synaptische versterking en groei van dendritische spines blokkeerde. Circuits die niet naar de BNST leidden, werden veel minder beïnvloed, wat benadrukt hoe precies de CCK2R-“schakelaar” is bedraad. 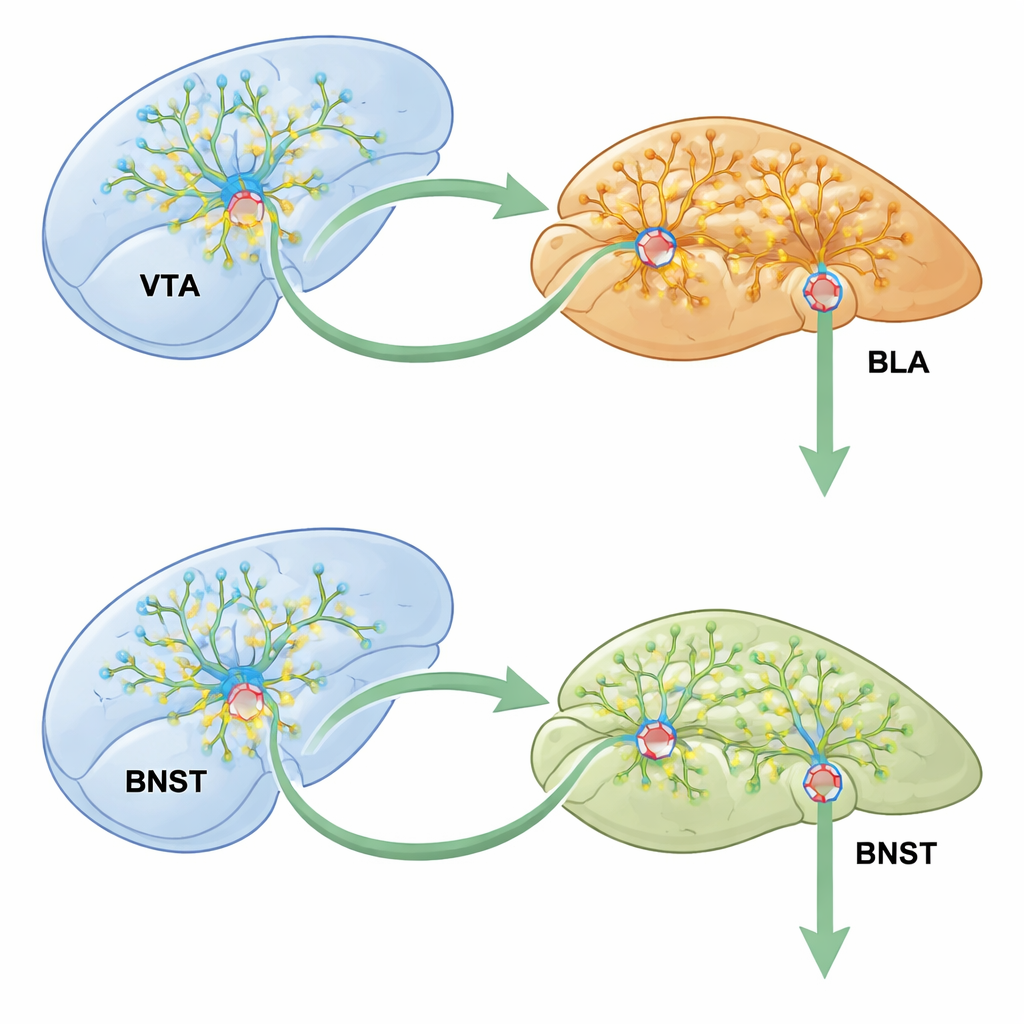
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar laat de studie zien dat meth een specifiek buik–hersen boodschappersysteem kapert — CCK dat werkt via CCK2R — binnen een gedefinieerd VTA–BLA–BNST-pad om druggerelateerde herinneringen te versterken en de voorkeur voor drugsgeassocieerde plaatsen aan te jagen. Het uitschakelen van CCK2R in dit circuit wist veel kenmerken van verslaving bij de muizen uit, van verhoogde neuronale vuurfreqenties tot extra synapsen en veranderde hersengolven, zonder breed emoties of cognitie te verstoren. Voor een leek betekent dit dat wetenschappers een zeer selectieve “stroomonderbreker” voor meth-beloning hebben geïdentificeerd. Medicijnen die veilig CCK2R blokkeren in de juiste hersenbanen zouden op termijn kunnen helpen om meth-cravings en terugvalrisico te verzwakken en zo een gerichtere therapie bieden dan de huidige benaderingen.
Bronvermelding: Wang, J., Zhang, M., Qiao, L. et al. CCK2R regulates METH-induced CPP acquisition within VTA-BLA-BNST circuit in male mice. Transl Psychiatry 16, 210 (2026). https://doi.org/10.1038/s41398-026-03982-y
Trefwoorden: methamfetamineverslaving, hersenbeloningscircuits, cholecystokinine, amygdala en BNST, drugsherinnering