Clear Sky Science · pl
CCK2R reguluje pozyskiwanie CPP wywołanego METH w obwodzie VTA-BLA-BNST u samców myszy
Dlaczego ma to znaczenie dla ludzi i społeczeństwa
Uzależnienie od metamfetaminy rozbija życie ludzi, a obecne terapie często nie powstrzymują silnych głodów narkotykowych ani nawrotów. To badanie zagląda głęboko do mózgu, by odnaleźć konkretny „przełącznik”, który pomaga metamfetaminie powiązać przyjemne efekty leku z miejscami i sygnałami w otoczeniu. Wskazując ten przełącznik w precyzyjnym łańcuchu regionów mózgu u myszy, praca sugeruje nowe, bardzo ukierunkowane sposoby osłabiania pamięci narkotykowej i zmniejszania siły przyciągania metamfetaminy, przy jednoczesnym zachowaniu normalnego nastroju i funkcji poznawczych w dużej mierze nienaruszonych. 
Szlak mózgowy, który zamienia kontekst w głód
Naukowcy skupili się na trzyetapowym szlaku łączącym kluczowe ośrodki nagrody i emocji: brzuszną nakrywkę (VTA), amygdalę podstawno-boczną (BLA) oraz jądro pasma przykomorowego (BNST). VTA zawiera neurony wydzielające dopaminę, które sygnalizują nagrodę; BLA pomaga przypisywać doświadczeniom wartość emocjonalną; a BNST integruje stres i motywację. Gdy myszy otrzymywały metamfetaminę w jednej komorze dwu-komorowego pudełka, później wolały tę stronę — klasyczny znak, że przyjemne efekty leku zostały powiązane z miejscem. Model „warunkowanej preferencji miejsca” pozwolił zespołowi śledzić, jak zmienia się aktywność w łańcuchu VTA–BLA–BNST w trakcie formowania pamięci narkotykowej.
Hormon trawienny pełniący funkcję w mózgu
Co zaskakujące, cząsteczka znana przede wszystkim z układu pokarmowego — cholecystokinina (CCK) — okazała się centralna. W mózgu niektóre neurony dopaminergiczne VTA także uwalniają CCK. Zespół użył genetycznie zmodyfikowanych myszy, aby usunąć CCK tylko z tych komórek. Bez CCK myszy nie rozwijały już silnej preferencji dla komory powiązanej z metamfetaminą, a zwykły napływ aktywności komórek VTA wywołany METH był osłabiony. Jednak te myszy zachowywały się normalnie w testach ruchu, pamięci oraz zachowań lękowych i depresyjnych. Sugeruje to, że CCK w VTA nie jest potrzebna do codziennego funkcjonowania mózgu, ale jest kluczowa, gdy metamfetamina stara się utrwalić silną pamięć nagrody.
Pojedynczy receptor jako krytyczna bramka w amygdali
CCK działa przez wiązanie się z receptorami na innych neuronach, a autorzy odkryli, że jeden z nich, zwany CCK2R, staje się szczególnie obfity w BLA po ekspozycji na METH. Gdy usunęli CCK2R specyficznie z komórek pobudzeniowych BLA, metamfetamina nie była już w stanie wywołać silnej preferencji miejsca, a nietypowy wysoki impuls aktywności w tych komórkach został w dużej mierze znormalizowany. Nagrania wysokiej rozdzielczości wykazały, że METH zwykle wzmacnia połączenia pobudzające i małe wyrostki zwane kolcami dendrytycznymi w BLA — zmiany powiązane z silniejszymi, długotrwałymi pamięciami. Usunięcie CCK2R zapobiegło tym strukturalnym i elektrycznym przesunięciom, pozostawiając jednocześnie ogólne uczenie się i nastrój nietknięte.
Rozszerzenie sygnału do ośrodka stresu
Historia nie kończy się w amygdali. Dzięki zaawansowanemu znakowaniu wirusowemu badacze wykazali, że neurony dopaminergiczne VTA zasilają komórki pobudzeniowe BLA, które z kolei projektują się do BNST, regionu powiązanego z lękiem i uzależnieniem. Wyciszenie łańcucha VTA–BLA–BNST podczas treningu z METH znacząco zmniejszyło preferencję miejsca i uspokoiło nadaktywne neurony BNST. Co kluczowe, wyłączenie CCK2R tylko w podzbiorze komórek BLA, które zarówno otrzymują wejście z VTA, jak i wysyłają sygnały do BNST, zablokowało efekty METH na aktywność BNST, wzmocnienie synaptyczne i wzrost kolców dendrytycznych. Obwody, które nie kierowały się do BNST, były znacznie mniej dotknięte, co podkreśla, jak precyzyjnie jest okablowany „przełącznik” CCK2R. 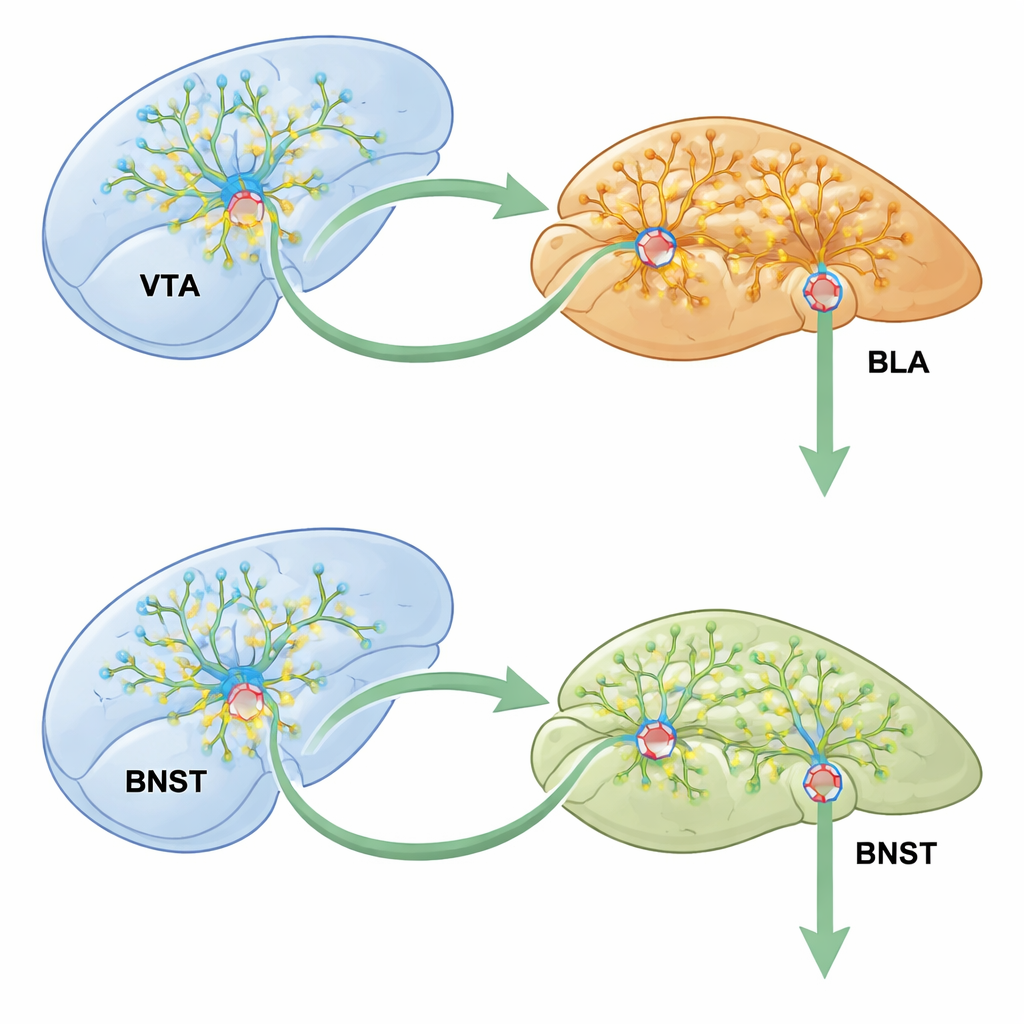
Co to może oznaczać dla przyszłego leczenia
Ogólnie badanie pokazuje, że METH przywłaszcza sobie specyficzny sygnał jelitowo-mózgowy — CCK działającą na CCK2R — w określonym szlaku VTA–BLA–BNST, aby utrwalić pamięci związane z narkotykiem i napędzać preferencję miejsc powiązanych z lekiem. Wyłączenie CCK2R w tym obwodzie wymazało wiele cech uzależnienia u myszy, od zwiększonej aktywności neuronów po dodatkowe synapsy i zmienione rytmy mózgowe, bez szerokiego zaburzania emocji czy poznania. Dla laika oznacza to, że naukowcy zidentyfikowali bardzo selektywny "wyłącznik obwodu" dla nagrody wywołanej METH. Leki, które bezpiecznie blokowałyby CCK2R w odpowiednich ścieżkach mózgu, mogłyby kiedyś pomóc osłabić głód po METH i ryzyko nawrotu, oferując bardziej ukierunkowaną terapię niż obecne podejścia.
Cytowanie: Wang, J., Zhang, M., Qiao, L. et al. CCK2R regulates METH-induced CPP acquisition within VTA-BLA-BNST circuit in male mice. Transl Psychiatry 16, 210 (2026). https://doi.org/10.1038/s41398-026-03982-y
Słowa kluczowe: uzależnienie od metamfetaminy, obwody nagrody w mózgu, cholecystokinina, amygdala i BNST, pamięć związana z narkotykami