Clear Sky Science · es
CCK2R regula la adquisición de CPP inducida por METH dentro del circuito VTA-BLA-BNST en ratones machos
Por qué esto importa para las personas y la sociedad
La adicción a la metanfetamina destroza vidas, y los tratamientos actuales a menudo no logran frenar los ansias intensas ni las recaídas. Este estudio explora a fondo el cerebro para encontrar un “interruptor” específico que ayuda a vincular los efectos placenteros de la metanfetamina con lugares y señales del entorno. Al localizar este interruptor en una cadena concreta de regiones cerebrales en ratones, el trabajo sugiere maneras nuevas y muy focalizadas de debilitar las memorias de la droga y reducir el poder de atracción de la metanfetamina, dejando en gran medida intacto el estado de ánimo y el pensamiento normales. 
Una vía cerebral que convierte el contexto en ansia
Los investigadores se centraron en una vía de tres pasos que conecta centros clave de recompensa y emoción: la área tegmental ventral (VTA), la amígdala basolateral (BLA) y el núcleo de la cama de la estría terminalis (BNST). La VTA contiene neuronas que liberan dopamina y señalan recompensa; la BLA ayuda a asignar valor emocional a las experiencias; y el BNST integra estrés y motivación. Cuando los ratones recibieron metanfetamina en una cámara de una caja de dos compartimentos, luego prefirieron ese lado, un signo clásico de que los efectos placenteros de la droga se habían asociado con ese lugar. Este modelo de “preferencia condicionada de lugar” permitió al equipo seguir cómo cambiaba la actividad en la cadena VTA–BLA–BNST conforme se formaban las memorias de la droga.
Una hormona digestiva que trabaja en el cerebro
Sorprendentemente, una molécula más conocida por su papel en el intestino —la colecistoquinina (CCK)— resultó ser central. En el cerebro, ciertas neuronas dopaminérgicas de la VTA también liberan CCK. El equipo usó ratones genéticamente modificados para eliminar la CCK únicamente de estas células. Sin CCK, los ratones ya no desarrollaron una fuerte preferencia por la cámara emparejada con metanfetamina, y el aumento habitual de disparo de las células de la VTA inducido por la droga se atenuó. Aun así, esos ratones se comportaron con normalidad en pruebas de movimiento, memoria, ansiedad y conductas parecidas a la depresión. Esto sugiere que la CCK de la VTA no es necesaria para las funciones cerebrales cotidianas, pero sí es crucial cuando la metanfetamina intenta consolidar una memoria de recompensa potente.
Un único receptor como puerta crítica en la amígdala
La CCK actúa uniéndose a receptores en otras neuronas, y los autores encontraron que uno de ellos, llamado CCK2R, se vuelve especialmente abundante en la BLA tras la exposición a metanfetamina. Cuando eliminaron CCK2R específicamente de las células excitadoras de la BLA, la metanfetamina ya no pudo crear una fuerte preferencia de lugar, y el estallido anómalo de actividad en esas células se normalizó en gran medida. Registros a escala fina mostraron que la metanfetamina normalmente potencia las conexiones excitatorias y pequeñas protuberancias llamadas espinas dendríticas en la BLA —cambios vinculados a memorias más fuertes y duraderas. Eliminar CCK2R previno estos cambios estructurales y eléctricos, nuevamente sin afectar el aprendizaje general ni el estado de ánimo.
Extendiendo la señal a un centro del estrés
La historia no terminó en la amígdala. Usando trazado viral sofisticado, los investigadores mostraron que las neuronas dopaminérgicas de la VTA alimentan a las células excitadoras de la BLA, que a su vez proyectan al BNST, una región ligada a la ansiedad y la adicción. Silenciar esta cadena VTA–BLA–BNST durante el entrenamiento con metanfetamina redujo drásticamente la preferencia de lugar y calmó las neuronas hiperactivas del BNST. De forma crucial, eliminar CCK2R únicamente en el subconjunto de células de la BLA que reciben entrada de la VTA y envían señales al BNST bloqueó los efectos de la metanfetamina sobre la actividad del BNST, el fortalecimiento sináptico y el crecimiento de espinas dendríticas. Los circuitos que no proyectaban al BNST se vieron mucho menos afectados, subrayando lo precisamente cableado que está el “interruptor” CCK2R. 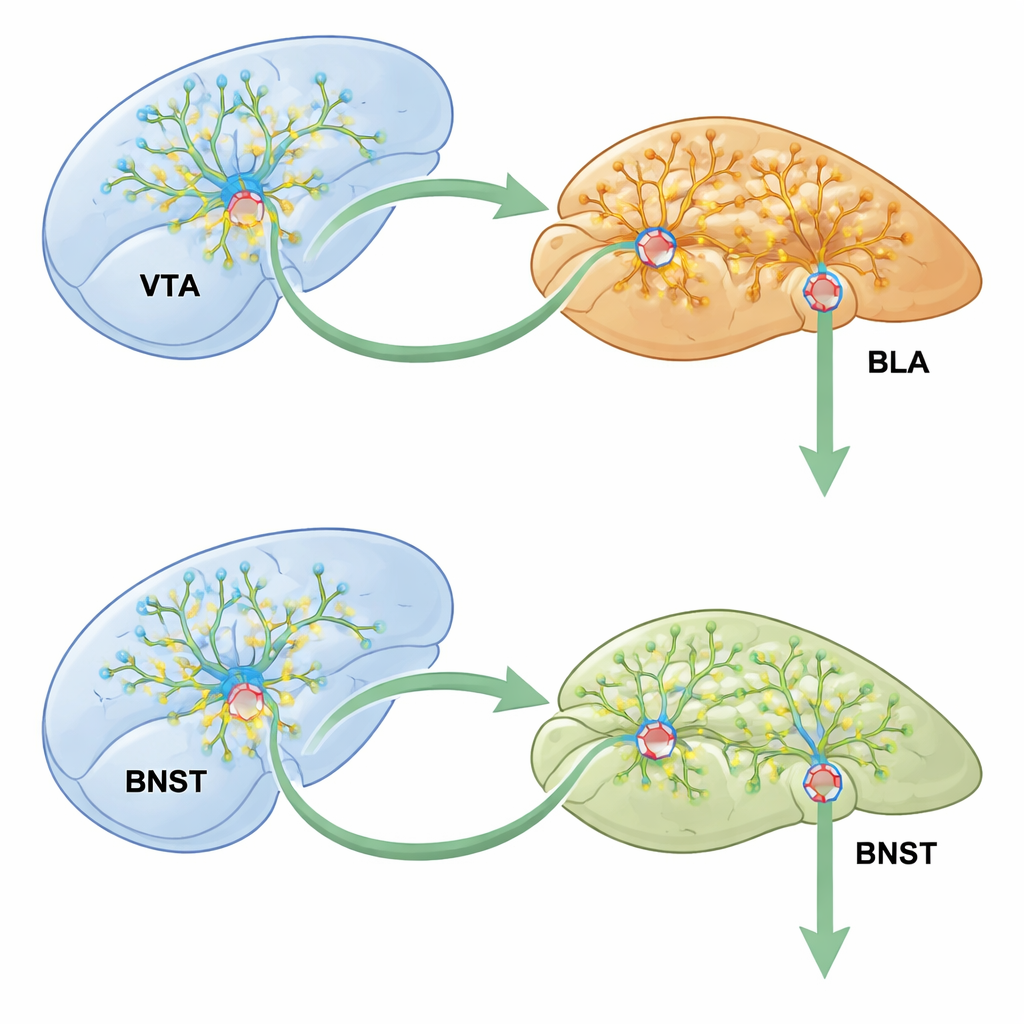
Qué podría significar esto para tratamientos futuros
En conjunto, el estudio muestra que la metanfetamina secuestra un sistema mensajero específico intestino–cerebro —la CCK actuando sobre CCK2R— dentro de una vía definida VTA–BLA–BNST para endurecer las memorias relacionadas con la droga y promover la preferencia por lugares asociados a la droga. Desactivar CCK2R en este circuito borró muchas señas de la adicción en los ratones, desde el aumento del disparo neuronal hasta sinapsis extras y ritmos cerebrales alterados, sin perturbar de manera general las emociones o la cognición. Para un lector no especializado, esto significa que los científicos han identificado un “interruptor de circuito” muy selectivo para la recompensa por metanfetamina. Fármacos que bloqueen de forma segura CCK2R en las vías cerebrales adecuadas podrían algún día ayudar a debilitar los antojos de metanfetamina y el riesgo de recaída, ofreciendo una terapia más focalizada que los enfoques actuales.
Cita: Wang, J., Zhang, M., Qiao, L. et al. CCK2R regulates METH-induced CPP acquisition within VTA-BLA-BNST circuit in male mice. Transl Psychiatry 16, 210 (2026). https://doi.org/10.1038/s41398-026-03982-y
Palabras clave: adicción a la metanfetamina, circuitos cerebrales de recompensa, colecistoquinina, amígdala y BNST, memoria de drogas