Clear Sky Science · fr
CCK2R régule l’acquisition de la CPP induite par la METH au sein du circuit VTA-BLA-BNST chez la souris mâle
Pourquoi cela compte pour les individus et la société
L’addiction à la méthamphétamine détruit des vies, et les traitements actuels peinent souvent à empêcher les envies puissantes et les rechutes. Cette étude explore en profondeur le cerveau pour identifier un « interrupteur » précis qui permet à la meth d’associer ses effets plaisants aux lieux et aux indices environnementaux. En localisant cet interrupteur dans une chaîne précise de régions cérébrales chez la souris, le travail suggère des approches très ciblées pour affaiblir les mémoires liées à la drogue et réduire l’attraction pour la meth, tout en épargnant en grande partie l’humeur et les fonctions cognitives normales. 
Un circuit cérébral qui transforme le contexte en envie
Les chercheurs se sont concentrés sur une voie en trois étapes reliant des centres clés de la récompense et des émotions : l’aire tegmentale ventrale (VTA), l’amygdale basolatérale (BLA) et le noyau du lit de la strie terminale (BNST). La VTA contient des neurones dopaminergiques qui signalent la récompense ; la BLA aide à attribuer une valeur émotionnelle aux expériences ; et le BNST intègre stress et motivation. Lorsque des souris recevaient de la meth dans une chambre d’une boîte à deux compartiments, elles préféraient ensuite ce côté, signe classique que les effets agréables de la drogue se sont liés à ce lieu. Ce modèle de « préférence de lieu conditionnée » a permis à l’équipe de suivre comment l’activité dans la chaîne VTA–BLA–BNST évoluait lors de la formation des souvenirs liés à la drogue.
Une hormone digestive qui joue un rôle dans le cerveau
De manière surprenante, une molécule surtout connue au niveau intestinal — la cholécystokinine (CCK) — s’est avérée centrale. Dans le cerveau, certains neurones dopaminergiques de la VTA libèrent aussi de la CCK. L’équipe a utilisé des souris génétiquement modifiées pour supprimer la CCK uniquement dans ces cellules. Sans CCK, les souris ne développaient plus une forte préférence pour la chambre associée à la meth, et l’augmentation habituelle de l’activité des cellules de la VTA sous meth était atténuée. Pourtant, ces souris se comportaient normalement lors de tests de motricité, de mémoire, d’anxiété et de comportements de type dépressif. Cela suggère que la CCK de la VTA n’est pas nécessaire au fonctionnement quotidien du cerveau, mais qu’elle est cruciale quand la meth tente d’ancrer un souvenir de récompense puissant.
Un seul récepteur comme verrou critique dans l’amygdale
La CCK agit en se liant à des récepteurs sur d’autres neurones, et les auteurs ont constaté que l’un d’eux, appelé CCK2R, devient particulièrement abondant dans la BLA après exposition à la meth. Lorsqu’ils ont supprimé CCK2R spécifiquement dans les cellules excitatrices de la BLA, la meth ne pouvait plus induire une forte préférence de lieu, et l’explosion d’activité anormale dans ces cellules était en grande partie normalisée. Des enregistrements fins ont montré que la meth augmente habituellement les connexions excitrices et les petites protubérances appelées épines dendritiques dans la BLA — des changements associés à des souvenirs plus forts et plus durables. La suppression de CCK2R empêchait ces modifications structurales et électriques, tout en préservant de nouveau l’apprentissage général et l’état émotionnel.
Propagation du signal vers un centre du stress
L’histoire ne s’est pas arrêtée dans l’amygdale. Grâce à un traçage viral sophistiqué, les chercheurs ont montré que les neurones dopaminergiques de la VTA alimentent les cellules excitatrices de la BLA, qui projettent à leur tour vers le BNST, une région liée à l’anxiété et à l’addiction. Mettre au silence cette chaîne VTA–BLA–BNST pendant l’entraînement à la meth réduisait fortement la préférence de lieu et calmait les neurones BNST hyperactifs. De manière cruciale, supprimer CCK2R uniquement dans le sous-ensemble de cellules BLA qui reçoivent l’entrée de la VTA et envoient des signaux au BNST bloquait les effets de la meth sur l’activité du BNST, le renforcement synaptique et la croissance des épines dendritiques. Les circuits qui ne projetaient pas vers le BNST étaient beaucoup moins affectés, soulignant à quel point l’« interrupteur » CCK2R est câblé de manière précise. 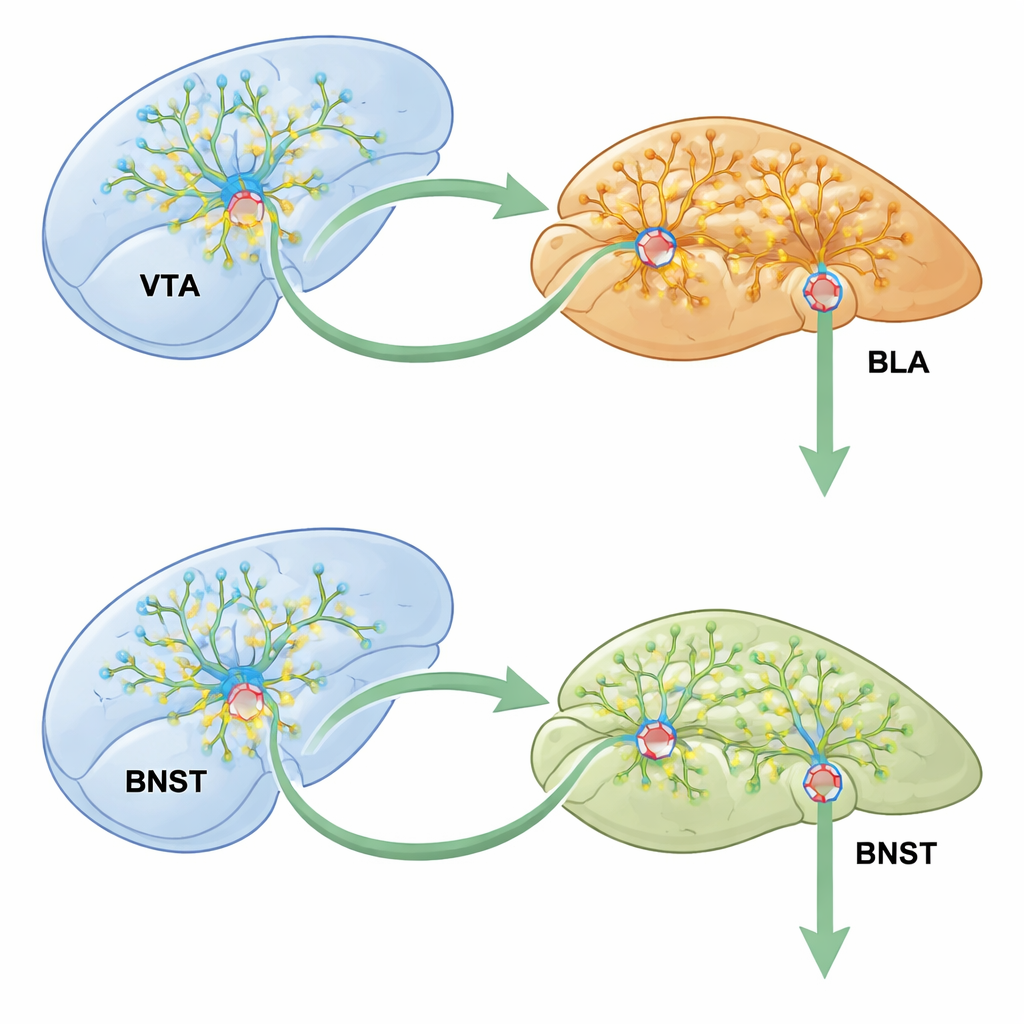
Ce que cela pourrait signifier pour le traitement futur
Dans l’ensemble, l’étude montre que la meth détourne un système messager gut–brain spécifique — la CCK agissant sur CCK2R — au sein d’un trajet VTA–BLA–BNST défini pour consolider les souvenirs liés à la drogue et favoriser la préférence pour les lieux associés à la drogue. Couper CCK2R dans ce circuit effaçait de nombreux signes d’addiction chez les souris, de l’hyperactivité neuronale à l’excès de synapses et aux altérations des rythmes cérébraux, sans perturber de façon générale l’émotion ou la cognition. Pour un lecteur non spécialiste, cela signifie que les scientifiques ont identifié un « disjoncteur » très sélectif pour la récompense liée à la meth. Des médicaments qui bloquent en toute sécurité CCK2R dans les bons circuits cérébraux pourraient un jour aider à affaiblir les envies de meth et le risque de rechute, offrant une thérapie plus ciblée que les approches actuelles.
Citation: Wang, J., Zhang, M., Qiao, L. et al. CCK2R regulates METH-induced CPP acquisition within VTA-BLA-BNST circuit in male mice. Transl Psychiatry 16, 210 (2026). https://doi.org/10.1038/s41398-026-03982-y
Mots-clés: addiction à la méthamphétamine, circuits cérébraux de la récompense, cholécystokinine, amygdale et BNST, mémoire liée à la drogue