Clear Sky Science · ru
Стратегии целевой доставки лекарств на основе пептидов для лечения остеоартрита
Новые пути доставки лекарств в болящие суставы
Остеоартрит — одна из самых частых причин боли в суставах и утраты подвижности, однако современные методы лечения в основном снимают симптомы, а не останавливают заболевание. Одна из ключевых причин проста: очень трудно доставить препараты в нужные участки сустава и удержать их там. В этом обзоре рассматривается, как крошечные молекулы — пептиды — могут быть специально спроектированы, чтобы переносить лекарства глубоко в поражённые ткани сустава, потенциально превращая кратковременное облегчение боли в настоящее, долговременное восстановление.
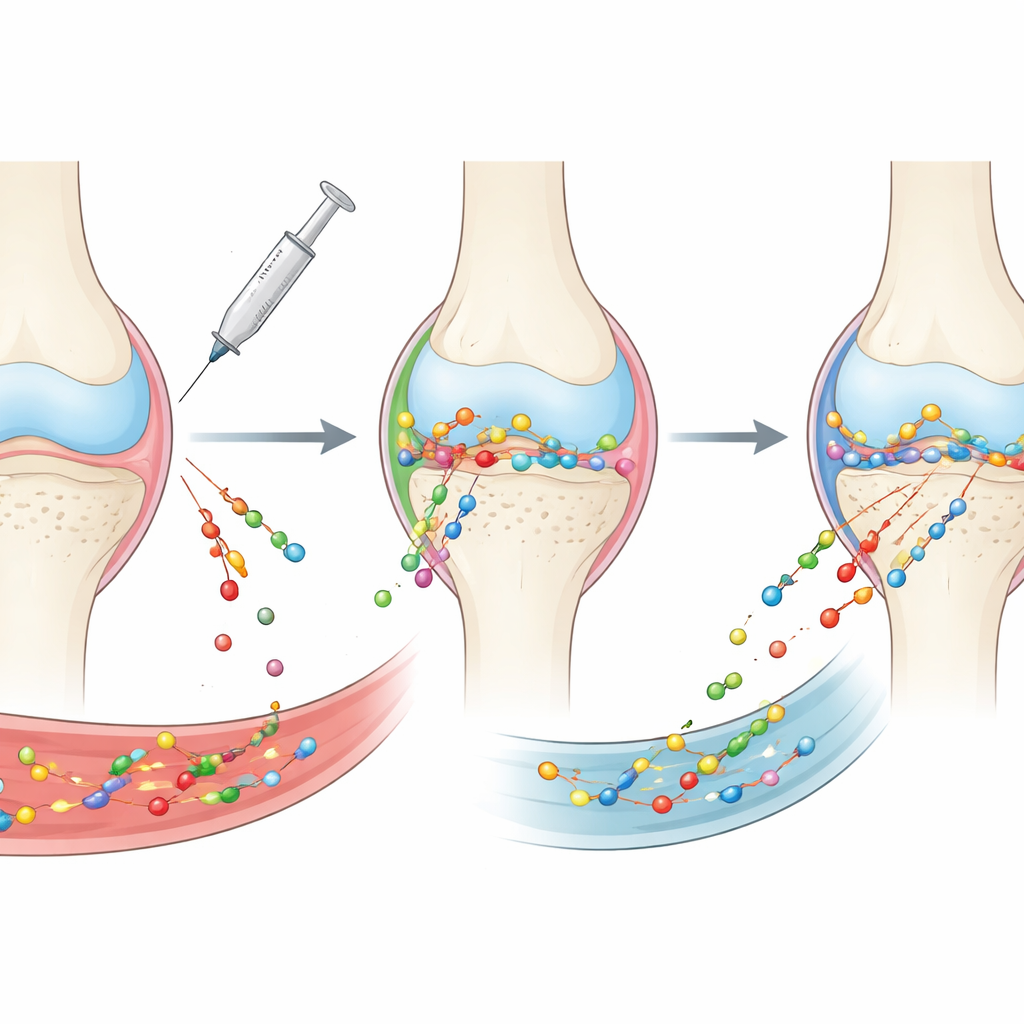
Почему так трудно лечить дегенеративный артрит
Остеоартрит уже недостаточно рассматривать как простое «истирание» хряща. Это заболевание всего сустава, в которое вовлечены хрящ, синовиальная оболочка, подлежащая кость, связки, жировые подушки и окружающая жидкость. Каждая из этих тканей имеет свою структуру и химические свойства, которые вместе образуют полосу препятствий для любого лекарства. Препараты, вводимые в полость сустава, быстро вымываются суставной жидкостью и кровеносными сосудами и испытывают сложности с проницанием через плотные, сетчато‑образные структуры. Лекарства, принимаемые внутрь или вводимые в вену, попадают в богатую кровеносными сосудами синовиальную оболочку и кость, но лишь малая часть достигает хряща, многое теряется по ходу всему организму. В результате многие перспективные молекулы так и не попадают в те места, где они наиболее нужны, или не задерживаются там достаточно долго, чтобы оказать эффект.
Пептиды как умные «адресные» носители
Пептиды — короткие цепочки аминокислот — занимают промежуточное положение между малыми молекулами и крупными терапевтическими антителами. Поскольку учёные могут изменять их последовательность практически по одному звену, пептиды можно настроить так, чтобы они прикреплялись к очень специфическим мишеням: определённому типу коллагена, богатому сахаром гелю, поверхности клетки или даже микрокристаллам минерала в кости. Авторы описывают два основных подхода к обнаружению таких «наводящих» последовательностей: широкие скрининги огромных библиотек пептидов и рациональное проектирование на основе известных характеристик ткани, например её заряда. После идентификации эти наводящие пептиды можно приклеить к препаратам, наночастицам или биологическим носителям, таким как экзосомы, направляя их к хрящу, синовии или субхондральной кости и помогая удерживаться на месте.
Достижение хряща, синовиальной оболочки и кости
Хрящ, гладкое покрытие на концах костей, особенно труднодоступен, поскольку он плотный и лишён кровеносных сосудов. Здесь полезны пептиды, распознающие основные строительные блоки хряща. Некоторые связываются с коллагеновыми волокнами, придающими хрящу прочность; другие используют сильный отрицательный заряд ткани, применяя положительно заряженные последовательности, которые притягиваются и удерживаются как магнит. Такие переносчики могут транспортировать противовоспалительные белки, факторы роста, усиливающие восстановление, контрастные агенты для визуализации или даже экзосомы с генетическим материалом, позволяя препаратам проникать на всю глубину хряща и оставаться там в течение нескольких дней. Похожие стратегии применимы к синовиальной оболочке, где специфические пептиды нацеливаются на фибробластоподобные клетки, иммунные клетки или аномальные новые сосуды, которые разрастаются при заболевании, концентрируя препараты, успокаивающие воспаление. В кости непосредственно под хрящом пептиды могут направлять терапевтические агенты к клеткам, формирующим кость, к клеткам, её разрушающим, или к самому минералу, помогая восстановить баланс ремоделирования кости, который в противном случае усугубляет остеоартрит.
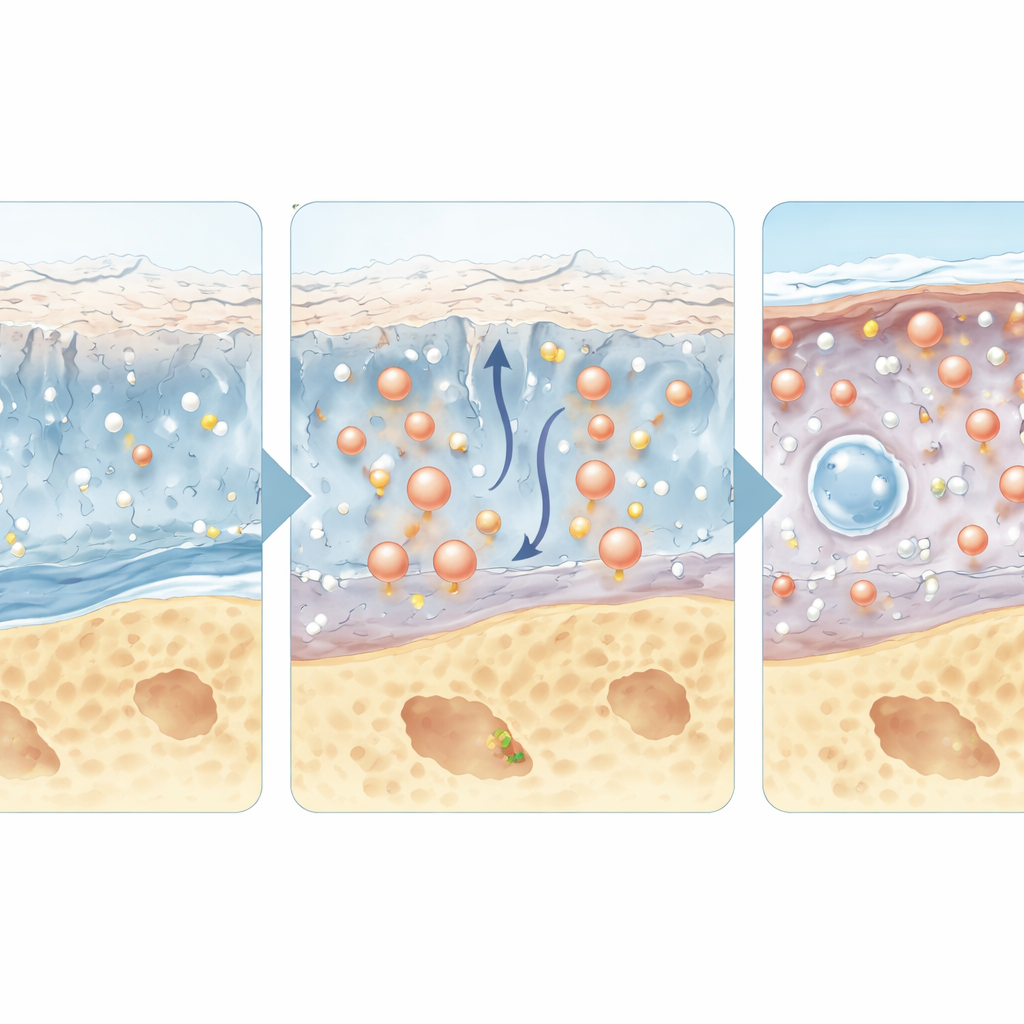
Пептиды, которые сами являются лекарствами
Помимо роли «маячков», некоторые пептиды действуют непосредственно как лекарства. Растущий список гормоноподобных и сигнальных пептидов способен снижать воспаление, защищать клетки хряща от повреждений, стимулировать синтез новой матрицы или подавлять болевые сигналы от нервов в суставе. Например модифицированные версии гамма‑подобного пептида‑1 (glucagon‑like peptide‑1), уже используемые при диабете и ожирении, также могут защищать ткани сустава от воспалительного стресса. Другие пептиды имитируют натуральные факторы, поощряющие рост хряща, или блокируют молекулы, вызывающие боль. Многие такие кандидаты показали положительный эффект в экспериментальных моделях на животных, а некоторые опираются на препараты, уже применяемые в клинике для других состояний, что делает их привлекательными для перепрофилирования при остеоартрите.
Увеличение стойкости пептидных препаратов и улучшение их тестирования
Одно из основных препятствий состоит в том, что пептиды обычно недолговечны: ферменты в крови и суставной жидкости быстро их расщепляют, а почки выводят из организма. Обзор описывает несколько способов обхода этой проблемы. Химики могут заменять уязвимые участки нестандартными аминокислотами, фиксировать пептиды в петли с помощью дисульфидных связей для жёсткости структуры или сцеплять их с более крупными партнёрами — полимерами, липидами или белками — что замедляет распад и выведение. Одновременно разработка с помощью компьютера и моделирование начинают ускорять поиск новых стабильных последовательностей и предсказывать их связывание с мишенями. На стороне тестирования продвинутые модели «сустав‑на‑чипе», объединяющие человеческий хрящ, синовию, кость и контролируемый поток жидкости, могут предоставить более реалистичную площадку для испытаний по сравнению с традиционными клеточными культурами или животными моделями, помогая отбирать множество конструкций перед дорогостоящими клиническими испытаниями.
К более умным и длительно действующим методам лечения суставов
В совокупности работы, рассмотренные в этой статье, указывают на будущее, в котором остеоартрит лечат не только обезболиванием, но и точечной доставкой мощных терапий в каждую из ключевых тканей сустава с удержанием их там достаточно долго, чтобы изменить ход болезни. Пептиды, созданные на заказ, могут служить и адресными метками, и активными лекарственными агентами, ориентируясь в сложной «географии» сустава и ограничивая воздействие на остальной организм. По мере того как инженерия стабильности, компьютерное проектирование и модели, релевантные для человека, продолжают развиваться, стратегии на основе пептидов могут наконец открыть путь к модифицирующим заболевание лечениям, возвращающим подвижность и комфорт людям с остеоартритом.
Цитирование: Hakim, B., Zhang, H., Selvadoss, A. et al. Peptide-based targeted drug delivery strategies for osteoarthritis treatment. npj Biomed. Innov. 3, 27 (2026). https://doi.org/10.1038/s44385-026-00082-w
Ключевые слова: остеоартрит, пептидная доставка лекарств, таргетирование хряща, воспаление суставов, регенеративная медицина