Clear Sky Science · fr
Stratégies de délivrance ciblée de médicaments à base de peptides pour le traitement de l’arthrose
Nouvelles façons d’amener les médicaments dans les articulations douloureuses
L’arthrose est l’une des causes les plus fréquentes de douleur et d’invalidité articulaires, et les traitements actuels soulagent surtout les symptômes plutôt que d’arrêter la maladie. Une raison majeure est étonnamment simple : il est très difficile d’amener les médicaments jusqu’aux bonnes zones de l’articulation et de les y maintenir. Cette revue examine comment de minuscules molécules appelées peptides peuvent être conçues sur mesure pour transporter des médicaments profondément dans les tissus articulaires malades — transformant potentiellement un soulagement passager en une véritable réparation durable.
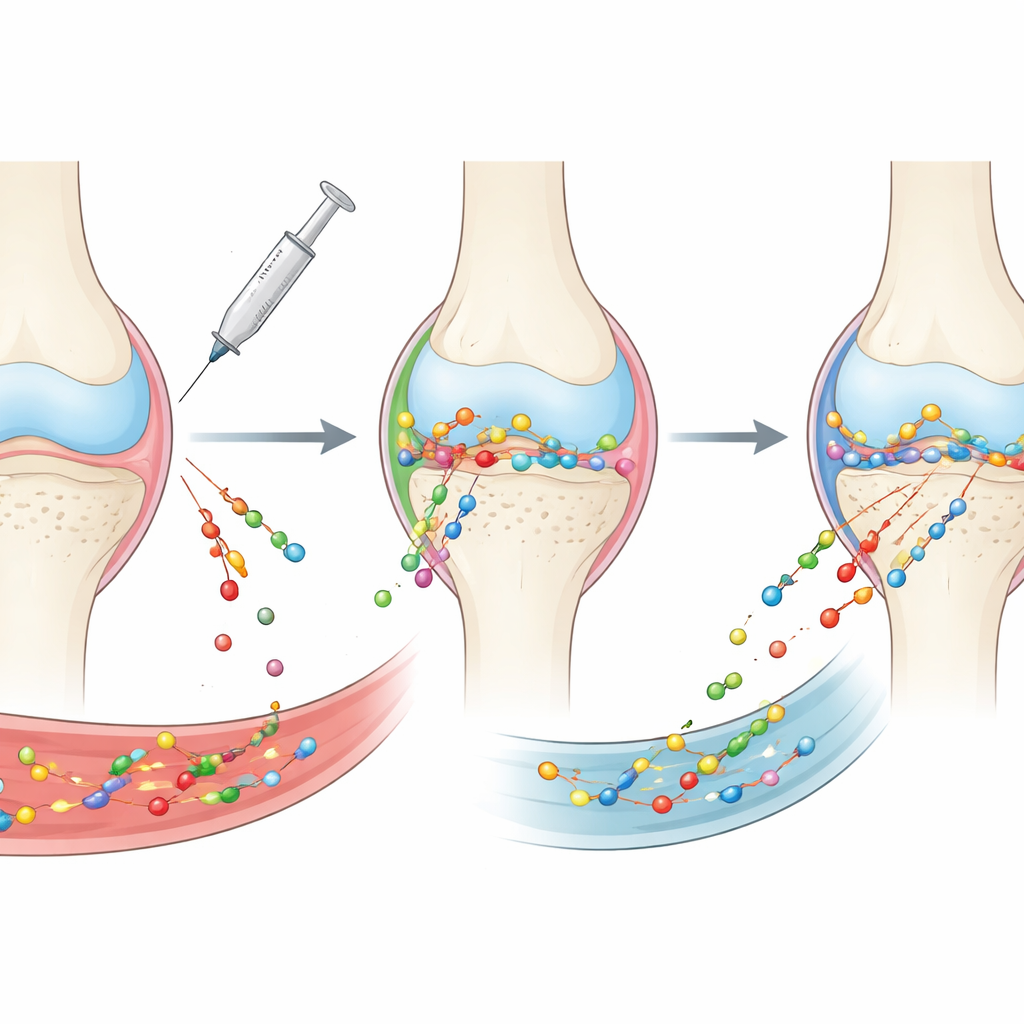
Pourquoi il est si difficile de traiter l’arthrite d’usure
L’arthrose n’est plus considérée comme un simple « usure » du cartilage. C’est une maladie de l’articulation entière qui implique le cartilage, la membrane synoviale, l’os sous-jacent, les ligaments, les coussinets adipeux et le liquide qui les baigne. Chacun de ces tissus a sa propre structure et sa propre chimie, formant ensemble un véritable parcours d’obstacles pour tout médicament. Les médicaments injectés dans l’espace articulaire sont rapidement évacués par le liquide synovial et les vaisseaux sanguins, et peinent à traverser des tissus denses et en réseau. Les médicaments administrés par voie orale ou intraveineuse atteignent la membrane synoviale riche en sang et l’os, mais seule une infime fraction pénètre dans le cartilage et beaucoup se perd dans le reste de l’organisme. Ainsi, de nombreuses molécules prometteuses n’atteignent jamais les zones où elles sont le plus nécessaires ou n’y restent pas assez longtemps pour être efficaces.
Les peptides comme dispositifs d’orientation intelligents
Les peptides — courtes chaînes d’acides aminés — se situent entre les petits médicaments et les grosses thérapies par anticorps. Parce que les scientifiques peuvent ajuster leur séquence presque un bloc de construction à la fois, les peptides peuvent être conçus pour se fixer à des cibles très spécifiques : un type de collagène, un gel riche en sucres, une surface cellulaire, ou même de minuscules cristaux minéraux dans l’os. Les auteurs décrivent deux manières principales de découvrir de telles séquences « d’orientation » : un criblage large de vastes bibliothèques de peptides, et la conception rationnelle basée sur les caractéristiques connues d’un tissu, comme sa charge globale. Une fois identifiés, ces peptides d’adressage peuvent être collés sur des médicaments, des nanoparticules ou des vecteurs biologiques comme les exosomes, les dirigeant vers le cartilage, la synoviale ou l’os sous-chondral et aidant à les y maintenir.
Atteindre le cartilage, la membrane synoviale et l’os
Le cartilage, la couche lisse aux extrémités des os, est particulièrement difficile d’accès car il est dense et dépourvu de vaisseaux sanguins. Ici, les peptides qui reconnaissent les principaux composants du cartilage sont utiles. Certains se lient aux fibres de collagène qui donnent au cartilage sa résistance ; d’autres exploitent la forte charge négative du tissu en utilisant des séquences chargées positivement qui sont attirées et retenues comme par des aimants. Ces vecteurs peuvent acheminer des protéines anti-inflammatoires, des facteurs de croissance qui stimulent la réparation, des agents d’imagerie ou même des exosomes transportant des gènes, permettant aux médicaments de pénétrer sur toute l’épaisseur du cartilage et d’y rester pendant des jours. Des stratégies similaires s’appliquent à la membrane synoviale, où des peptides spécifiques ciblent les cellules fibroblastiques, les cellules immunitaires ou les nouveaux vaisseaux anormaux qui poussent pendant la maladie, concentrant les médicaments qui calment l’inflammation. Dans l’os juste sous le cartilage, les peptides peuvent guider les thérapeutiques vers les cellules formatrices d’os, les cellules résorbant l’os ou vers le minéral lui‑même, aidant à rééquilibrer le remodelage osseux qui, sinon, aggrave l’arthrose.
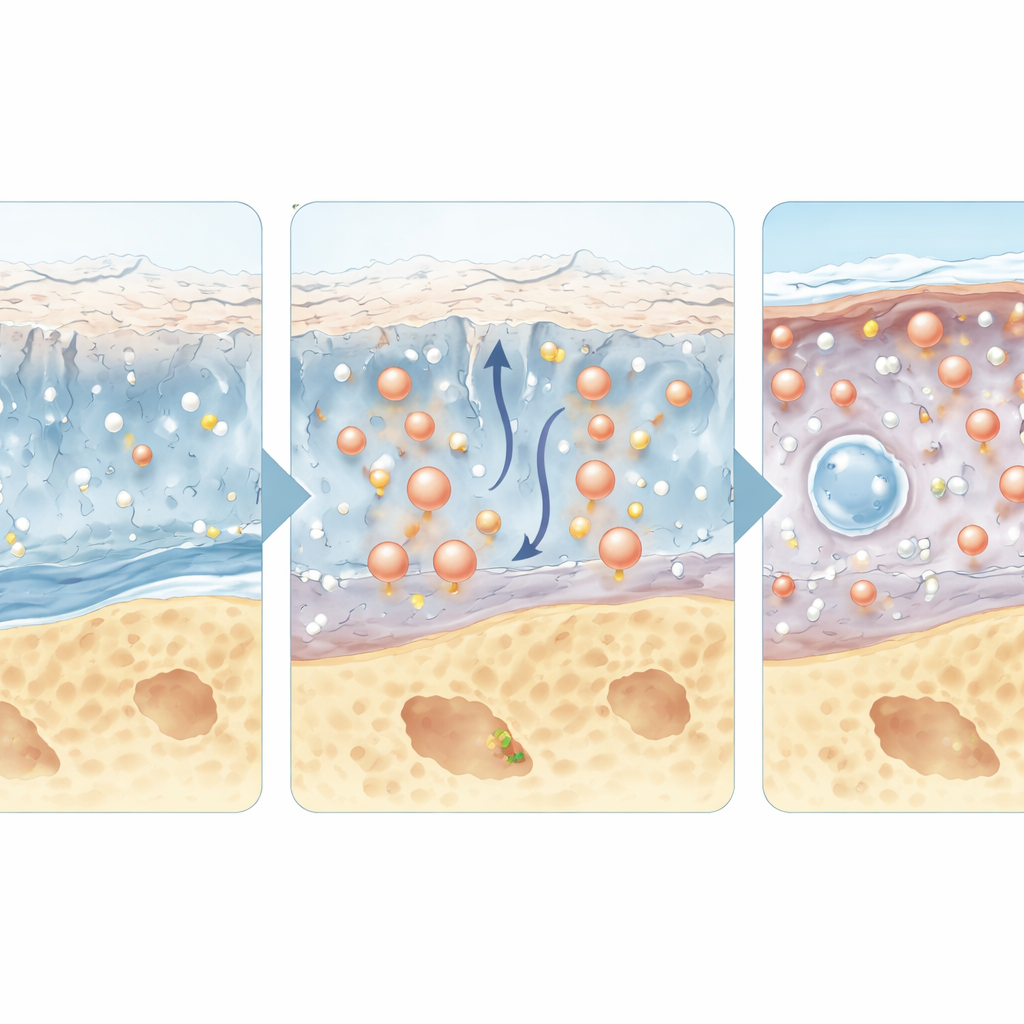
Des peptides qui sont eux-mêmes des médicaments
Au-delà de leur rôle d’adresses, certains peptides agissent directement comme médicaments. Une liste croissante de peptides hormonaux et de signalisation peut réduire l’inflammation, protéger les cellules du cartilage des dommages, stimuler la production de matrice ou atténuer les signaux de douleur provenant des nerfs de l’articulation. Par exemple, des versions modifiées du peptide‑1 de type glucagon, déjà utilisées pour traiter le diabète et l’obésité, peuvent aussi protéger les tissus articulaires du stress inflammatoire. D’autres peptides imitent des facteurs naturels favorisant la croissance du cartilage, ou bloquent des molécules déclenchant la douleur. Beaucoup de ces candidats ont montré des bénéfices dans des modèles animaux, et certains s’appuient sur des médicaments déjà utilisés en clinique pour d’autres affections, ce qui les rend attractifs pour un repositionnement vers l’arthrose.
Prolonger la durée d’action des traitements peptidiques et mieux les tester
Un obstacle majeur est que les peptides sont normalement de courte durée ; des enzymes dans le sang et le liquide articulaire les dégradent rapidement, et les reins les éliminent. La revue présente plusieurs solutions de contournement. Les chimistes peuvent remplacer des acides aminés vulnérables par des variants non standards, boucler les peptides avec des liaisons disulfure pour rigidifier leur conformation, ou les accrocher à des partenaires plus volumineux comme des polymères, des lipides ou des protéines qui ralentissent leur dégradation et leur clairance. Parallèlement, la conception assistée par ordinateur et la simulation commencent à accélérer la recherche de nouvelles séquences stables et à prédire comment elles se lient à leurs cibles. Côté essais, des modèles avancés de « joint‑on‑a‑chip » combinant cartilage humain, synovium, os et flux de fluide contrôlé peuvent offrir un terrain d’essai plus réaliste que les cultures cellulaires traditionnelles ou les études animales, aidant à cribler de nombreux designs avant de passer à des essais coûteux.
Vers des thérapies articulaires plus intelligentes et plus durables
Dans l’ensemble, les travaux passés en revue pointent vers un avenir où l’arthrose serait traitée non seulement en calmant la douleur, mais en délivrant avec précision des thérapeutiques puissantes à chacun des tissus clés de l’articulation et en les y maintenant suffisamment longtemps pour modifier le cours de la maladie. Les peptides conçus sur mesure peuvent agir à la fois comme étiquettes d’adresse et comme médicaments actifs, naviguant dans la géographie complexe de l’articulation tout en limitant l’exposition au reste de l’organisme. À mesure que l’ingénierie de la stabilité, la conception assistée par ordinateur et les systèmes de test pertinents pour l’homme continuent de mûrir, les stratégies à base de peptides pourraient enfin débloquer des traitements modifiant la maladie et redonnant mobilité et confort aux personnes vivant avec l’arthrose.
Citation: Hakim, B., Zhang, H., Selvadoss, A. et al. Peptide-based targeted drug delivery strategies for osteoarthritis treatment. npj Biomed. Innov. 3, 27 (2026). https://doi.org/10.1038/s44385-026-00082-w
Mots-clés: arthrose, libération de médicaments par peptide, ciblage du cartilage, inflammation articulaire, médecine régénératrice