Clear Sky Science · pl
Strategie celowanego dostarczania leków oparte na peptydach w leczeniu choroby zwyrodnieniowej stawów
Nowe sposoby dostarczania leków do bolących stawów
Choroba zwyrodnieniowa stawów jest jedną z najczęstszych przyczyn bólu i niepełnosprawności stawów, a dzisiejsze terapie głównie łagodzą objawy zamiast zatrzymać postęp choroby. Jednym z głównych powodów jest, paradoksalnie, prosty problem: bardzo trudno jest doprowadzić leki do właściwych miejsc w stawie i sprawić, by tam pozostały. Ten przegląd opisuje, jak małe cząsteczki zwane peptydami można zaprojektować tak, by przenosiły leki głęboko do chorobowo zmienionych tkanek stawu — potencjalnie zmieniając krótkotrwałą ulgę w bólu w prawdziwą, długotrwałą naprawę.
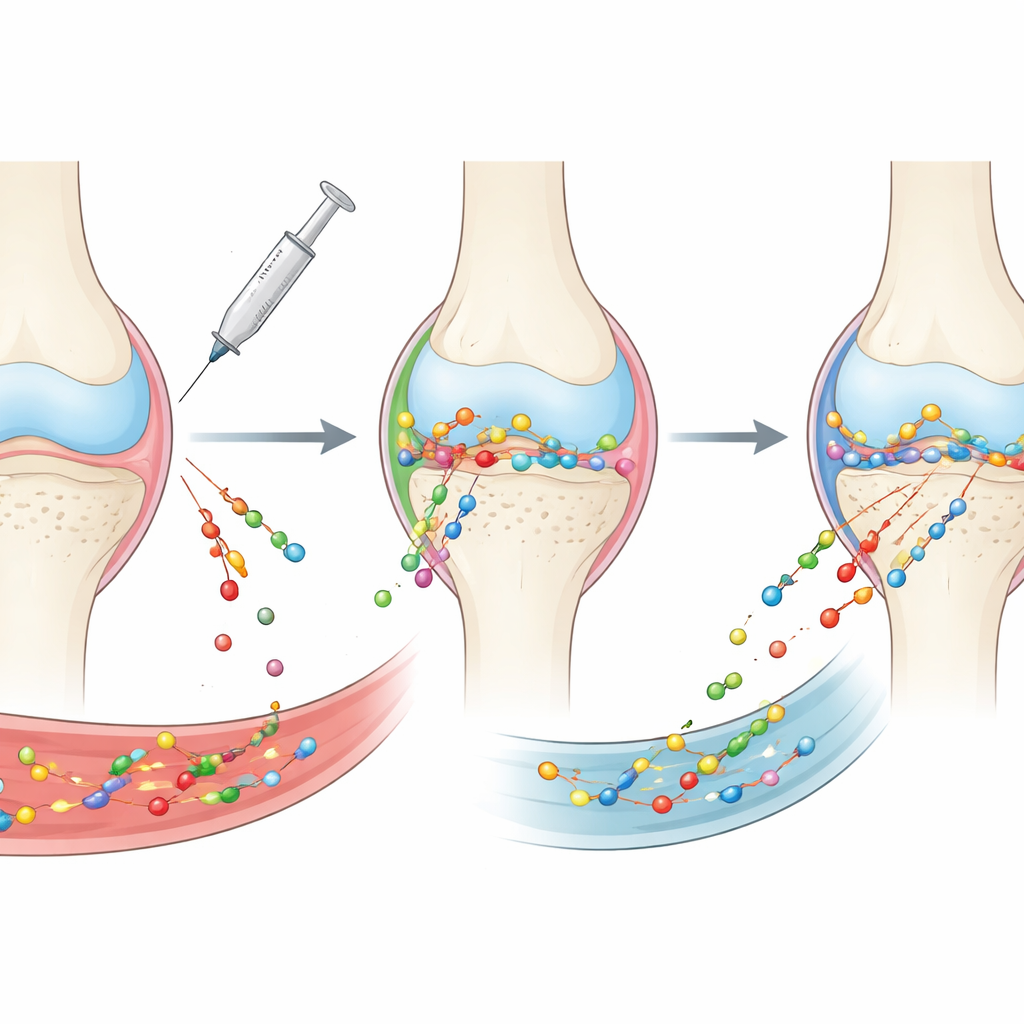
Dlaczego leczenie choroby zwyrodnieniowej jest tak trudne
Choroba zwyrodnieniowa stawów nie jest już postrzegana jedynie jako „zużycie” chrząstki. To choroba całego stawu obejmująca chrząstkę, błonę maziową, leżącą pod nią kość, więzadła, poduszeczki tłuszczowe i płyn stawowy. Każda z tych tkanek ma swoją strukturę i chemię, które tworzą szereg barier dla każdego leku. Leki wstrzyknięte do jamy stawowej są szybko usuwane przez płyn stawowy i naczynia krwionośne, i mają trudność z przejściem przez gęstą, sieciowatą tkankę. Preparaty podawane doustnie lub dożylnie trafiają do bogatej we krwi wyściółki stawowej i kości, ale tylko niewielka ich część dociera do chrząstki, a reszta jest rozpraszana po organizmie. W rezultacie wiele obiecujących molekuł nigdy nie dociera tam, gdzie są najbardziej potrzebne, lub nie utrzymuje się wystarczająco długo, by działać.
Peptydy jako inteligentne „wskazówki adresowe”
Peptydy — krótkie łańcuchy aminokwasów — mieszczą się między lekami małocząsteczkowymi a dużymi terapiami przeciwciałowymi. Ponieważ naukowcy mogą dobierać ich sekwencję niemal jeden aminokwas po drugim, peptydy można tak zaprojektować, by przyczepiały się do bardzo specyficznych celów: rodzaju kolagenu, żelopodobnej substancji bogatej w cukry, powierzchni komórkowej, a nawet drobnych kryształków mineralnych w kości. Autorzy opisują dwa główne sposoby znajdowania takich „nakierowujących” sekwencji: szerokie przesiewy olbrzymich bibliotek peptydów oraz projektowanie racjonalne oparte na znanych cechach tkanki, na przykład jej ładunku. Po zidentyfikowaniu te peptydy-homing można przyczepiać do leków, nanocząstek lub nośników biologicznych, takich jak egzosomy, kierując je ku chrząstce, błonie maziowej lub kości podchrzęstnej i pomagając im tam pozostać.
Dostęp do chrząstki, wyściółki stawu i kości
Chrząstka, gładka powłoka na końcach kości, jest szczególnie trudna do osiągnięcia, ponieważ jest gęsta i nieunaczyniona. Tutaj przydatne są peptydy rozpoznające główne składniki budulcowe chrząstki. Niektóre wiążą się z włóknami kolagenowymi, które nadają chrząstce wytrzymałość; inne wykorzystują silny ujemny ładunek tkanki, stosując dodatnio naładowane sekwencje, które są przyciągane i utrzymywane niczym magnesy. Te nośniki mogą wciągać białka przeciwzapalne, czynniki wzrostu pobudzające naprawę, środki obrazujące, a nawet egzosomy niosące geny, pozwalając lekom przeniknąć przez pełną głębokość chrząstki i utrzymywać się w niej przez dni. Podobne strategie stosuje się względem błony maziowej, gdzie określone peptydy kierują się ku komórkom fibroblastopodobnym, komórkom układu odpornościowego lub nieprawidłowym nowo powstającym naczyniom krwionośnym, koncentrując leki łagodzące zapalenie. W kości tuż pod chrząstką peptydy mogą prowadzić terapie do komórek tworzących kość, komórek resorbujących kość lub samego minerału, pomagając przywrócić równowagę przebudowy kostnej, która w przeciwnym razie pogarszałaby przebieg choroby zwyrodnieniowej.
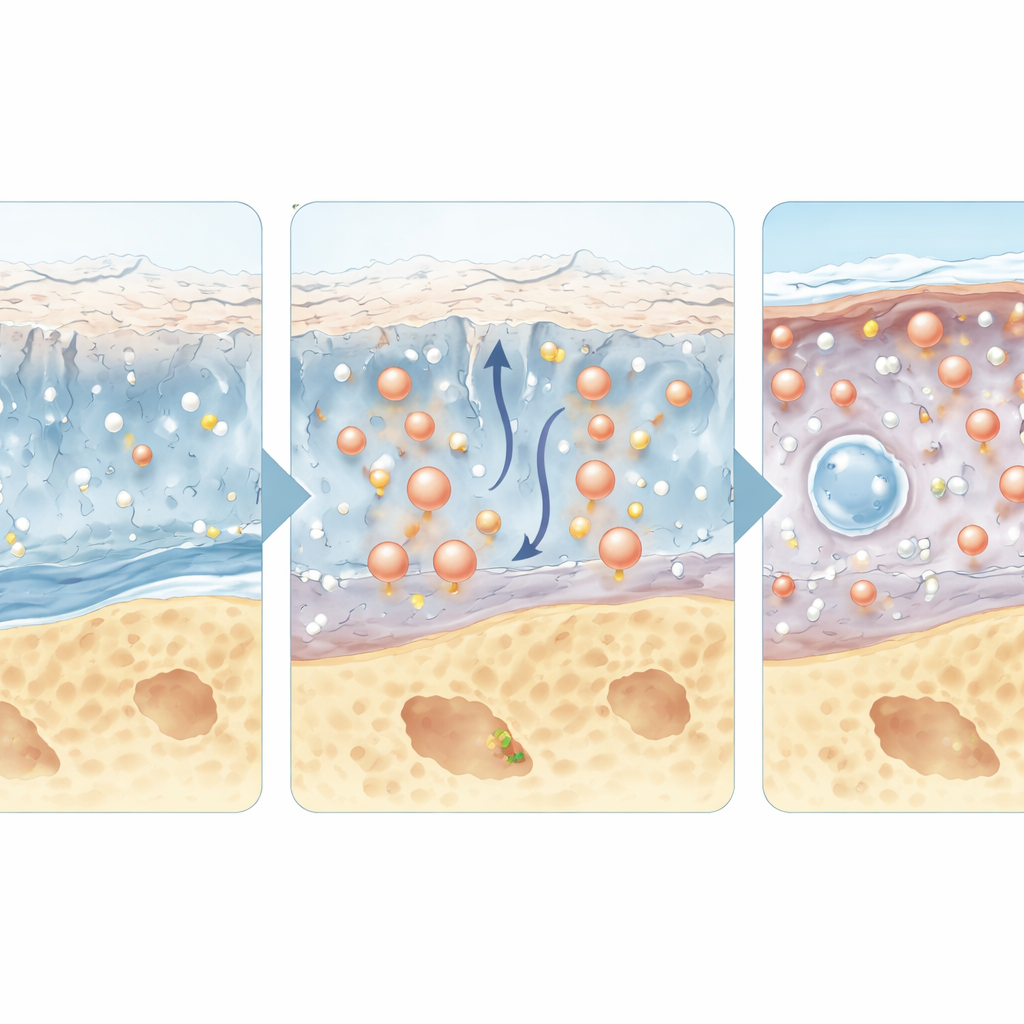
Peptydy będące lekami samymi w sobie
Poza rolą sygnałów kierujących, niektóre peptydy działają bezpośrednio jako leki. Coraz dłuższa lista peptydów hormonalnych i sygnałowych może tłumić zapalenie, chronić komórki chrząstki przed uszkodzeniem, pobudzać produkcję macierzy lub osłabiać sygnały bólowe z nerwów w stawie. Na przykład zmodyfikowane wersje peptydu podobnego do glukagonu‑1, już stosowanego w leczeniu cukrzycy i otyłości, mogą także chronić tkanki stawowe przed stresem zapalnym. Inne peptydy naśladują naturalne czynniki zachęcające do wzrostu chrząstki lub blokują molekuły wywołujące ból. Wiele takich kandydatów wykazało korzyści w modelach zwierzęcych, a niektóre opierają się na lekach już stosowanych klinicznie w innych schorzeniach, co czyni je atrakcyjnymi do ponownego zastosowania w chorobie zwyrodnieniowej stawów.
Wydłużanie działania peptydów i lepsze testowanie
Jedną z głównych przeszkód jest to, że peptydy zazwyczaj nie są trwałe; enzymy we krwi i płynie stawowym szybko je rozkładają, a nerki usuwają je z organizmu. Przegląd opisuje kilka sposobów obejścia tego problemu. Chemicy mogą zamieniać podatne miejsca na niestandardowe aminokwasy, zszywać peptydy w pętle za pomocą mostków disiarczkowych, by usztywnić ich kształt, lub przyłączać je do większych partnerów, takich jak polimery, lipidy czy białka, co spowalnia rozkład i eliminację. Jednocześnie projektowanie wspomagane komputerowo i symulacje zaczynają przyspieszać poszukiwanie nowych, stabilnych sekwencji i przewidywać, jak będą wiązać się ze swoimi celami. W zakresie testowania zaawansowane modele „staw na chipie”, łączące ludzką chrząstkę, błonę maziową, kość i kontrolowany przepływ płynu, mogą oferować bardziej realistyczne pole prób niż tradycyjne hodowle komórkowe czy badania na zwierzętach, umożliwiając przesiewanie wielu konstrukcji przed przejściem do kosztownych prób klinicznych.
W kierunku mądrzejszych, dłużej działających terapii stawów
Podsumowując, prace zebrane w tym artykule wskazują na przyszłość, w której choroba zwyrodnieniowa stawów jest leczona nie tylko poprzez tłumienie bólu, lecz przez precyzyjne dostarczanie silnych terapii do kluczowych tkanek stawu i utrzymywanie ich tam wystarczająco długo, by zmienić przebieg choroby. Peptydy zaprojektowane na miarę mogą pełnić rolę zarówno etykiet adresowych, jak i aktywnych leków, nawigując po skomplikowanej geografii stawu i ograniczając ekspozycję reszty organizmu. W miarę jak inżynieria stabilności, projektowanie wspomagane komputerowo i testy o większym znaczeniu klinicznym będą dojrzewać, strategie oparte na peptydach mogą wreszcie odblokować leki modyfikujące przebieg choroby, przywracając ruch i komfort osobom żyjącym z chorobą zwyrodnieniową stawów.
Cytowanie: Hakim, B., Zhang, H., Selvadoss, A. et al. Peptide-based targeted drug delivery strategies for osteoarthritis treatment. npj Biomed. Innov. 3, 27 (2026). https://doi.org/10.1038/s44385-026-00082-w
Słowa kluczowe: choroba zwyrodnieniowa stawów, dostarczanie leków peptydowych, celowanie w chrząstkę, zapalenie stawów, medycyna regeneracyjna