Clear Sky Science · de
Peptidbasierte zielgerichtete Wirkstofffreisetzungsstrategien zur Behandlung der Osteoarthritis
Neue Wege, Medikamente in schmerzende Gelenke zu bringen
Osteoarthritis ist eine der häufigsten Ursachen für Gelenkschmerzen und Behinderungen, doch die heutigen Behandlungen lindern meist nur die Symptome, anstatt die Krankheit aufzuhalten. Ein entscheidender Grund ist überraschend einfach: Es ist sehr schwer, Wirkstoffe in die richtigen Bereiche des Gelenks zu bringen und dort zu halten. Dieser Übersichtsartikel untersucht, wie winzige Moleküle, sogenannte Peptide, maßgeschneidert werden können, um Arzneistoffe tief in erkrankte Gelenkgewebe zu transportieren — und so kurzzeitige Schmerzlinderung möglicherweise in echte, lang anhaltende Reparatur zu verwandeln.
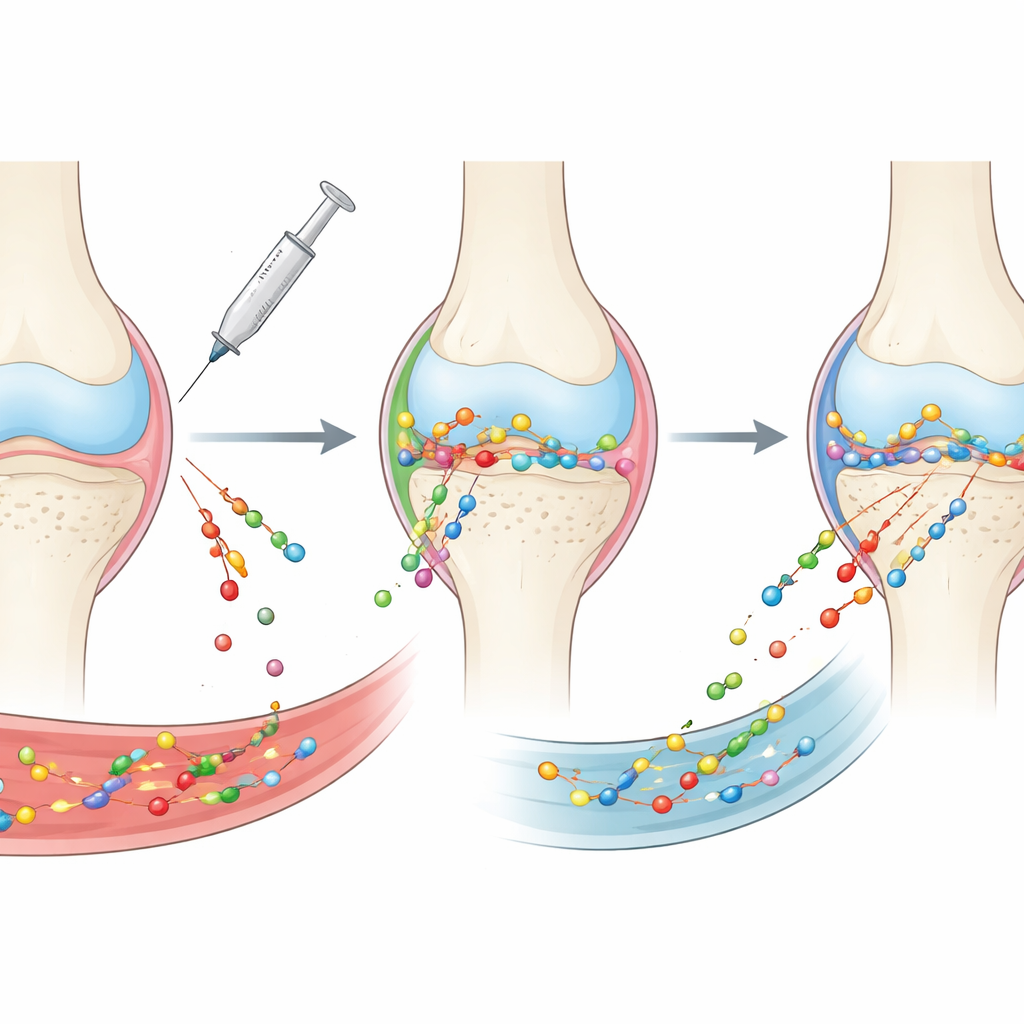
Warum die Behandlung von Verschleißarthrose so schwierig ist
Osteoarthritis wird nicht mehr nur als reiner "Verschleiß" des Knorpels gesehen. Es ist eine Erkrankung des gesamten Gelenks, die Knorpel, Synovialauskleidung, den darunter liegenden Knochen, Bänder, Fettpolster und die sie umgebende Flüssigkeit umfasst. Jedes dieser Gewebe hat seine eigene Struktur und Chemie, die zusammen eine Reihe von Barrieren für jeden Wirkstoff bilden. In das Gelenk injizierte Medikamente werden schnell durch Gelenkflüssigkeit und Blutgefäße ausgespült und haben Schwierigkeiten, dichte, netzartige Gewebe zu durchdringen. Systemisch verabreichte Medikamente erreichen die blutreichen Gelenkauskleidung und den Knochen, doch nur ein winziger Bruchteil gelangt in den Knorpel; vieles geht im Rest des Körpers verloren. Daher erreichen viele vielversprechende Moleküle nie die Orte, an denen sie am meisten gebraucht werden, oder verweilen nicht lange genug dort, um zu wirken.
Peptide als intelligente Ortungsgeräte
Peptide — kurze Aminosäureketten — liegen zwischen kleinmolekularen Arzneistoffen und großen Antikörpertherapien. Weil Wissenschaftler ihre Sequenz fast Baustein für Baustein abstimmen können, lassen sich Peptide so gestalten, dass sie an sehr spezifische Ziele binden: einen bestimmten Kollagentyp, ein zuckerreiches Gel, eine Zelloberfläche oder sogar winzige Mineralienkristalle im Knochen. Die Autoren beschreiben zwei Hauptwege, wie solche "Ortsbestimmungs"-Sequenzen gefunden werden: breit angelegte Screeningverfahren großer Peptidbibliotheken und rationale Gestaltung basierend auf bekannten Eigenschaften eines Gewebes, etwa seiner Gesamtladung. Einmal identifiziert, können diese Zielpeptide an Medikamente, Nanopartikel oder biologische Träger wie Exosomen gekoppelt werden, wodurch sie Richtung Knorpel, Synovium oder subchondralen Knochen gelenkt werden und dort haften bleiben.
Knorpel, Gelenkauskleidung und Knochen erreichen
Knorpel, die glatte Schicht an den Enden der Knochen, ist besonders schwer erreichbar, weil er dicht ist und keine Blutgefäße besitzt. Hier sind Peptide, die die Hauptbausteine des Knorpels erkennen, nützlich. Einige binden an Kollagenfasern, die dem Knorpel seine Festigkeit verleihen; andere nutzen die stark negative Ladung des Gewebes, indem sie positiv geladene Sequenzen verwenden, die wie Magneten angezogen und gehalten werden. Solche Träger können entzündungshemmende Proteine, Wachstumsfaktoren, die die Reparatur fördern, Bildgebungsmittel oder sogar genetische Fracht in Exosomen hineinschleppen, sodass Wirkstoffe durch die gesamte Knorpeltiefe eindringen und dort Tage lang verbleiben. Ähnliche Strategien lassen sich auf die Synovialauskleidung übertragen, wo spezifische Peptide auf fibroblastähnliche Zellen, Immunzellen oder die abnormalen neuen Blutgefäße zielen, die sich während der Erkrankung bilden, und so Wirkstoffe konzentrieren, die die Entzündung dämpfen. Im Knochen direkt unter dem Knorpel können Peptide Therapeutika zu knochenbildenden Zellen, knochenabbauenden Zellen oder direkt zur Mineralmatrix führen und so das Knochenumbaugleichgewicht wiederherstellen, das andernfalls die Osteoarthritis verschlimmert.
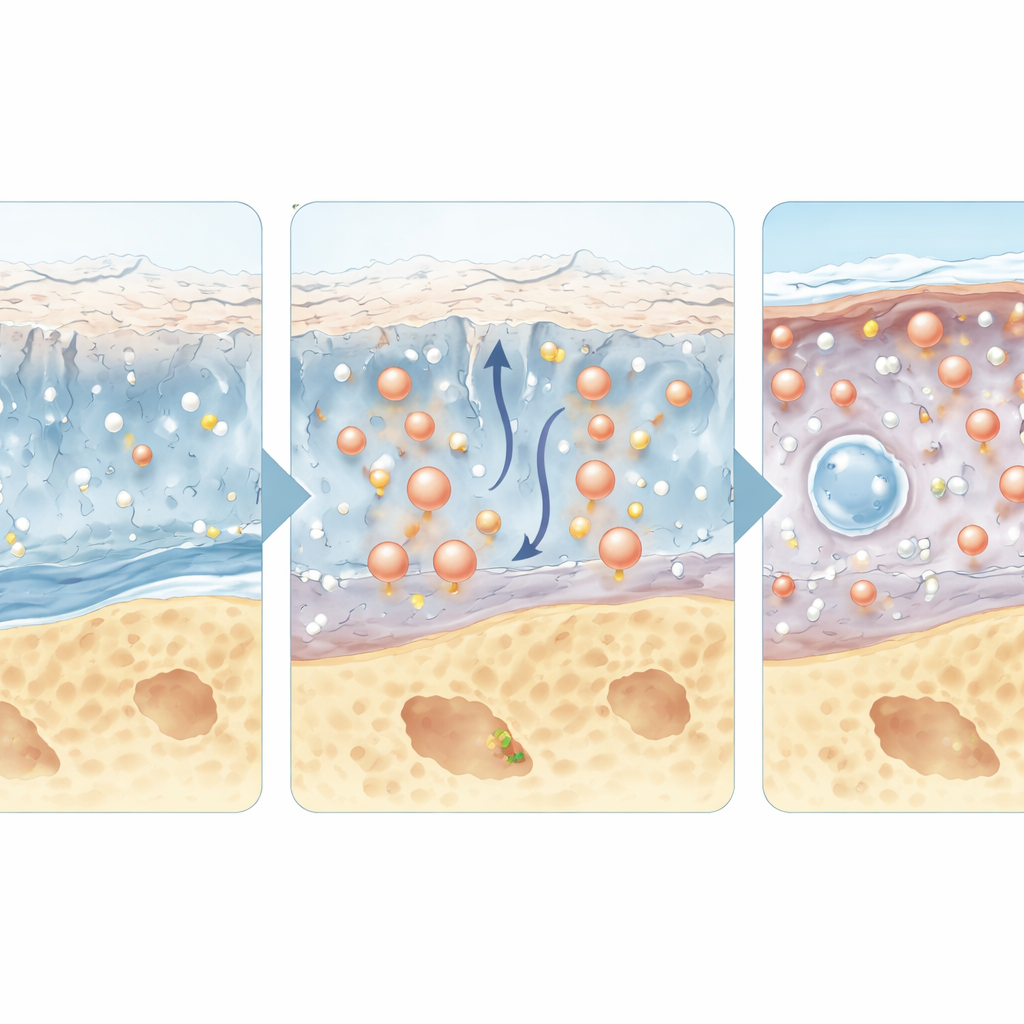
Peptide, die selbst Medikamente sind
Über ihre Rolle als Ortungsmarken hinaus wirken einige Peptide direkt als Arzneimittel. Eine wachsende Zahl hormonsimilarer und signalgebender Peptide kann Entzündungen abschwächen, Knorpelzellen vor Schäden schützen, die Produktion von neuer Matrix anregen oder Schmerzsignale von Nerven im Gelenk dämpfen. Beispielsweise können modifizierte Varianten des Glucagon-like Peptid‑1, das bereits zur Behandlung von Diabetes und Adipositas eingesetzt wird, auch Gelenkgewebe vor entzündungsbedingtem Stress schützen. Andere Peptide ahmen natürliche Faktoren nach, die das Knorpelwachstum fördern, oder blockieren Moleküle, die Schmerzen auslösen. Viele dieser Kandidaten zeigten positive Effekte in Tiermodellen, und einige bauen auf bereits klinisch eingesetzten Medikamenten für andere Erkrankungen auf, was sie für eine Umwidmung zur Behandlung der Osteoarthritis attraktiv macht.
Peptidtherapien haltbarer machen und besser testen
Eine große Hürde ist, dass Peptide normalerweise kurzlebig sind; Enzyme im Blut und in der Gelenkflüssigkeit bauen sie schnell ab, und die Nieren scheiden sie aus. Die Übersicht skizziert mehrere Umgehungsstrategien. Chemiker können an verwundbaren Stellen nicht‑standard Aminosäuren einbauen, Peptide mit Disulfidbrücken zu Schlaufen verbinden, um ihre Form zu stabilisieren, oder sie an größere Partner wie Polymere, Lipide oder Proteine koppeln, die den Abbau und die Ausscheidung verlangsamen. Gleichzeitig beschleunigen computergestützte Entwurfs‑ und Simulationsverfahren die Suche nach neuen stabilen Sequenzen und helfen vorherzusagen, wie sie an ihre Ziele binden. Beim Testen könnten fortschrittliche "Gelenk‑auf‑einem‑Chip"‑Modelle, die menschlichen Knorpel, Synovium, Knochen und kontrollierten Flüssigkeitsfluss kombinieren, eine realistischere Prüfplattform bieten als traditionelle Zellkulturen oder Tierversuche und viele Designs screeningtauglich machen, bevor teure Studien beginnen.
Auf dem Weg zu intelligenteren, länger wirkenden Gelenktherapien
Insgesamt weist die hier zusammengestellte Arbeit in eine Zukunft, in der Osteoarthritis nicht nur durch Schmerzlinderung behandelt wird, sondern durch präzise Lieferung potenter Therapien an die wichtigsten Gewebe des Gelenks — und deren Verweilen dort lange genug, um den Krankheitsverlauf zu verändern. Maßgeschneiderte Peptide können sowohl als Adressetiketten als auch als aktive Wirkstoffe fungieren, die sich in der komplexen Geographie des Gelenks zurechtfinden und gleichzeitig die Belastung des übrigen Körpers begrenzen. Mit fortschreitender Stabilitätsoptimierung, computergestütztem Design und humanrelevanten Testsystemen könnten peptidbasierte Strategien schließlich krankheitsmodifizierende Behandlungen ermöglichen, die Bewegung und Wohlbefinden für Menschen mit Osteoarthritis wiederherstellen.
Zitation: Hakim, B., Zhang, H., Selvadoss, A. et al. Peptide-based targeted drug delivery strategies for osteoarthritis treatment. npj Biomed. Innov. 3, 27 (2026). https://doi.org/10.1038/s44385-026-00082-w
Schlüsselwörter: Osteoarthritis, Peptid-Wirkstofffreisetzung, Knorpelzielsteuerung, Gelenkentzündung, regenerative Medizin