Clear Sky Science · he
אסטרטגיות משלוח תרופות ממוקד על בסיס פפטידים לטיפול באוסטאוארטריטיס
דרכים חדשות להכניס תרופות למפרקים הכואבים
אוסטאוארטריטיס היא אחת הסיבות השכיחות ביותר לכאב מפרקי ולנכות, אך הטיפולים הקיימים כיום מרגיעים בעיקר תסמינים ולא עוצרים את המחלה. סיבה מרכזית לכך היא פשוטה להפליא: קשה מאוד להעביר תרופות ולהשאיר אותן בחלקים המתאימים של המפרק. סקירה זו חקרה כיצד מולקולות זעירות הנקראות פפטידים ניתנות לעיצוב מותאם כדי לשאת תרופות עמוק לרקמות המושפעות במפרק — וכך להפוך הקלה קצרה לכאב לתיקון ממשי וארוך טווח.
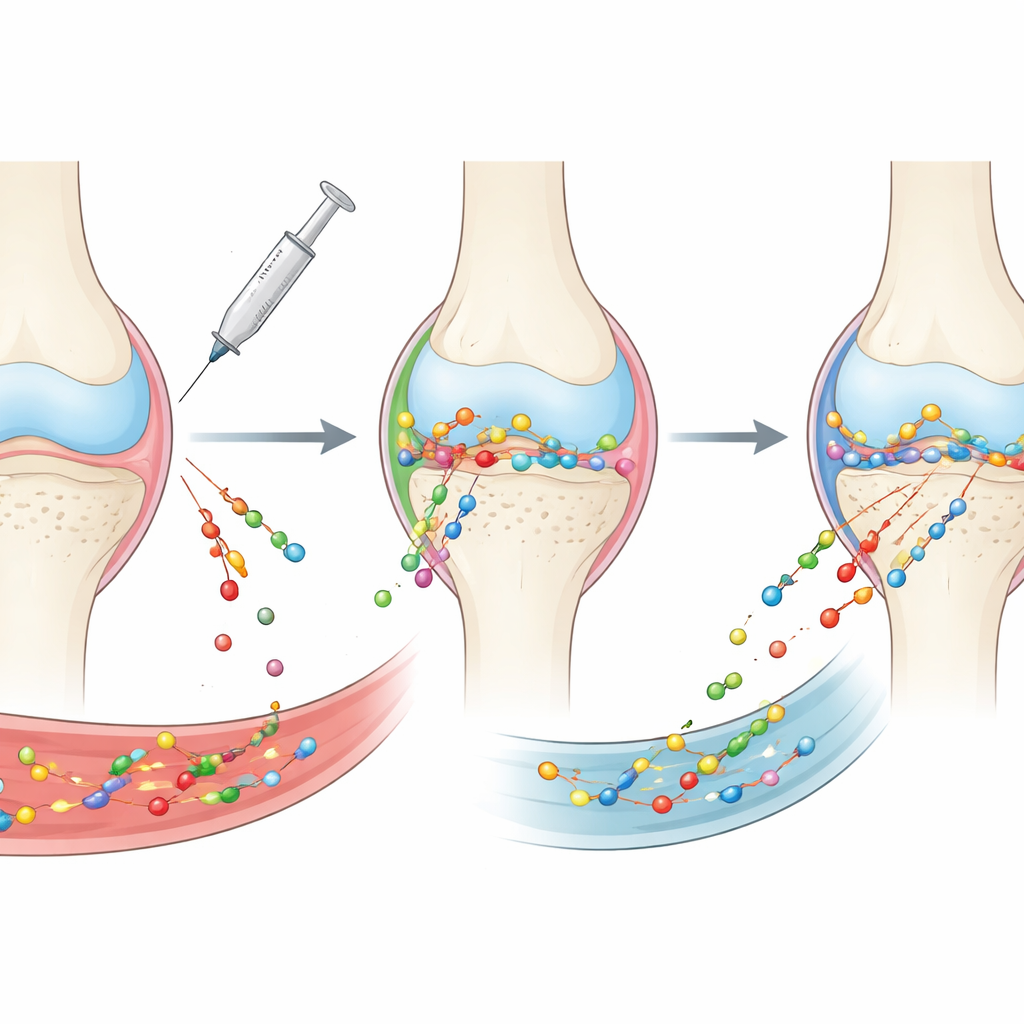
מדוע קשה כל כך לטפל בדלקת מפרקים שחיקתית
כיום לא רואים עוד את אוסטאוארטריטיס כ"בלאי" פשוט של הסחוס. זו מחלה של המפרק כולו, הכוללת את הסחוס, רירית הסינוביה, העצם התחתונה, הרצועות, כריות השומן והנוזל שמקיף אותן. לכל אחת מהרקמות הללו מבנה וכימיה משלה, שיוצרים יחד מסלול מחסומים מול כל תרופה. תרופות שמוחדרות לחלל המפרק נשטפות במהירות על ידי נוזל המפרק וכלי הדם, והן מתקשות לעבור דרך רקמה צפופה ופירלית. תרופות שניתנות דרך הפה או הוריד מגיעות לרירית העשירה בכלי דם ולעצם, אך רק אחוז זעום נכנס לסחוס ורובן נפגע בגוף. כתוצאה מכך, מולקולות מבטיחות רבות לא מגיעות לאתרים שבהם הן נדרשות או אינן נשארות שם מספיק זמן כדי להשפיע.
פפטידים כמכשירי ניווט חכמים
פפטידים — שרשרות קצרות של חומצות אמינו — ממוקמים בין תרופות קטנות לבין טיפולים מבוססי נוגדנים גדולים. מאחר שמדענים יכולים לכוונן את רצף החומצות אמינו כמעט יחידה אחר יחידה, ניתן להנדס פפטידים שיתפסו מטרות מאוד ספציפיות: סוג מסוים של קולגן, ג'ל עשיר בסוכרים, פני־תא, או אפילו גבישים מינרליים זעירים בעצם. המחברים מתארים שתי דרכים עיקריות בהן נמצא רצף "מכוון" כזה: סריקה רחבה של ספריות פפטידים עצומות, ותכנון רציונלי המבוסס על תכונות ידועות של רקמה, כגון המטען הכולל שלה. לאחר זיהוי, ניתן להצמיד את פפטידים הניווט הללו לתרופות, לנאנו־חלקיקים או לנושאים ביולוגיים כמו אקסוזומים, ולהכוונתן אל הסחוס, הסינוביה או העצם התת־חלקתי ולסייע להן להישאר במקום.
להגיע לסחוס, לרירית ולעצם
הסחוס, הציפוי החלק בקצות העצמות, קשה במיוחד להגיע אליו משום שהוא צפוף וחסר כלי דם. כאן פפטידים שמזהים את מבני הבניין העיקריים של הסחוס מועילים. חלקם נקשרים לסיבי קולגן שנותנים לסחוס את חוזקו; אחרים מנצלים את המטען השלילי החזק של הרקמה באמצעות רצפים בעלי מטען חיובי שנמשכים ונשמרים בה כמו מגנטים. נשאים אלה יכולים לגרור חלבונים אנטי‑דלקתיים, גורמי גדילה שמעודדים שיקום, סוכני הדמיה או אפילו אקסוזומים נושאי גנים, ולאפשר לתרופות לחדור לעומק הסחוס ולהישאר שם במשך ימים. אסטרטגיות דומות חלות על רירית הסינוביה, שבה פפטידים ספציפיים מתמקדים בתאים דמויי פיברובלסט, בתאים חיסוניים או בכלי הדם החדשים הבלתי תקינים שמופיעים במחלה — וכך מרוכזות תרופות המרגיעות דלקת. בעצם שמתחת לסחוס, פפטידים יכולים להנחות טיפולים לתאים בוני‑עצם, לתאים מפרקי עצם או אל המינרל עצמו, ולסייע לאזן מחדש את עיצוב העצם שפעמים רבות מחמירה את האוסטאוארטריטיס.
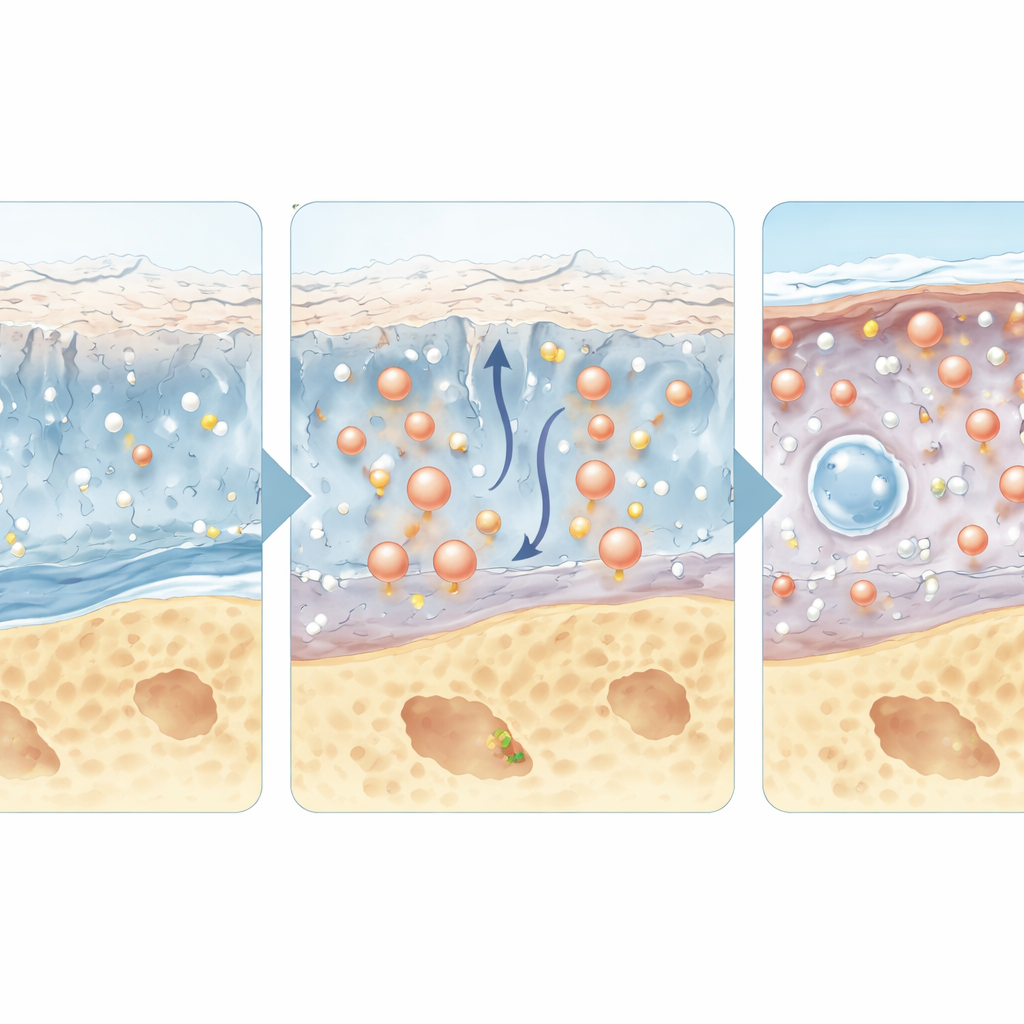
פפטידים שהם תרופות בעצמם
בנוסף לשמש כאותות ניווט, חלק מהפפטידים פועלים ישירות כתרופות. רשימה הולכת וגדלה של פפטידים הדומים להורמונים ולמולקולות סימון יכולה להפחית דלקת, להגן על תאי הסחוס מפגיעה, לעודד יצור מטריצה חדש או לדכא אותות כאב מהעצב במפרק. לדוגמה, גרסאות מוודאות של גלוקגון‑דומה‑1, שמשמשות כבר לטיפול בסוכרת והשמנת יתר, יכולות גם להגן על רקמות המפרק מפני סטרס דלקתי. פפטידים אחרים מחקים גורמים טבעיים שמעודדים גדילת סחוס או חוסמים מולקולות שמעוררות כאב. מועמדים רבים כאלה הראו תועלת במודלים בבעלי חיים, וחלקם מסתמכים על תרופות שכבר נמצאות בשימוש קליני במצבים אחרים, מה שהופך אותם לאטרקטיביים לשימוש מחדש באוסטאוארטריטיס.
להפוך טיפולי פפטיד לעמידים יותר ולבדוק אותם טוב יותר
מכשול מרכזי הוא שפפטידים בדרך כלל קצרים־זמן; אנזימים בדם ובנוזל המפרק מפצלים אותם במהירות, והכליות מסלקות אותם מהגוף. הסקירה מפרטת מספר פתרונות. כימאים יכולים להחליף חומצות אמינו לא־סטנדרטיות בנקודות פגיעות, לתפור פפטידים ללולאות בקשרי דיסולפיד כדי להקשיח את המבנה, או להצמידם לשותפים גדולים יותר כמו פולימרים, שומנים או חלבונים שמאטו פירוק וסילוק. במקביל, עיצוב וסימולציה בעזרת מחשב מתחילים לזרז את החיפוש אחר רצפים יציבים חדשים ולחזות כיצד הם נקשרים למטרותיהם. בצד הבדיקות, מודלים מתקדמים מסוג "מפרק על שבב" שמשלבים סחוס אנושי, סינוביה, עצם וזרימת נוזל מבוקרת עשויים להציע שדה מבחן ריאלי יותר מתרביות תאים מסורתיות או ניסויים בבעלי חיים, ולסייע לסנן עיצובים רבים לפני שמתקדמים לניסויים יקרים.
לקראת טיפולי מפרקים חכמים וארוכי טווח
ביחד, המחקרים שנסקרו במאמר זה מצביעים על עתיד שבו אוסטאוארטריטיס תטופל לא רק באמצעות ההרדמה של הכאב, אלא על‑ידי אספקה מדויקת של טיפולים חזקים לכל אחת מרקמות המפתח במפרק ולהשאירם שם מספיק זמן כדי לשנות את מהלך המחלה. פפטידים מותאמים אישית יכולים לשמש גם כתוויות יעד וגם כתרופות פעילות, לנווט בנוף המורכב של המפרק תוך הגבלת החשיפה לשאר הגוף. ככל שנדסת העמידות, העיצוב המונחה במחשב ומערכות בדיקה הרלוונטיות לאדם יתפתחו, אסטרטגיות מבוססות פפטידים עשויות סוף‑סוף לשחרר טיפולים המשנים את המחלה ושמשיבים תנועה ונוחות לאנשים החיים עם אוסטאוארטריטיס.
ציטוט: Hakim, B., Zhang, H., Selvadoss, A. et al. Peptide-based targeted drug delivery strategies for osteoarthritis treatment. npj Biomed. Innov. 3, 27 (2026). https://doi.org/10.1038/s44385-026-00082-w
מילות מפתח: אוסטאוארטריטיס, משלוח תרופות על בסיס פפטידים, מיקוד בסחוס, דלקת מפרקים, רפואה שיקומית