Clear Sky Science · ru
Композитная мембрана PGA-TMC/PTMC/nHA с синергетическими барьерными и остеогенными функциями для улучшенной регенерации дефектов кости
Помощь переломам: заживление становится лучше
Когда часть кости отсутствует — после удаления зуба, травмы или операции — организму трудно заполнить пустоту до того, как мягкие ткани вырастут и закроют пространство. Стоматологи и хирурги часто помещают тонкие барьерные пластины над такими дефектами, чтобы удерживать пространство открытым и дать возможность сформироваться новой кости. В этой работе предложена новая рассасывающаяся мембрана, спроектированная так, чтобы быть прочнее, служить дольше и активно стимулировать рост кости, что потенциально может улучшить результаты для пациентов, которым требуется восстановление кости в челюсти или черепе.
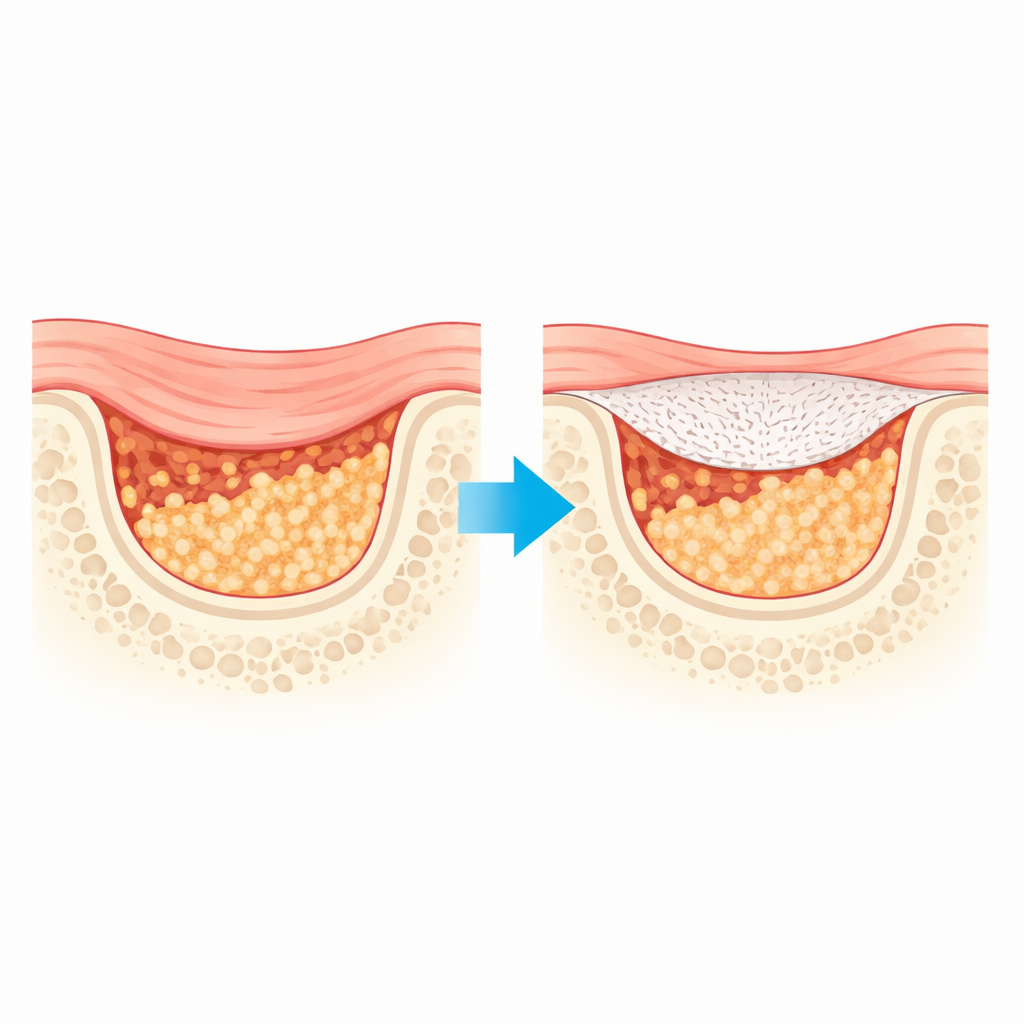
Почему существующие покрытия для кости не всегда эффективны
Стандартные барьерные мембраны, используемые при управляемой регенерации кости, действуют как временная крыша над строительной площадкой: они не дают быстрорастущим мягким тканям проникнуть, пока медленнее растущая кость заполняет пространство снизу. Многие клинически используемые сегодня пластины изготовлены из животных тканей. Несмотря на широкое применение, они могут разлагаться слишком быстро и не всегда достаточно прочны, чтобы дольше удерживать костные трансплантаты на месте в течение месяцев, необходимых для полного заживления. Существующие синтетические материалы решают некоторые из этих проблем, но часто становятся слабыми непредсказуемо по мере разрушения и мало способствуют активной стимуляции нового костеобразования.
Проектирование более разумного опорного каркаса
Чтобы решить эти проблемы, исследователи создали композитную мембрану под названием PGTTH с использованием техники получения тонких волокон. Материал сочетает три ключевых компонента: жесткий, но биоразлагаемый каркас, придающий листу основную прочность; более мягкий эластичный компонент, который разлагается медленно и равномерно, сохраняя форму мембраны; и мелкие частицы костеподобного минерала (нано-гидроксиапатит), схожие с природным минералом человеческой кости. Прядя их вместе в сетку нанофибров, полученный лист имитирует структуру собственной внеклеточной матрицы организма, предлагая как механическую поддержку, так и благоприятную поверхность для прикрепления клеток.
Оценка прочности, стабильности и биосовместимости
Команда вначале проверила, может ли новый материал физически выполнять требуемые функции. По сравнению с упрощёнными версиями, лишёнными одного или нескольких компонентов, полная мембрана PGTTH оказалась прочнее, более гибкой и лучше соответствующей жесткости губчатой кости, что снижает риск разрыва или чрезмерной изоляции зоны заживления от естественных нагрузок. В жидкой среде, имитирующей условия в организме, она незначительно набухала, но сохраняла толщину и форму. В течение восьми недель в лабораторном растворе PGTTH и связанная контрольная мембрана распадались медленно и равномерно, тогда как более простой материал разрушился раньше, что свидетельствует о его преждевременной недееспособности как барьера. Поверхность PGTTH также обеспечивала сбалансированную гидрофильность и гидрофобность, что важно для первичного оседания белков и клеток на материале.
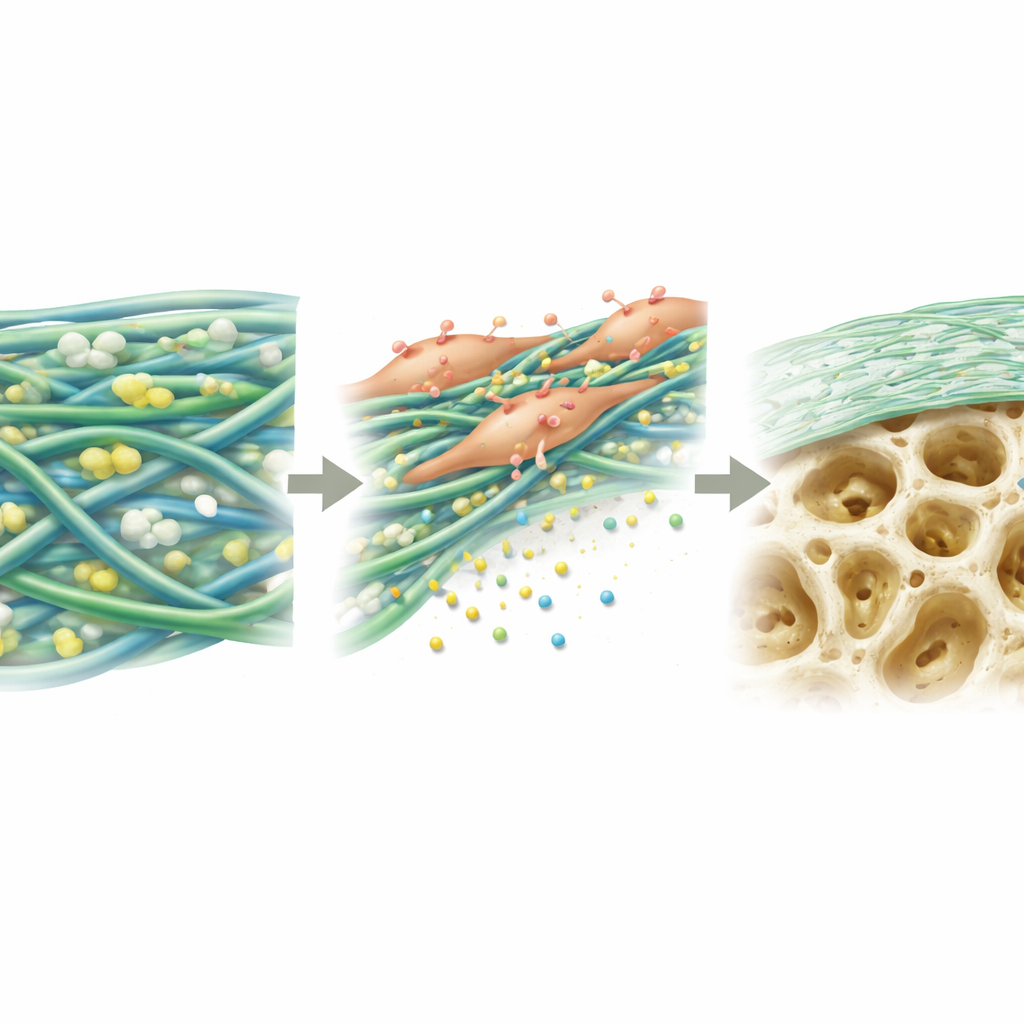
Стимулирование работы остеогенных клеток
Далее учёные изучили поведение стволовых клеток костного мозга на различных мембранах. На PGTTH клетки прикреплялись легче, сильнее распространялись и лучше размножались в течение нескольких дней по сравнению с другими тестируемыми материалами. В условиях, стимулирующих образование кости, в течение трёх недель клетки на PGTTH образовывали больше минеральных отложений — ранних строительных блоков кости — чем клетки на сравниваемых листах. На молекулярном уровне клетки усиливали активность нескольких ключевых генов и белков, вовлечённых в превращение стволовых клеток в остеобласты. Авторы связывают это с сочетанием свойств поверхности мембраны и медленного высвобождения ионов кальция и фосфата из костеподобных частиц, которые вместе дают биохимические сигналы, подталкивающие клетки к формированию новой кости.
Подтверждение регенерации кости in vivo
Чтобы проверить, переносятся ли эти преимущества на живой организм, команда создала большие круглые дефекты в черепах крыс — отверстия, которые сами по себе не зарастают. Некоторые дефекты оставляли открытыми, некоторые закрывали более простой мембраной, а другие — новой PGTTH. Через двенадцать недель высокоразрешающая 3D-визуализация показала, что дефекты, покрытые PGTTH, содержали значительно больше новой кости с более плотной и взаимосвязанной структурой, чем в других группах. Под микроскопом эти участки выглядели поразительно как зрелая, хорошо организованная кость со слоистой структурой и однородным минерализованным содержимым, в отличие от пятнистого, фиброзного или неполного восстановления, наблюдавшегося при использовании старого материала или при отсутствии мембраны.
Что это может значить для пациентов
В целом исследование показывает, что тщательно подобранная смесь прочных, но мягких полимеров и костеподобного минерала может делать больше, чем просто блокировать мягкие ткани: она способна активно направлять и ускорять собственный костеобразующий процесс организма. Хотя работы пока проводились на крысах и требуются дополнительные долгосрочные и механистические исследования, мембрана PGTTH, по-видимому, обеспечивает как стабильную «крышу», так и биологический «импульс», необходимые для сложного заживления кости. Если будущие исследования подтвердят её безопасность и эффективность у людей, такой материал может улучшить лечение дефектов челюстной кости, дентальные импланты и другие процедуры, зависящие от надёжной и высококачественной регенерации кости.
Цитирование: Wang, J., Wang, P., Wang, B. et al. PGA-TMC/PTMC/nHA composite membrane with synergistic barrier and osteogenic functions for enhanced bone defect regeneration. Sci Rep 16, 10815 (2026). https://doi.org/10.1038/s41598-026-45665-0
Ключевые слова: управляемая регенерация кости, биоактивные мембраны, инженерия костной ткани, нано-гидроксиапатит, электропряденые каркасы