Clear Sky Science · ar
غشاء مركب PGA-TMC/PTMC/nHA بوظائف حاجزية وتكوينية للعظام متكاملة لتعزيز تجدد عيوب العظام
مساعدة العظام المكسورة على الشفاء بشكل أفضل
عندما يفقد جزء من العظم — بعد خلع سن أو إصابة أو عملية جراحية — يكافح الجسم لإعادة بناء الفجوة قبل أن ينمو النسيج الرخو ويغلق المكان. كثيرًا ما يضع أطباء الأسنان والجراحون صفائح حاجزية رقيقة فوق هذه العيوب للحفاظ على الفراغ مفتوحًا بحيث يمكن أن يتكوّن عظم جديد. تعرض هذه الورقة غشاءً قابلًا للذوبان ومصممًا حديثًا ليكون أقوى، ويدوم لفترة أطول، ويشجع بنشاط نمو العظم، مما قد يحسّن النتائج للمرضى الذين يحتاجون إلى إعادة بناء العظم في الفك أو الجمجمة.
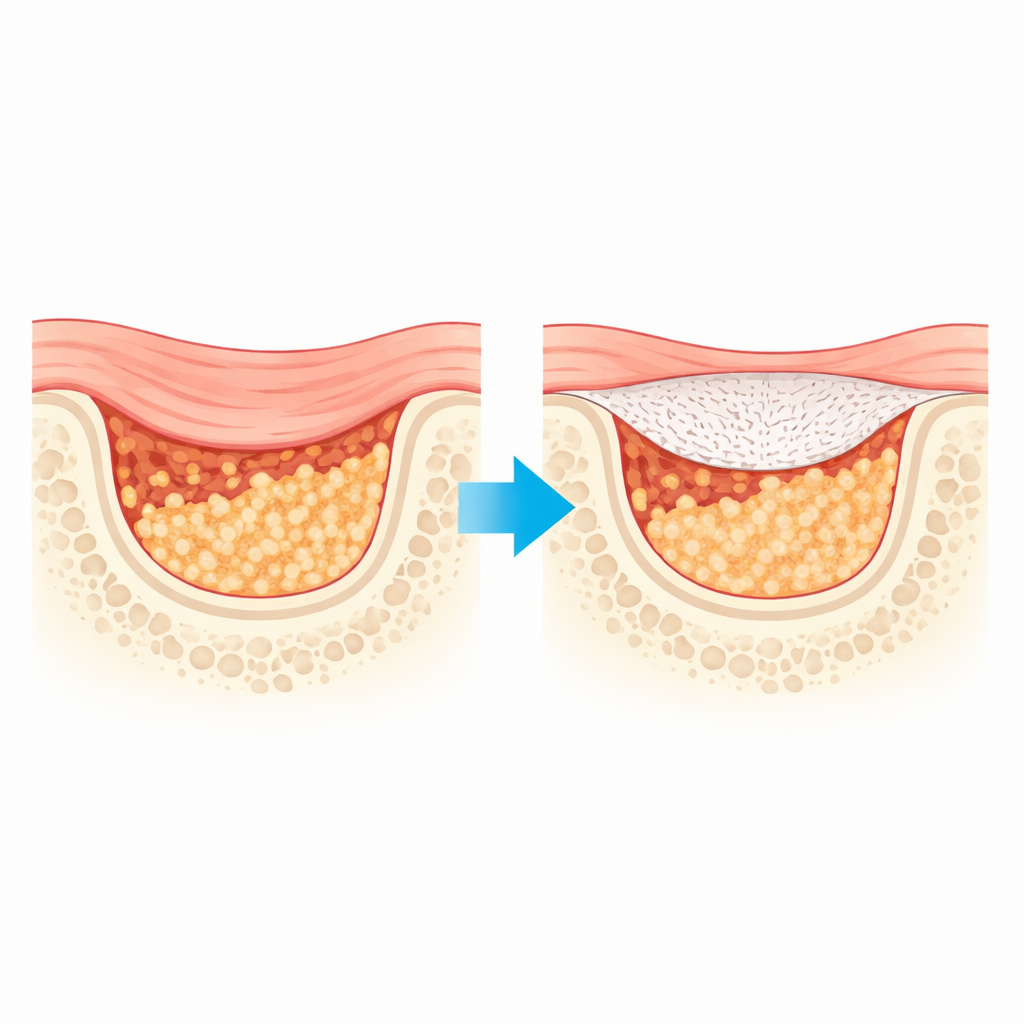
لماذا تغطيات العظام الحالية غير كافية
تعمل أغشية الحاجز القياسية المستخدمة في توجيه تجدد العظام مثل الأسقف المؤقتة لموقع بناء: تمنع غزو النسيج الرخو الذي ينمو بسرعة بينما يملأ العظم الأبطأ النمو الفراغ من تحته. العديد من الصفائح المستخدمة سريريًا اليوم مصنوعة من أنسجة حيوانية. وبالرغم من قبولها الواسع، فقد تتحلل بسرعة كبيرة وقد لا تكون قوية بما يكفي للحفاظ على ترقيع العظم الدقيق في مكانه خلال الأشهر المطلوبة للشفاء الكامل. تحل المواد الاصطناعية الشبيهة بالبلاستيك بعض هذه المشكلات لكنها غالبًا ما تضعف بشكل غير متوقع أثناء تحللها ولا تفعل الكثير لتحفيز نمو عظم جديد بنشاط.
تصميم دعامة ذكية أفضل
لمعالجة هذه المشكلات، أنشأ الباحثون غشاءً مركبًا أطلقوا عليه اسم PGTTH باستخدام تقنية غزل الألياف الدقيقة. يجمع المادّة بين ثلاثة مكونات رئيسية: عمود فقري قابل للتحلل لكنه صلب يوفر للقِطعة قوتها الأساسية؛ مكوّن أكثر ليونة ومرونة يتحلل ببطء وبشكل مستقيم للحفاظ على شكل الغشاء؛ وجسيمات دقيقة من معدن شبيه بالعظم (نانو-هيدروكسي أباتيت) تشبه المعدن الطبيعي في العظم البشري. عند غزلها معًا في شبكة من الألياف النانوية، يحاكي الصفيح الناتج بنية المصفوفة الداعمة في الجسم حول الخلايا، مقدّمًا دعمًا ميكانيكيًا وسطحًا مناسبًا لتعلق الخلايا.
اختبار القوة والثبات وملاءمة الخلايا
تحقق الفريق أولًا مما إذا كانت المادة الجديدة يمكن أن تؤدي فعليًا كما هو مطلوب. مقارنةً بالإصدارات الأبسط التي تفتقر إلى واحد أو أكثر من المكونات، كان غشاء PGTTH الكامل أقوى وأكثر مرونة وأكثر تطابقًا مع صلابة العظم الإسفنجي، مما يقلل من خطر تمزقه أو منعه المفرط للقوى الطبيعية عن منطقة الشفاء. في ظروف سائلة مشابهة للجسم، تورم بشكل معتدل لكنه حافظ على سمكه وشكله. على مدى ثمانية أسابيع في محلول مخبري، تحلّل PGTTH وغشاء ضابط ذي صلة ببطء وبشكل منتظم، بينما انهارت مادة أبسط في وقت أبكر، ما يوحي بأنها ستفشل مبكرًا كحاجز. كما أن سطح PGTTH حقق توازنًا بين جذب الماء ومقاومته، وهو أمر مهم لكيفية ارتكاز البروتينات والخلايا على المادة في البداية.
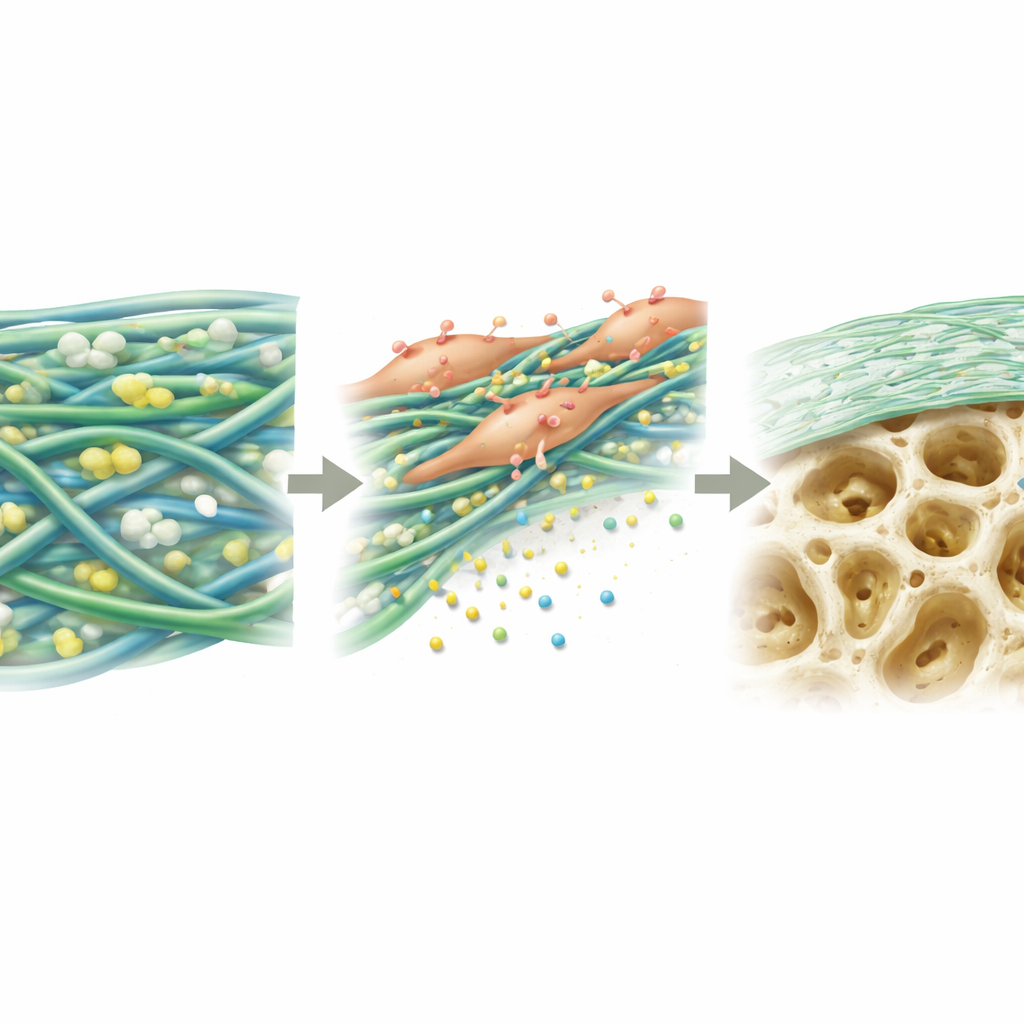
تشجيع خلايا تكون العظم على أداء وظيفتها
بعد ذلك، فحص العلماء سلوك خلايا جذعية نقي العظم على الأغشية المختلفة. على PGTTH، علّقت الخلايا بسهولة أكبر، وانتشرت بشكل أوسع، وتكاثرت أفضل على مدى عدة أيام مقارنةً بالمواد الأخرى المختبرة. على مدار ثلاثة أسابيع في ظروف محفزة لتكوين العظم، أنتجت الخلايا على PGTTH رواسب معدنية أكثر — اللبنات الأولى لتكوين العظم — مقارنةً بالخلايا على الصفائح المعيارية. على المستوى الجزيئي، ضاعفت الخلايا نشاط عدة جينات وبروتينات رئيسية متورطة في تحويل الخلايا الجذعية إلى خلايا مكوّنة للعظم. يعزو المؤلفون ذلك إلى مزيج من خصائص سطح الغشاء والإطلاق البطيء لأيونات الكالسيوم والفوسفات من الجسيمات الشبيهة بالعظم، التي ترسل معًا إشارات كيميائية حيوية تدفع الخلايا نحو بناء عظم جديد.
إثبات إصلاح العظم في حيوانات حية
للتحقق مما إذا كانت هذه المزايا تتحول إلى شفاء حقيقي، أحدث الفريق عيوبًا دائرية كبيرة في جماجم الجرذان — ثقوب لن تملأ ذاتيًا بطبيعة الحال. تُركت بعض العيوب مكشوفة، وغطيت بعضها بغشاء أبسط، وغطيت أخرى بصفحة PGTTH الجديدة. بعد اثني عشر أسبوعًا، أظهرت صور ثلاثية الأبعاد عالية الدقة أن العيوب المغطاة بـ PGTTH احتوت على عظم جديد أكثر بكثير وبنية أكثر كثافة وترابطًا من مجموعات الاختبار الأخرى. تحت المجهر، بدات هذه المناطق شبيهة بشكل لافت للعظم الناضج والمنظم جيدًا، ببنية طبقية ومحتوى معدني موحّد، بدلاً من الإصلاح البقعي أو الليفي أو غير المكتمل الذي لوحظ مع المادة الأقدم أو دون غشاء على الإطلاق.
ما الذي قد يعنيه هذا للمرضى
بشكل عام، تُظهر الدراسة أن مزيجًا مضبوطًا بعناية من بلاستيكيات قوية لكنها لطيفة ومعدن شبيه بالعظم يمكنه أن يفعل أكثر من مجرد حجز النسيج الرخو: يمكنه توجيه وتسريع عملية بناء العظم التي يقوم بها الجسم بنفسه. ورغم أن العمل أُجري حتى الآن على الجرذان ولا تزال هناك حاجة إلى دراسات أطول أجلاً وأكثر تفصيلًا في الآليات، يبدو أن غشاء PGTTH يوفر كلًا من "السقف" المستقر و"الدفع" البيولوجي الذي يتطلبه الشفاء العظمي المعقّد. إذا أكدت الأبحاث المستقبلية سلامته وفعاليته في البشر، فقد تُحسّن هذه المادة علاجات إصلاح عظم الفك، وزرعات الأسنان، وإجراءات أخرى تعتمد على تجدد عظمي موثوق وعالي الجودة.
الاستشهاد: Wang, J., Wang, P., Wang, B. et al. PGA-TMC/PTMC/nHA composite membrane with synergistic barrier and osteogenic functions for enhanced bone defect regeneration. Sci Rep 16, 10815 (2026). https://doi.org/10.1038/s41598-026-45665-0
الكلمات المفتاحية: توجيه تجدد العظام, أغشية نشطة حيوياً, هندسة نسيج العظام, نانو-هيدروكسي أباتيت, هياكل مسداة بالحلول الكهربائية