Clear Sky Science · ru
Трансплантация фекальной микробиоты плюс иммунотерапия при метастатическом раке почки: фазa 1 исследования PERFORM
Почему кишечник может иметь значение при лечении рака почки
Иммунотерапия изменила подход к лечению распространённого рака почки, давая некоторым пациентам дополнительные годы жизни. Но эти мощные препараты также могут активировать иммунную систему против здоровых органов, вызывая серьёзные, иногда угрожающие жизни побочные эффекты. В этом исследовании стоит, на первый взгляд, простой вопрос с большими последствиями: если сначала «сбросить» микробиом кишечника, приняв тщательно отобранный донорский материал в капсуле, можно ли сделать иммунотерапию одновременно безопаснее и эффективнее?
Новое применение звучащего непривычно метода
В исследовании PERFORM тестировали подход, называемый трансплантацией фекальной микробиоты (ФМТ), у пациентов с метастатическим почечно-клеточным раком — наиболее распространённой формой распространённого рака почки. Вместо традиционной ФМТ через колоноскопию пациенты проглатывали замороженные капсулы, приготовленные из кала тщательно отобранных здоровых доноров. Двадцать пациентов, не получавших предыдущей системной терапии, приняли три курса таких капсул, а затем начали стандартные схемы на основе иммунотерапии, например комбинированные ингибиторы контрольных точек или иммунотерапию в сочетании с таргетными препаратами. Главным вопросом была безопасность — не приведёт ли добавление донорских микроорганизмов к неприемлемым рискам при одновременном применении мощных иммунных препаратов?
Безопасность, побочные эффекты и первые признаки пользы
Хорошая новость в том, что сама ФМТ показалась безопасной. Лишь у одного пациента возник лёгкий желудочно-кишечный симптом, явно связанный с приёмом капсул. Более серьёзные иммунно-опосредованные побочные эффекты — такие как колит, кожная сыпь, артрит или гормональные нарушения — соответствовали ожидаемому профилю при применении самих иммунотерапевтических препаратов. У половины пациентов наблюдались тяжёлые (3-й степени) иммунные токсичности, но ни у кого не возникли наиболее опасные события 4-й или 5-й степени, и неожиданных осложнений не выявлено. В части пользы: среди 18 пациентов с измеримыми опухолями у 9 отмечалось значительное уменьшение размеров опухоли, а у 2 — полная ремиссия. Примечательно, что большинство пациентов с ответом на лечение не переносили тяжёлых иммунных побочных эффектов, что даёт основание полагать: хорошо настроенный микробиом может помочь достичь компромисса — сильного противоопухолевого эффекта при меньших сопутствующих повреждениях.
Кишечное сообщество как балансирующий механизм
Чтобы понять, почему некоторые пациенты переносили лечение лучше, исследователи отслеживали микробов, молекулы и иммунные клетки в крови и кале в течение десяти недель. Пациенты, избежавшие тяжёлых побочных эффектов, развивали более разнообразные сообщества кишечных микроорганизмов после ФМТ и сохраняли это разнообразие со временем. Их микробные профили становились более похожими на профили здоровых доноров — не только по наличию видов, но и по их функциональным возможностям, в особенности по способности вырабатывать противовоспалительные соединения, такие как короткоцепочечные жирные кислоты. У этих пациентов также сохранялись более высокие уровни некоторых циркулирующих метаболитов, включая витамин A, определённые аминокислоты и молекулы, связанные с энергетическим обменом — все они ранее ассоциировались с лучшей регуляцией иммунитета и реакциями на стресс. В совокупности этот паттерн указывает на то, что стабильная, функционально богатая экосистема кишечника может смягчать воспалительные всплески, вызванные иммунотерапией, одновременно поддерживая её противораковый эффект.
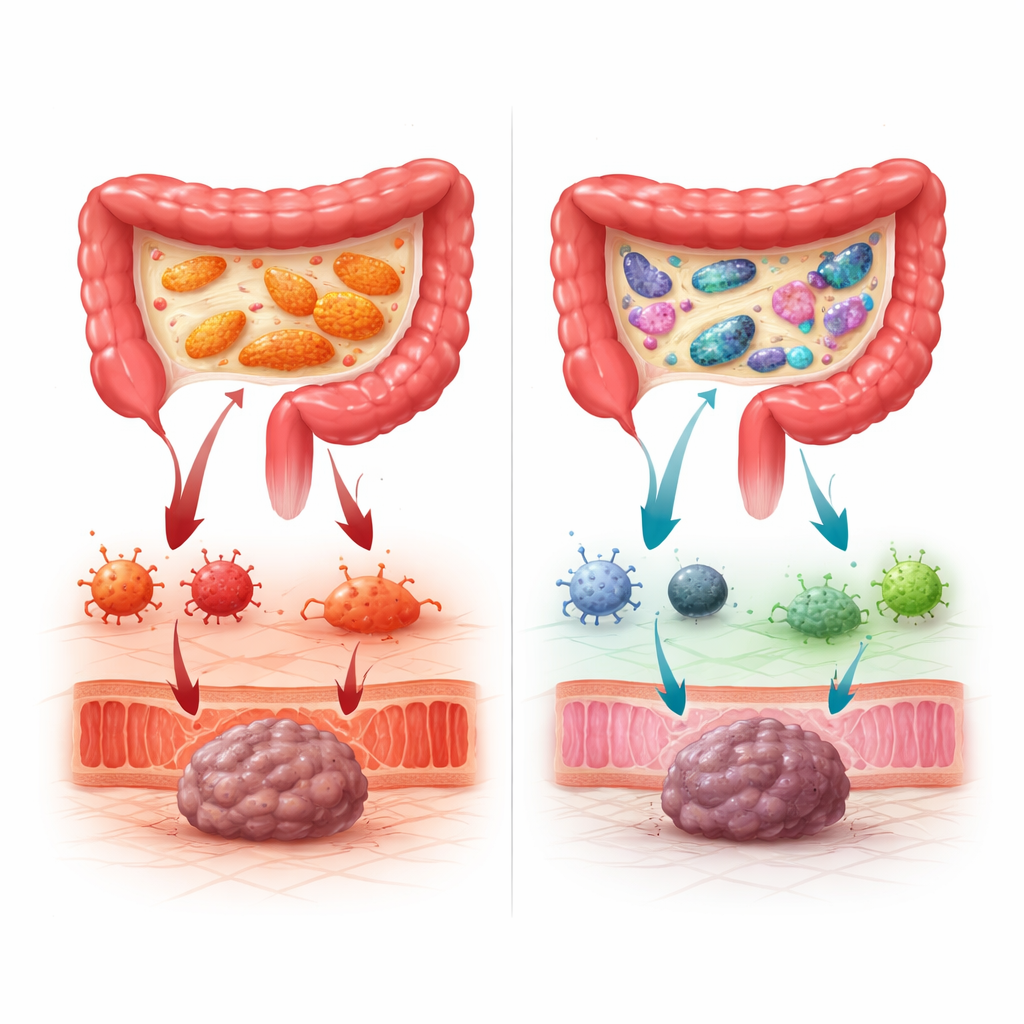
Когда одна бактерия нарушает равновесие
Не все бактерии оказались полезными. Команда выделила один вид в частности — Segatella copri — который становился проблемой при превышении определённого порога роста. Пациенты с высокими уровнями этого микроорганизма после ФМТ значительно чаще развивали тяжёлый иммунно-опосредованный колит и другие токсичности, особенно при лечении комбинацией ипилимумаба и ниволумаба. Многие из этих пациентов также не отвечали на терапию. Важно, что не имело значения, пришёл ли S. copri с донорским материалом или уже присутствовал у пациента в низких концентрациях: если условия позволяли ему «процвести», риск токсичности и резистентности возрастал. Высокие уровни S. copri связывались с кровяным «отпечатком» воспаления и иммунными профилями, показывающими чрезмерную активность цитотоксических Т-клеток при снижении регуляторных клеток и защитных натуральных киллеров, что свидетельствует о потере внутреннего контроля и баланса.
Что это означает для будущей онкологической помощи
Проще говоря, исследование показывает: формирование микробиома кишечника до и во время иммунотерапии может повлиять на то, будет ли иммунная система эффективно бороться с раком, не атакуя при этом сам организм. Введение тщательно подобранной смеси здоровых микроорганизмов в виде капсул ФМТ оказалось безопасным в этом небольшом исследовании и ассоциировалось с лучшими ответами и меньшей частотой тяжёлых побочных эффектов при условии, что пересаженное сообщество оставалось разнообразным, противовоспалительным и функционально устойчивым. В то же время полученные данные предостерегают: определённые бактерии, такие как S. copri, и микробные черты, способствующие воспалению, могут склонить пациента к опасной токсичности и плохим исходам. Хотя нужны более масштабные исследования, PERFORM указывает на будущее, в котором онкологи смогут скринировать доноров и пациентов по микробиому, избирательно усиливать защитные виды и избегать рискованных — используя кишечник как мощный рычаг для тонкой настройки иммунотерапии рака.
Цитирование: Fernandes, R., Jabbarizadeh, B., Rajeh, A. et al. Fecal microbiota transplantation plus immunotherapy in metastatic renal cell carcinoma: the phase 1 PERFORM trial. Nat Med 32, 1325–1336 (2026). https://doi.org/10.1038/s41591-025-04183-8
Ключевые слова: метастатический рак почки, трансплантация фекальной микробиоты, микробиом кишечника, ингибиторы иммунных контрольных точек, токсичность лечения