Clear Sky Science · it
Trapianto di microbiota fecale più immunoterapia nel carcinoma renale metastatico: lo studio di fase 1 PERFORM
Perché il tuo intestino potrebbe avere importanza nel trattamento del tumore al rene
L’immunoterapia ha rivoluzionato il modo in cui i medici trattano il cancro renale avanzato, offrendo ad alcuni pazienti anni di vita in più. Ma questi farmaci potenti possono anche scatenare il sistema immunitario contro organi sani, provocando effetti collaterali gravi e talvolta letali. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: se prima «azzeriamo» il microbioma intestinale usando feci di donatore attentamente selezionate in capsule, possiamo rendere l’immunoterapia sia più sicura sia più efficace?
Un nuovo impiego per un trattamento dal nome insolito
Lo studio PERFORM ha testato un approccio chiamato trapianto di microbiota fecale, o FMT, in persone con carcinoma renale metastatico, la forma più comune di cancro renale avanzato. Invece del tradizionale FMT somministrato via colon, i pazienti hanno ingerito capsule congelate ottenute dalle feci donate da volontari sani sottoposti a rigorosi controlli. Venti pazienti, ancora privi di trattamenti sistemici, hanno assunto tre cicli di queste capsule e poi hanno iniziato regimi standard a base di immunoterapia, come la combinazione di due inibitori dei checkpoint immunitari o l’immunoterapia associata a farmaci mirati. L’obiettivo principale era la sicurezza: aggiungere microbi di donatore a farmaci immunoterapici potenti avrebbe creato rischi inaccettabili?
Sicurezza, effetti collaterali e primi benefici
La buona notizia è che l’FMT di per sé è sembrato sicuro. Solo un paziente ha manifestato un lieve disturbo intestinale chiaramente collegabile alle capsule. Gli effetti collaterali immuno-correlati più seri — come colite, eruzione cutanea, artrite o problemi ormonali — corrispondevano a quanto normalmente atteso dai soli farmaci immunoterapici. Metà dei pazienti ha sperimentato tossicità immunitarie gravi (grado 3), ma nessuno ha sviluppato eventi di grado 4 o 5 e non sono emerse complicazioni inattese. Sul fronte dei benefici, tra i 18 pazienti con tumori misurabili, 9 hanno mostrato una riduzione significativa del cancro e 2 hanno ottenuto risposte complete. Colpisce che la maggior parte dei pazienti responder non abbia sofferto gravi effetti immunitari, suggerendo che un microbioma ben equilibrato potrebbe consentire il meglio di entrambi i mondi: forte attività anti-tumorale con meno danni collaterali.
La comunità intestinale come atto di equilibrio
Per capire perché alcuni pazienti tolleravano meglio il trattamento, i ricercatori hanno monitorato microbi, molecole e cellule immunitarie nel sangue e nelle feci per dieci settimane. I pazienti che evitarono gravi effetti collaterali hanno sviluppato comunità intestinali più diverse dopo l’FMT e le hanno mantenute nel tempo. I loro profili microbici sono diventati più simili a quelli dei donatori sani, non solo nella presenza di specie ma anche nelle funzioni che quei microbi possono svolgere — in particolare la capacità di produrre composti anti-infiammatori come gli acidi grassi a catena corta. Questi pazienti hanno anche mantenuto livelli più alti di certi metaboliti circolanti, tra cui vitamina A, specifici amminoacidi e molecole legate all’energia, tutti associati a una regolazione immunitaria e a risposte allo stress più sane. Nel complesso, questo schema suggerisce che un ecosistema intestinale stabile e ricco di funzioni può aiutare ad attutire gli shock infiammatori dell’immunoterapia pur sostenendo i suoi effetti antitumorali.
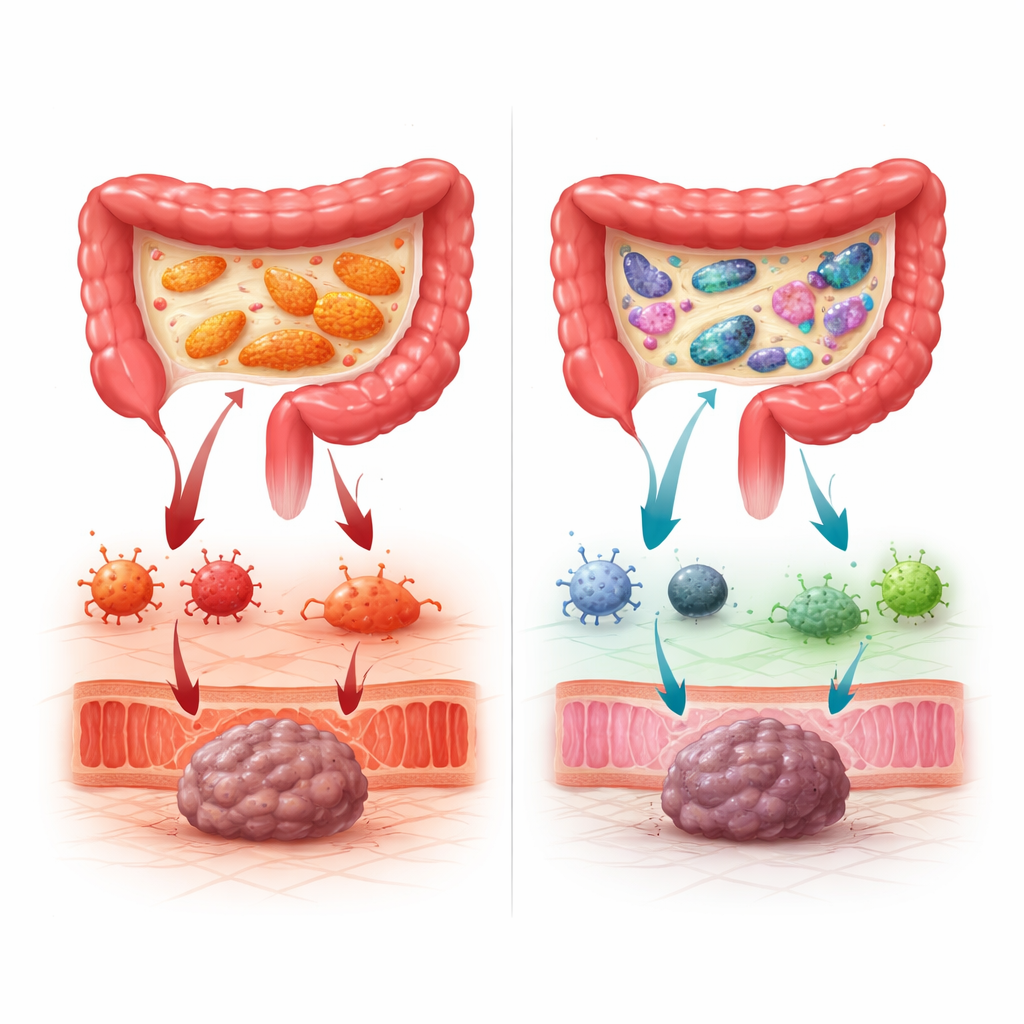
Quando un batterio fa pendere la bilancia
Non tutti i batteri sono stati utili. Il team ha identificato una specie in particolare, Segatella copri, che è diventata problematica quando cresceva oltre una certa soglia. I pazienti che si ritrovarono con alti livelli di questo microbo dopo l’FMT avevano molte più probabilità di sviluppare colite immuno-correlata grave e altre tossicità, specialmente quando trattati con la combinazione di ipilimumab e nivolumab. Molti di questi pazienti non risposero al trattamento. È importante notare che non importava se S. copri provenisse dal donatore o fosse già presente a bassi livelli nel paziente: se le condizioni permettevano la sua fioritura, aumentava il rischio di tossicità e resistenza. Alti livelli di S. copri erano associati a un «impronta» ematica di infiammazione e a modelli di cellule immunitarie che mostravano linfociti T citotossici iperattivi ma meno cellule regolatorie e cellule natural killer protettive, segnalando una perdita dei controlli interni.
Cosa significa per la cura oncologica futura
In termini semplici, questo studio suggerisce che plasmare il microbioma intestinale prima e durante l’immunoterapia può influenzare se il sistema immunitario combatte efficacemente il cancro senza attaccare l’organismo. Introdurre una miscela accuratamente selezionata di microbi sani tramite capsule di FMT è stato sicuro in questo piccolo trial ed è risultato associato a risposte migliori e a meno effetti collaterali gravi quando la comunità trapiantata restava diversificata, anti-infiammatoria e funzionalmente robusta. Allo stesso tempo, i risultati avvertono che batteri specifici come S. copri, e certi tratti microbici che promuovono l’infiammazione, possono spingere i pazienti verso tossicità pericolose e esiti sfavorevoli. Pur necessitando di trial più ampi, PERFORM indica un futuro in cui gli oncologi potrebbero selezionare donatori e pazienti in base al loro profilo microbico, potenziare selettivamente le specie protettive ed evitare quelle rischiose — usando l’intestino come una leva potente per calibrare l’immunoterapia oncologica.
Citazione: Fernandes, R., Jabbarizadeh, B., Rajeh, A. et al. Fecal microbiota transplantation plus immunotherapy in metastatic renal cell carcinoma: the phase 1 PERFORM trial. Nat Med 32, 1325–1336 (2026). https://doi.org/10.1038/s41591-025-04183-8
Parole chiave: carcinoma renale metastatico, trapianto di microbiota fecale, microbioma intestinale, inibitori dei checkpoint immunitari, tossicità del trattamento