Clear Sky Science · ru
Двойная эстерификация, катализируемая карбеном, обеспечивает энантиоселективную конформационную «закупорку» пилар[5]аренов
Формирование крошечных колец для «умных» материалов
Химики учатся лепить молекулы почти как часовые мастера формуют шестерёнки. В этом исследовании показано, как «зафиксировать» небольшую кольцевую молекулу в одной «рукообразной» конформации, используя простой катализатор и доступные ингредиенты. Поскольку такие кольца могут заключать другие молекулы, новый контроль над формой может повлиять на развитие сенсоров, материалов и медицинских инструментов.
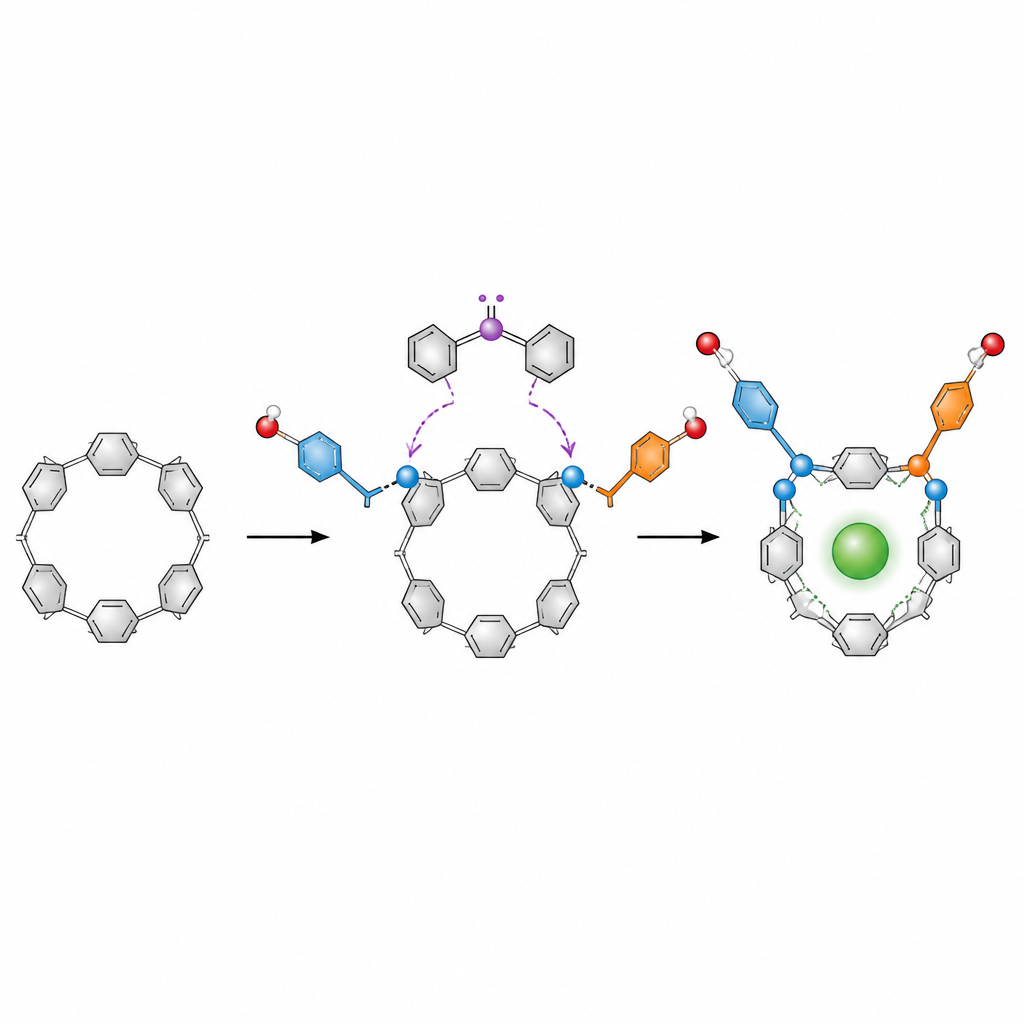
Почему форма кольца важна
Главными героями здесь выступают пилар[5]арены — кольца, напоминающие пончик, собранные из пяти повторяющихся ароматических звеньев. Эти кольца популярны в хост–гост химии, где они служат крошечными контейнерами для ионов, лекарств или красителей. На бумаге пилар[5]арен может принимать несколько зеркально-симметричных форм, между которыми он свободно переключается. Чтобы использовать их как точные инструменты, химикам нужно «заморозить» одну хиральную форму и обогатить одну зеркальную конфигурацию относительно другой, но существующие методы часто зависят от металлов, множества стадий и утомительного разделения смесей.
Безметалльный кратчайший путь к зафиксированным кольцам
Авторы разработали гораздо более простой подход на основе органокатализа, где реакции направляют малые органические молекулы вместо металлов. Они взяли диформильный пилар[5]арен — версию кольца с двумя реакционноспособными альдегидными группами. В присутствии хирального карбенового катализатора, окислителя и основания эти группы проходят двойную эстерификацию с ароматическими спиртами, такими как нафтолы. Каждая реакция присоединяет к кольцу эстерификационную «руку». После установки двух громоздких рук кольцо больше не может свободно переворачиваться, поэтому одна хиральная форма фиксируется и становится значительно предпочтительной.
Настройка зоны действия реакции
Путём систематического тестирования команда подобрала условия, обеспечивающие как высокие выходы, так и сильное предпочтение одной зеркальной формы. Они исследовали, как природа катализатора, растворителя, основания и окислителя влияет на результат, и обнаружили, что ацетат натрия в дихлорметане при умеренной температуре работает особенно хорошо. Процесс допускает широкий набор ароматических партнёров, включая нафтолы с электронно-донорами или акцепторами, а также разные фенолы. С помощью умелого стерического анализа они показали, что только заместители достаточной длины и громоздкости действительно препятствуют перевороту кольца, что объясняет, почему мелкие группы, такие как метил, не дают стабильных хиральных продуктов.
От простых колец к сложным гостям
Метод выходит за рамки простых строительных блоков. Исследователи успешно присоединили фрагменты из природных и биоактивных молекул, такие как эстрон и средство для снижения холестерина эзетимиб, при этом сохраняя высокий контроль над «ручностью». Они дополнительно продемонстрировали, что зафиксированные кольца выдерживают нагревание и химические модификации, не теряя хиральной чистоты. В граммовом масштабе ключевой продукт образуется практически в количественном выходе. Дополнительные реакции по оставшимся функциональным группам создают более сложные структуры, включая ротаксан, в котором гантелеобразная молекула продета через кольцо пилар[5]арена и зафиксирована громоздкими стопперами.
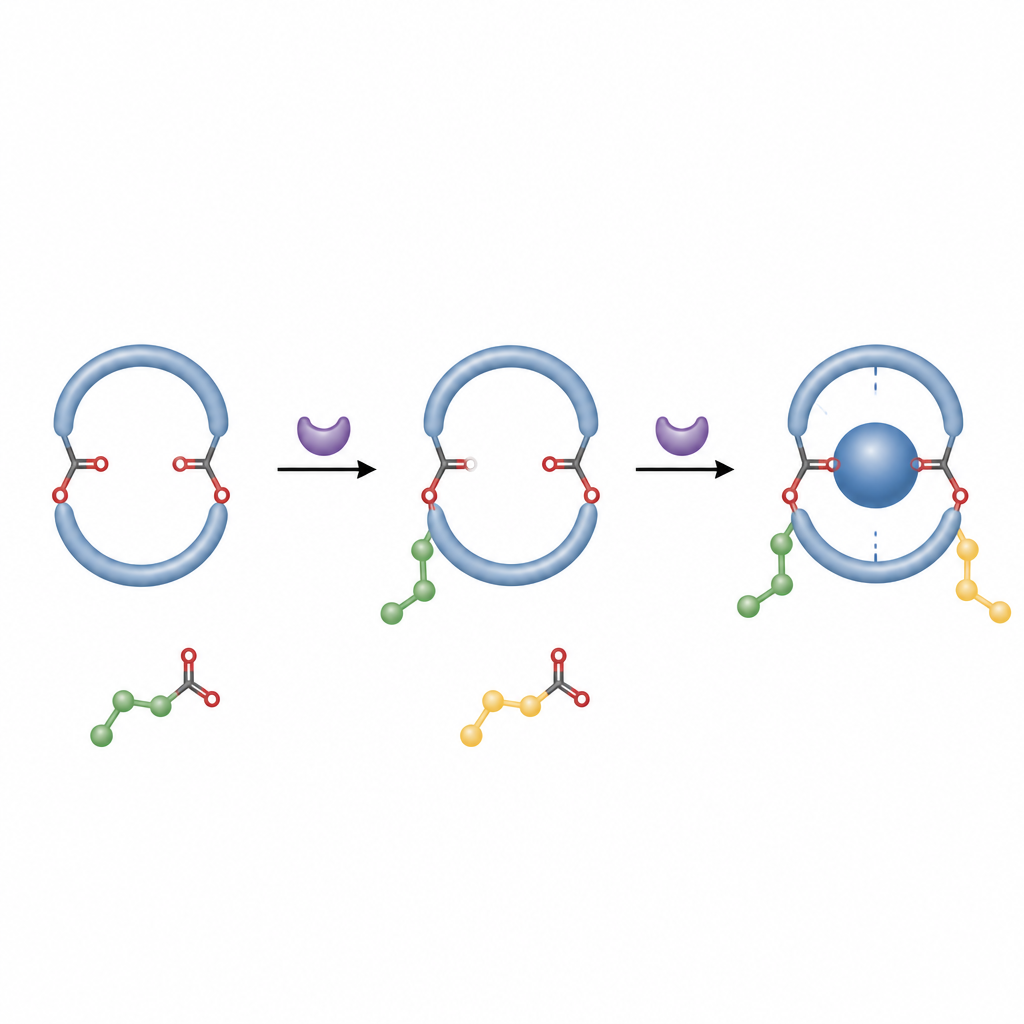
Что это значит для будущих молекулярных машин
Популярными словами, авторы нашли способ защёлкнуть молекулярное кольцо в фиксированную левую или правую позу с помощью простого безметалльного процесса. Это значительно упрощает подготовку чистых, однозначно сформованных хостов, которые могут предсказуемо удерживать другие молекулы. Такой контроль над «ручностью» и стабильностью важен для разработки отзывчивых материалов, хиральных сенсоров и молекулярных устройств, и эта простая двойная эстерификация предлагает практичный новый путь к таким продвинутым структурам.
Цитирование: Dočekal, V., Hladík, O., Lóška, L. et al. Carbene-catalyzed double esterification enables enantioselective conformational self-locking of pillar[5]arenes. Nat Commun 17, 4253 (2026). https://doi.org/10.1038/s41467-026-70809-1
Ключевые слова: пиларарены, органокатализ, хиральные хосты, эстерификация, супрамолекулярная химия