Clear Sky Science · pl
Katalizowana karbenem podwójna estryfikacja umożliwia enantioselektywne samozablokowanie konformacyjne pillar[5]arenów
Formowanie maleńkich pierścieni dla inteligentnych materiałów
Chemicy uczą się rzeźbić molekuły niemal jak zegarmistrzowie formują koła zębate. W tym badaniu pokazano, jak „zablokować” małą, pierścieniową cząsteczkę w jednej, zorientowanej jak dłoń formie, używając prostego katalizatora i powszechnych reagentów. Ponieważ takie pierścienie potrafią obejmować inne molekuły, ta nowa kontrola kształtu może mieć wpływ na przyszłe czujniki, materiały i narzędzia medyczne.
Dlaczego kształt pierścienia ma znaczenie
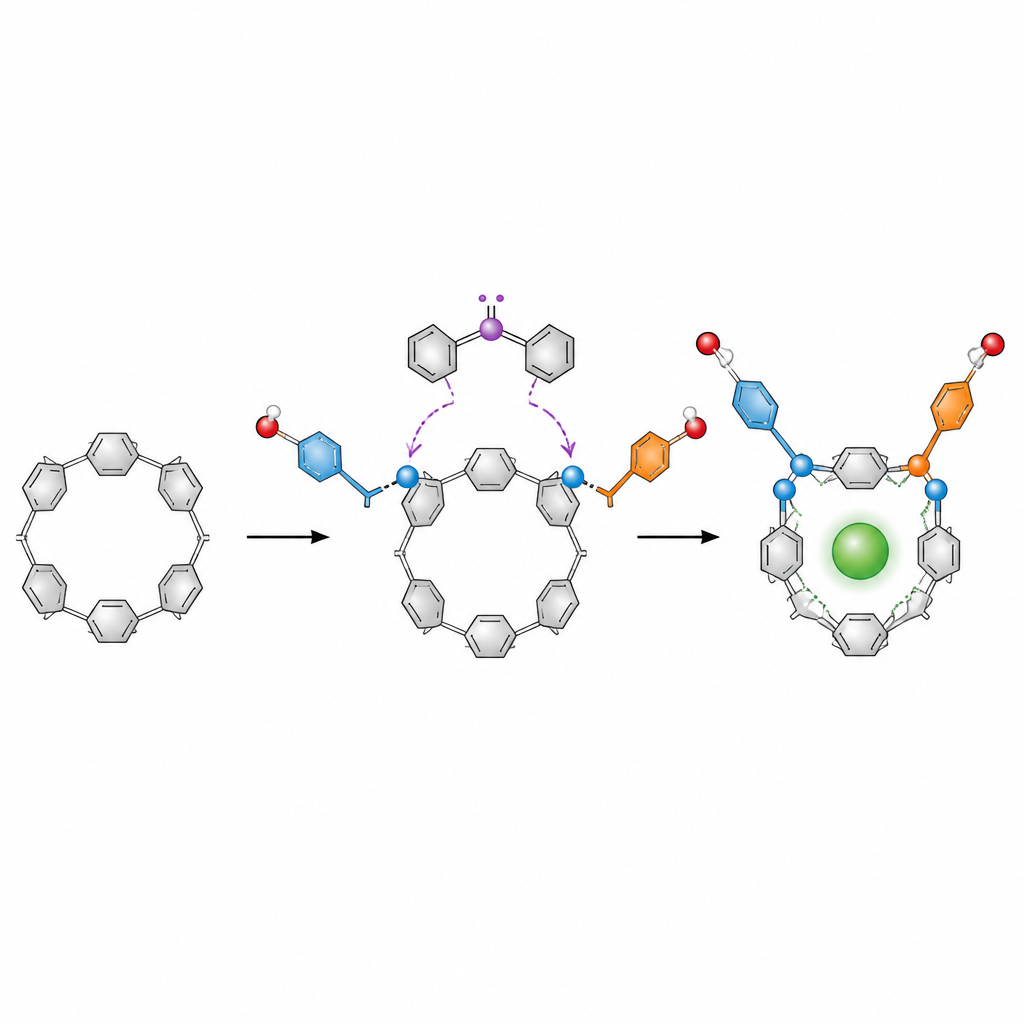
Gwiazdami tej pracy są pillar[5]areny, pierścieniopodobne struktury zbudowane z pięciu powtarzających się jednostek aromatycznych. Te pierścienie są popularne w chemii gospodarz–gość, gdzie działają jako maleńkie pojemniki dla jonów, leków czy barwników. W teorii pillar[5]arena może skręcać się do kilku form lustrzanych, które przemieniają się nawzajem. Aby użyć ich jako precyzyjnych narzędzi, chemicy muszą zamrozić jedną „ręczną” formę i wzbogacić jedną lustrzaną postać względem drugiej, jednak istniejące metody często opierają się na metalach, wielu etapach i żmudnym rozdziale mieszanin.
Metalowo‑wolny skrót do zablokowanych pierścieni
Autorzy opracowali znacznie prostsze podejście oparte na organokatalizie, która używa małych cząsteczek organicznych zamiast metali do kierowania reakcjami. Wyjściowym związkiem była diformylowana pillar[5]arena, wersja pierścienia z dwiema reaktywnymi grupami aldehydowymi. W obecności chiralnego katalizatora karbenowego, utleniacza i zasady, grupy te przeszły podwójną estryfikację z aromatycznymi alkoholami, takimi jak naftole. Każda reakcja przyłączała do pierścienia estrowe „ramię”. Gdy dwa masywne ramiona znalazły się na miejscu, pierścień nie mógł już swobodnie obracać się, w efekcie jedna forma chiralna została zablokowana i silnie preferowana.
Dopasowywanie zasięgu reakcji
Poprzez systematyczne testy zespół odkrył warunki dające zarówno wysokie wydajności, jak i silne uprzywilejowanie jednej lustrzanej postaci. Zbadali, jak natura katalizatora, rozpuszczalnika, zasady i utleniacza wpływa na wynik, i stwierdzili, że octan sodu w dichlorometanie w umiarkowanej temperaturze działa szczególnie dobrze. Proces toleruje wiele różnych aromatycznych partnerów, w tym naftole z grupami elektrono‑donorowymi lub elektronowo‑akceptorowymi oraz różnorodne fenole. Dzięki sprytnej analizie sterycznej wykazali, że tylko podstawnikidługie i wystarczająco masywne rzeczywiście zapobiegają przewracaniu się pierścienia, co wyjaśnia, dlaczego małe grupy, takie jak metylowe, nie dostarczają stabilnych chiralnych produktów.
Od prostych pierścieni do złożonych gości
Metoda wykracza poza proste cegiełki. Badacze z powodzeniem przyłączyli fragmenty pochodzące z naturalnych i bioaktywnych molekuł, takich jak estron czy lek obniżający poziom cholesterolu ezetymib, zachowując przy tym wysoką kontrolę „ręczności”. Dodatkowo wykazali, że zablokowane pierścienie wytrzymują temperaturę i chemiczne modyfikacje bez utraty czystości chiralnej. W skali gramowej kluczowy produkt powstaje w prawie ilościowości. Dalsze reakcje na pozostających grupach funkcyjnych tworzą bardziej skomplikowane struktury, w tym rotaksan, w którym cząsteczka o kształcie hantli jest przewleczona przez pierścień pillar[5]areny i zatrzymana przez masywne stopery.
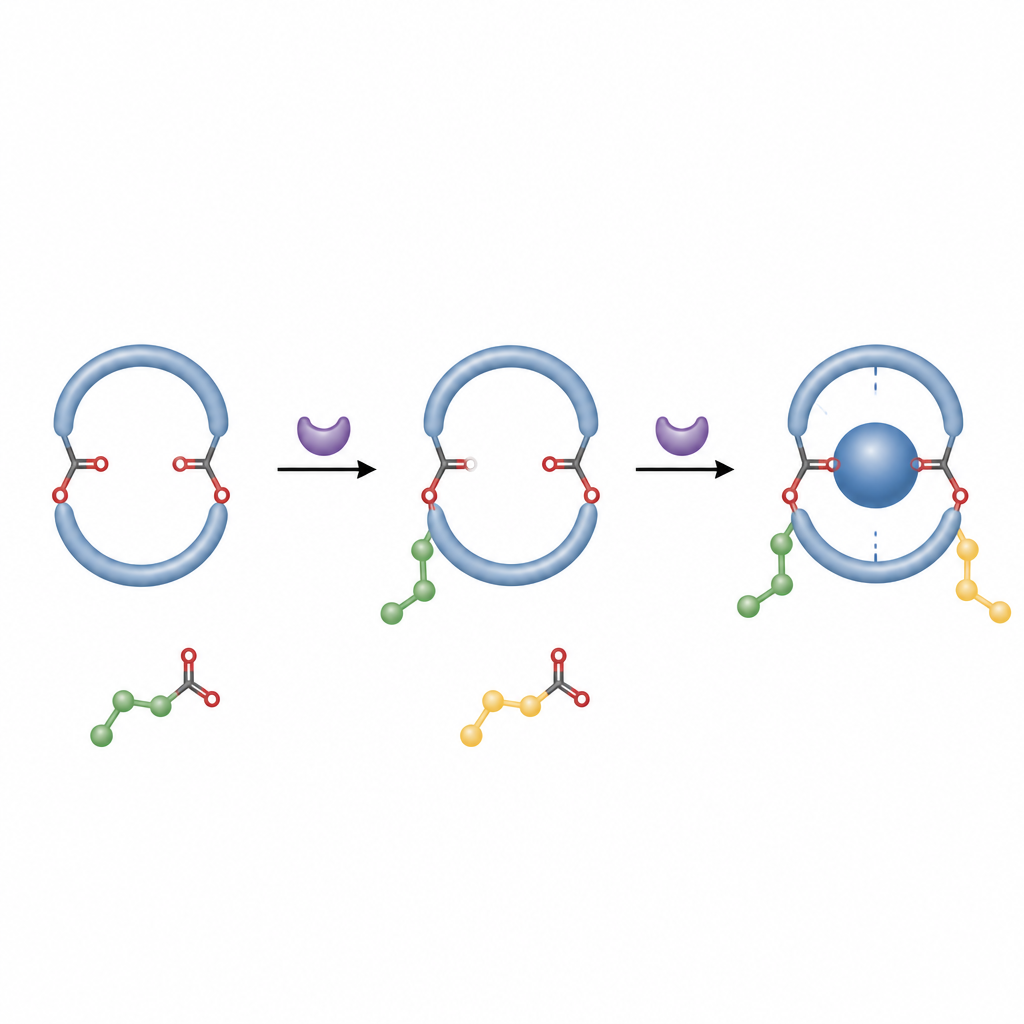
Co to oznacza dla przyszłych maszyn molekularnych
Mówiąc obrazowo, autorzy znaleźli sposób na zatrzaśnięcie molekularnego pierścienia w stałej, lewo‑ lub praworęcznej pozie, używając prostego, metalowo‑wolnego procesu. Ułatwia to przygotowanie czystych, zdefiniowanych kształtem gospodarzy, które mogą chwytać inne molekuły w przewidywalny sposób. Taka kontrola nad ręcznością i stabilnością jest istotna dla projektowania reaktywnych materiałów, chiralnych czujników i urządzeń molekularnych, a ta prostolinijna podwójna estryfikacja oferuje praktyczną nową drogę do tych zaawansowanych struktur.
Cytowanie: Dočekal, V., Hladík, O., Lóška, L. et al. Carbene-catalyzed double esterification enables enantioselective conformational self-locking of pillar[5]arenes. Nat Commun 17, 4253 (2026). https://doi.org/10.1038/s41467-026-70809-1
Słowa kluczowe: pillarareny, organokataliza, chiralne gospodarze, estryfikacja, chemia supramolekularna