Clear Sky Science · es
La doble esterificación catalizada por carbenos permite el auto-bloqueo conformacional enantioselectivo de pillar[5]arenos
Moldeando anillos diminutos para materiales inteligentes
Los químicos están aprendiendo a esculpir moléculas casi como relojeros que dan forma a engranajes. Este estudio muestra cómo «bloquear» una pequeña molécula en forma de anillo en una sola conformación enantiomérica, usando un catalizador simple e ingredientes comunes. Dado que dichos anillos pueden acunar otras moléculas, este nuevo control sobre la forma podría influir en sensores, materiales y herramientas médicas futuras.
Por qué importa la forma de un anillo
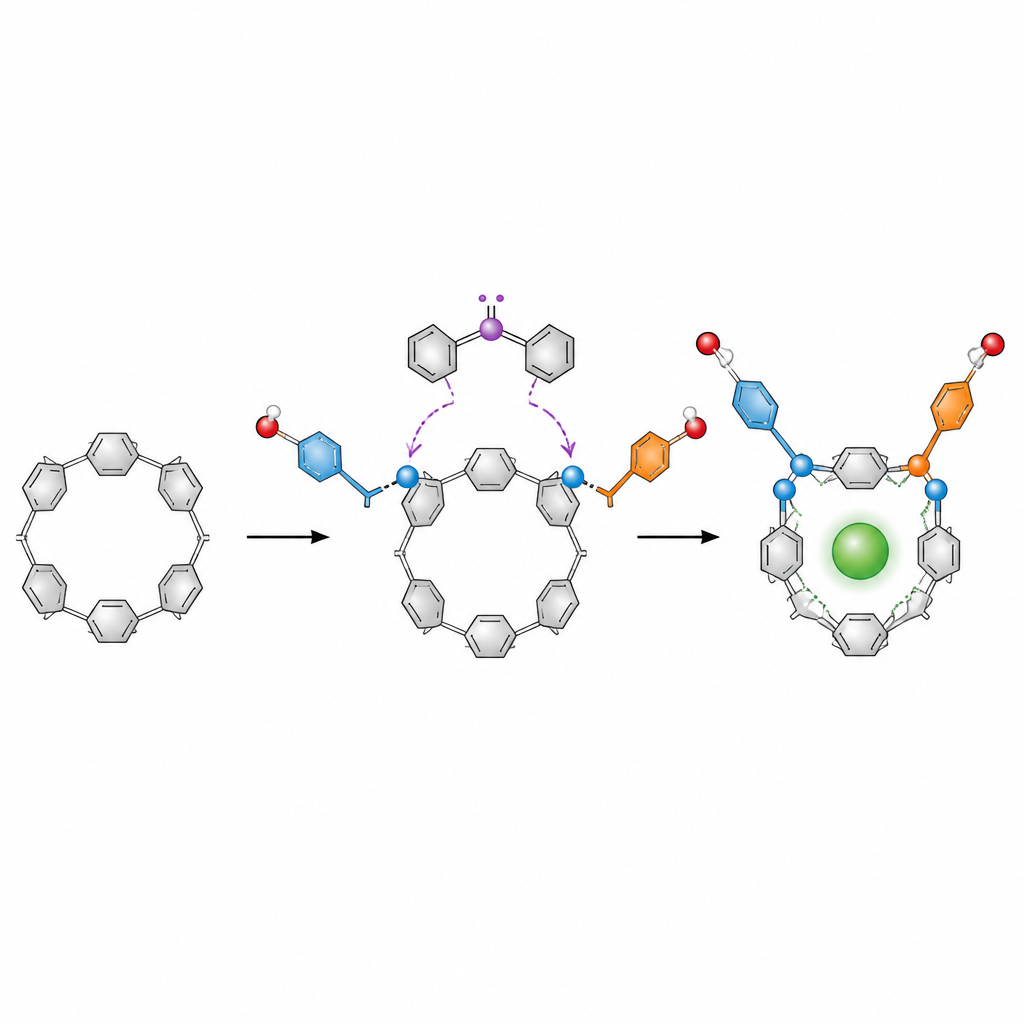
Las protagonistas son las pillar[5]arenas, anillos en forma de rosquilla construidos a partir de cinco unidades aromáticas repetidas. Estos anillos son populares en química hospedador-huésped, donde actúan como contenedores diminutos para iones, fármacos o colorantes. En teoría, una pillar[5]arena puede girar en varias formas镜espejo que se interconvierten. Para usarlas como herramientas precisas, los químicos deben congelar una conformación «de mano» y enriquecer una imagen especular sobre la otra, pero los métodos existentes a menudo dependen de metales, múltiples pasos y la tediosa separación de mezclas.
Un atajo sin metales hacia anillos bloqueados
Los autores diseñaron un enfoque mucho más simple basado en la organocatálisis, que utiliza pequeñas moléculas orgánicas en lugar de metales para dirigir las reacciones. Partieron de una pillar[5]arena diformilada, una versión del anillo con dos grupos aldehído reactivos. En presencia de un catalizador carbénico quiral, un oxidante y una base, estos grupos sufren una doble esterificación con alcoholes aromáticos como los naftoles. Cada reacción une un «brazo» éster al anillo. Una vez que dos brazos voluminosos están en su sitio, el anillo ya no puede girar libremente, por lo que una forma quiral queda bloqueada y fuertemente favorecida.
Ajustando el alcance de la reacción
Mediante pruebas sistemáticas, el equipo descubrió condiciones que proporcionan tanto altos rendimientos como una fuerte preferencia por una imagen especular. Examinaron cómo la naturaleza del catalizador, el disolvente, la base y el oxidante influye en el resultado, y encontraron que acetato de sodio en diclorometano a temperatura moderada funciona particularmente bien. El proceso tolera muchos socios aromáticos distintos, incluidos naftoles con grupos ricos o pobres en electrones y una variedad de fenoles. Usando un análisis estérico ingenioso, demostraron que solo los sustituyentes lo bastante largos y voluminosos impiden verdaderamente que el anillo se invierta, lo que explica por qué grupos pequeños como el metilo no dan productos chirales estables.
De anillos simples a huéspedes complejos
El método llega más allá de bloques de construcción simples. Los investigadores consiguieron unir fragmentos procedentes de moléculas naturales y bioactivas, como la estrona y el fármaco reductor del colesterol ezetimiba, sin perder el alto control de la «manitud». Además demostraron que los anillos bloqueados resisten el calor y las modificaciones químicas sin perder su pureza quiral. A escala de gramos, el producto clave se forma en rendimiento casi cuantitativo. Reacciones adicionales sobre grupos funcionales restantes generan estructuras más complejas, incluido un rotaxano, en el que una molécula en forma de mancuerna atraviesa el anillo de pillar[5]arena y queda atrapada por toberas voluminosas.
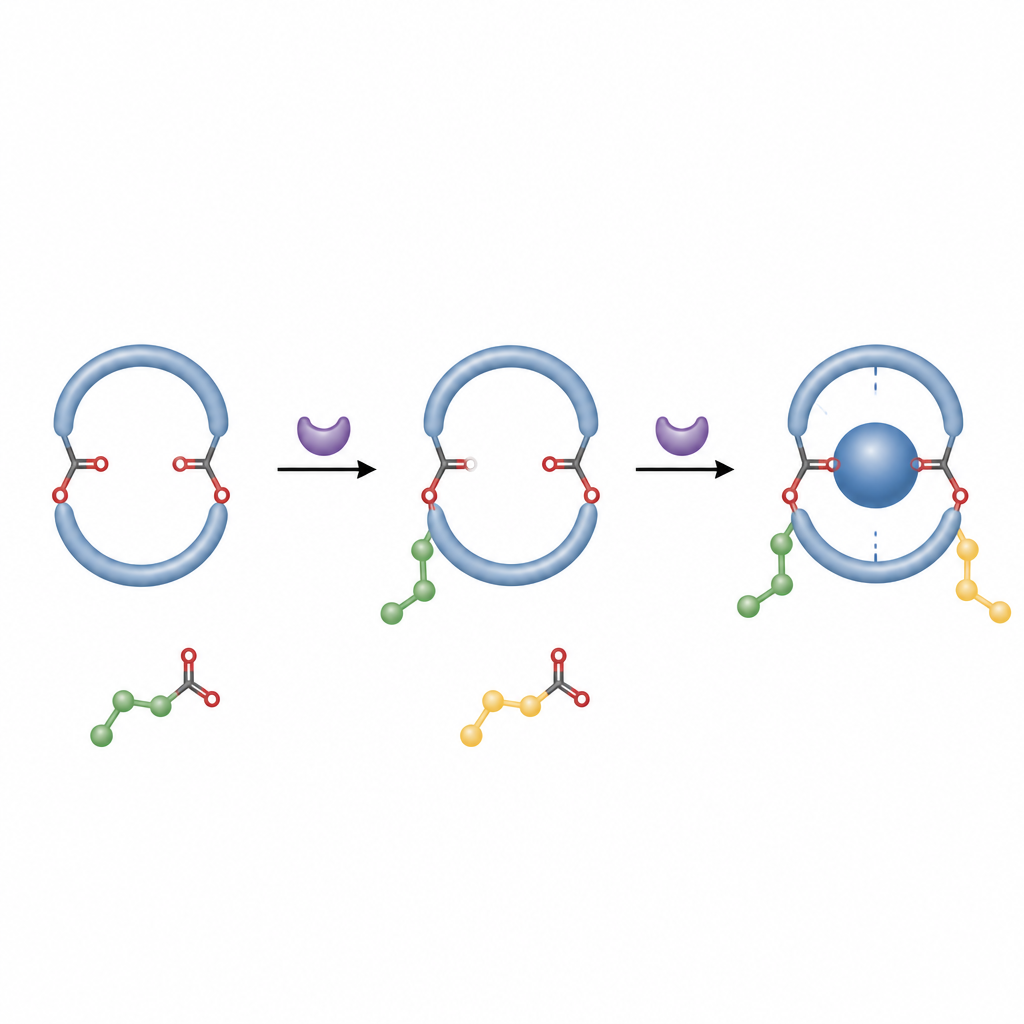
Qué significa esto para futuras máquinas moleculares
En términos cotidianos, los autores han encontrado una forma de fijar un anillo molecular en una pose izquierda o derecha usando un proceso simple y libre de metales. Esto facilita mucho la preparación de hospedadores puros y definidos en forma que pueden sujetar otras moléculas de maneras predecibles. Ese control sobre la quiralidad y la estabilidad es importante para diseñar materiales responsivos, sensores quirales y dispositivos moleculares, y esta sencilla doble esterificación ofrece una ruta práctica hacia esas estructuras avanzadas.
Cita: Dočekal, V., Hladík, O., Lóška, L. et al. Carbene-catalyzed double esterification enables enantioselective conformational self-locking of pillar[5]arenes. Nat Commun 17, 4253 (2026). https://doi.org/10.1038/s41467-026-70809-1
Palabras clave: pillararenos, organocatálisis, hospedadores quirales, esterificación, química supramolecular