Clear Sky Science · de
Carben-katalysierte doppelte Veresterung ermöglicht enantioselektives konformationelles Selbstverriegeln von Pillar[5]arenen
Formung winziger Ringe für intelligente Materialien
Chemiker lernen, Moleküle fast so präzise zu gestalten, wie Uhrmacher Zahnräder formen. Diese Studie zeigt, wie man ein kleines ringförmiges Molekül mithilfe eines einfachen Katalysators und gängiger Bausteine in einer handähnlichen Konformation „verriegeln“ kann. Da solche Ringe andere Moleküle aufnehmen können, könnte diese neue Formkontrolle künftige Sensoren, Materialien und medizinische Werkzeuge beeinflussen.
Warum die Form eines Rings wichtig ist
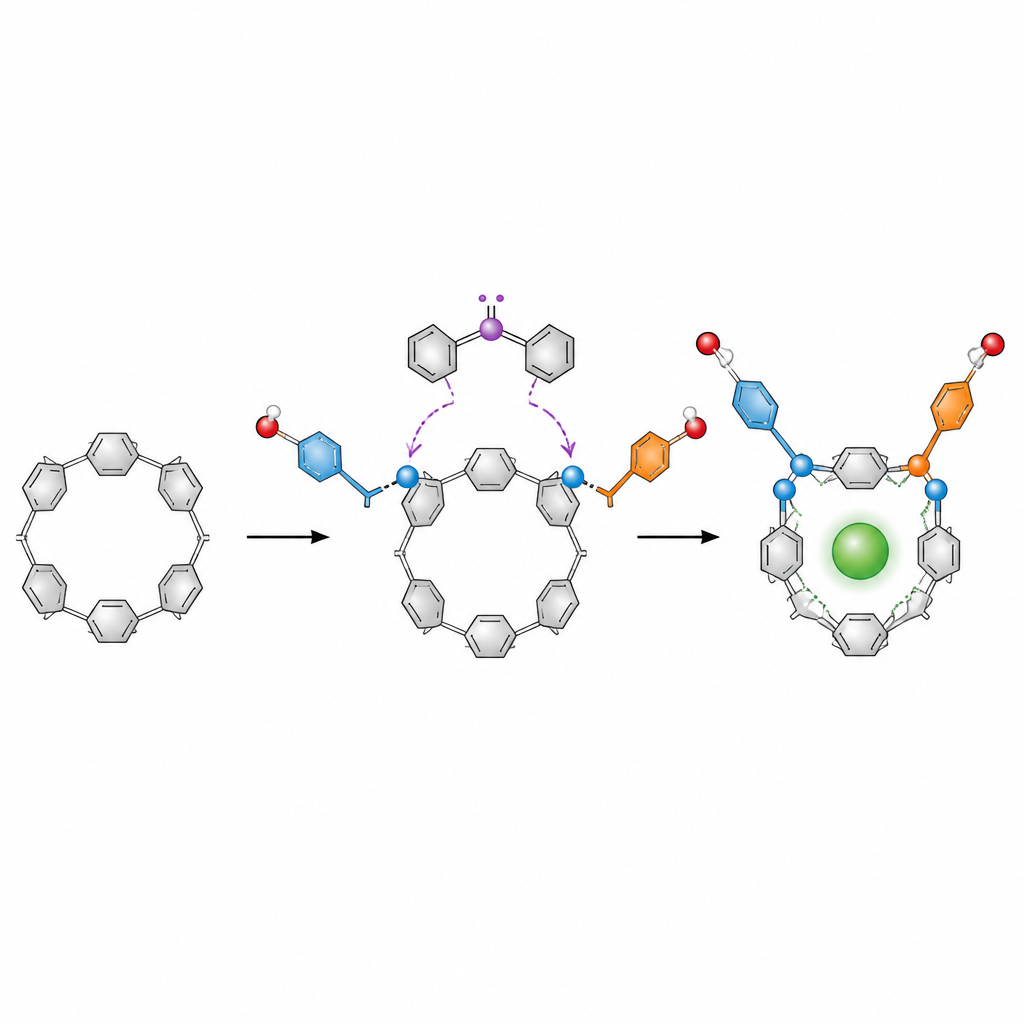
Die Protagonisten sind Pillar[5]arene, donutähnliche Ringe, die aus fünf sich wiederholenden aromatischen Einheiten aufgebaut sind. Diese Ringe sind in der Wirt‑Gast‑Chemie populär, wo sie als winzige Behälter für Ionen, Wirkstoffe oder Farbstoffe fungieren. Auf dem Papier kann sich ein Pillar[5]aren in mehrere spiegelbildliche Formen verdrehen, die hin und her tauschen. Um sie als präzise Werkzeuge einzusetzen, müssen Chemiker eine „händige“ Form einfrieren und ein Spiegelbild gegenüber dem anderen anreichern, doch bestehende Methoden beruhen häufig auf Metallen, mehreren Schritten und mühsamer Trennung von Gemischen.
Eine metallfreie Abkürzung zu verriegelten Ringen
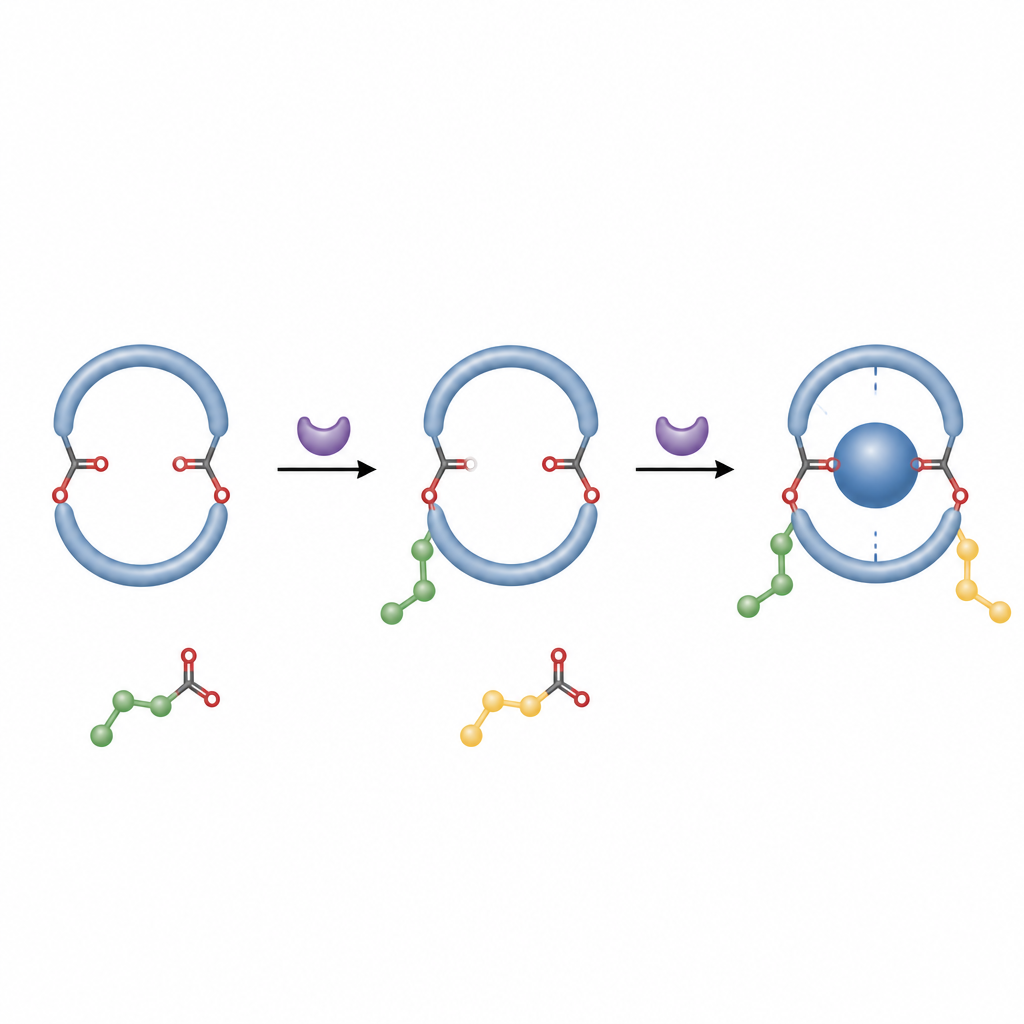
Die Autoren entwickelten einen deutlich einfacheren Ansatz auf Basis der Organokatalyse, bei der kleine organische Moleküle statt Metallen Reaktionen steuern. Ausgehend von einem diformylierten Pillar[5]aren — einer Ringversion mit zwei reaktiven Aldehydgruppen — führen ein chiraler Carben‑Katalysator, ein Oxidationsmittel und eine Base zu einer doppelten Veresterung mit aromatischen Alkoholen wie Naphtholen. Jede Reaktion heftet einen Ester‑„Arm“ an den Ring. Sobald zwei sperrige Arme angebracht sind, kann der Ring nicht mehr frei drehen, sodass eine chirale Form fixiert und stark bevorzugt wird.
Die Reichweite der Reaktion abstimmen
Durch systematische Tests fand das Team Bedingungen, die sowohl hohe Ausbeuten als auch starke Präferenz für ein Spiegelbild liefern. Sie untersuchten, wie die Natur des Katalysators, Lösungsmittels, der Base und des Oxidationsmittels das Ergebnis beeinflusst, und stellten fest, dass Natriumacetat in Dichlormethan bei moderater Temperatur besonders gut funktioniert. Der Prozess toleriert viele verschiedene aromatische Partner, einschließlich Naphthole mit elektronenspende- oder -ziehenden Gruppen sowie eine Reihe von Phenolen. Mithilfe einer geschickten sterischen Analyse zeigten sie, dass nur Substituenten, die lang und sperrig genug sind, wirklich verhindern, dass der Ring kippt — was erklärt, warum kleine Gruppen wie Methyl keine stabilen chiralen Produkte liefern.
Von einfachen Ringen zu komplexen Gästen
Das Verfahren geht über einfache Bausteine hinaus. Die Forscher hefteten erfolgreich Fragmente aus natürlichen und bioaktiven Molekülen an, etwa Estron und das cholesterinsenkende Medikament Ezetimib, und bewahrten dabei eine hohe Kontrolle über die „Händigkeit“. Sie zeigten weiter, dass die verriegelten Ringe Hitze und chemische Modifikation standhalten, ohne ihre chirale Reinheit zu verlieren. Im Grammmaßstab bildet sich das Schlüsselprodukt beinahe quantitativ. Zusätzliche Reaktionen an verbleibenden Funktionalitäten erzeugen komplexere Strukturen, darunter ein Rotaxan, bei dem ein hantelförmiges Molekül durch den Pillar[5]aren‑Ring aufgefädelt und durch sperrige Stopper eingeschlossen wird.
Was das für künftige molekulare Maschinen bedeutet
Alltagsgemäß haben die Autoren eine Möglichkeit gefunden, einen Molekülring mittels eines einfachen, metallfreien Verfahrens in eine feste links- oder rechtsdrehende Pose zu bringen. Das erleichtert die Herstellung reiner, formdefinierter Wirte, die andere Moleküle auf vorhersehbare Weise greifen können. Solche Kontrolle über Händigkeit und Stabilität ist wichtig für die Gestaltung reaktiver Materialien, chiraler Sensoren und molekularer Geräte — und diese unkomplizierte doppelte Veresterung bietet einen praktische neuen Zugang zu diesen fortgeschrittenen Strukturen.
Zitation: Dočekal, V., Hladík, O., Lóška, L. et al. Carbene-catalyzed double esterification enables enantioselective conformational self-locking of pillar[5]arenes. Nat Commun 17, 4253 (2026). https://doi.org/10.1038/s41467-026-70809-1
Schlüsselwörter: pillararenes, organokatalyse, chirale Wirte, Veresterung, supramolekulare Chemie